A François Jacob és Jacques Monod által használt kísérleti mikroorganizmus a közönséges laboratóriumi baktérium, az E. coli volt, de a Jacob és Monod által felfedezett alapvető szabályozási koncepciók közül sok alapvető fontosságú a sejtek szabályozásában minden szervezetben. A kulcsgondolat az, hogy a fehérjék nem szintetizálódnak, ha nincs rájuk szükség – a E. coli úgy takarékoskodik a sejt erőforrásaival és energiájával, hogy nem gyártja a három Lac fehérjét, ha nincs szükség a laktóz metabolizálására, például ha más cukrok, például glükóz áll rendelkezésre. A következő szakasz azt tárgyalja, hogy az E. coli hogyan vezérel bizonyos géneket az anyagcsere-szükségletek függvényében.
A második világháború alatt Monod a cukrok kombinációinak hatását vizsgálta az E. coli és a B. subtilis számára tápanyagforrásként. Monod más tudósok által baktériumokkal és élesztőgombákkal végzett hasonló vizsgálatokat követett. Megállapította, hogy a két különböző cukorral termesztett baktériumok gyakran két növekedési fázist mutattak. Ha például glükózt és laktózt is kaptak, először a glükózt (I. növekedési fázis, lásd a 2. ábrát), majd a laktózt (II. növekedési fázis) metabolizálták. A laktóz nem metabolizálódott a diaux növekedési görbe első szakaszában, mivel a β-galaktozidáz nem készült, amikor glükóz és laktóz is jelen volt a közegben. Monod ezt a jelenséget diauxiának nevezte el.

Monod ezután figyelmét a β-galaktozidáz képződés indukciójára összpontosította, amely akkor következett be, amikor a laktóz volt az egyetlen cukor a táptalajban.
A szabályozó mutánsok osztályozásaSzerkesztés
Jacob és Monod koncepcionális áttörése az volt, hogy felismerte a különbséget a szabályozó anyagok és azok között a helyek között, ahol azok a génexpresszió megváltoztatására hatnak. Jacob, aki korábban katona volt, egy olyan bombázó analógiáját használta, amely egy speciális rádióadás vagy jel fogadásakor szabadítja fel halálos rakományát. A működő rendszerhez egy földi adóra és egy vevőre van szükség a repülőgépben. Most tegyük fel, hogy a szokásos adó elromlott. Ezt a rendszert egy második, működőképes adó bevezetésével lehet működésre bírni. Ezzel szemben – mondta – tekintsünk egy bombázót, amelynek a vevője meghibásodott. Ennek a bombázónak a viselkedését nem lehet megváltoztatni egy második, működőképes repülőgép bevezetésével.”
A lac operon szabályozó mutánsainak elemzésére Jacob kifejlesztett egy olyan rendszert, amellyel a lac gének második példányát (lacI a promóterével, illetve lacZYA a promóterével és operátorával) be lehetett vinni egyetlen sejtbe. Az ilyen, a lac-gének szempontjából diploid, de egyébként normális baktériumkultúrát ezután a szabályozó fenotípus szempontjából vizsgálják. Különösen azt határozzák meg, hogy a LacZ és a LacY IPTG hiányában is keletkezik-e (mivel a mutáns gén által termelt laktózrepresszor nem működik). Ezt a kísérletet, amelyben a géneket vagy géncsoportokat páronként vizsgáljuk, komplementációs tesztnek nevezzük.
Ezt a tesztet az ábra szemlélteti (a lacA-t az egyszerűség kedvéért kihagytuk). Először bizonyos haploid állapotokat mutatunk be (azaz a sejt a lac géneknek csak egyetlen példányát hordozza). Az a) panel a repressziót, a b) az IPTG-vel történő indukciót, a c) és d) pedig a lacI gén, illetve az operátor mutációjának hatását mutatja. Az (e) panelen a represszor komplementációs tesztje látható. Ha a lac gének egyik példánya a lacI mutációját hordozza, de a másik példány vad típusú a lacI tekintetében, akkor a kapott fenotípus normális – de a lacZ kifejeződik, ha az induktor IPTG-nek van kitéve. A represszort érintő mutációkról azt mondják, hogy a vad típushoz képest recesszívek (és hogy a vad típus domináns), és ezt azzal magyarázzák, hogy a represszor egy kis fehérje, amely képes diffundálni a sejtben. A lac operonnak a hibás lacI gén melletti példányát a lacI második példányából termelt fehérje hatékonyan kikapcsolja.
Ha ugyanezt a kísérletet operátor mutációval végezzük, más eredményt kapunk (f panel). Az egy mutáns és egy vad típusú operátorhelyet hordozó sejt fenotípusa az, hogy a LacZ és LacY még az induktor IPTG hiányában is termelődik; mivel a sérült operátorhely, nem teszi lehetővé a represszor kötődését, hogy gátolja a szerkezeti gének transzkripcióját. Az operátor mutáció domináns. Ha az operátorhely, ahol a represszornak kötődnie kell, mutációval sérült, egy második funkcionális hely jelenléte ugyanabban a sejtben nem változtat a mutáns hely által szabályozott gének expresszióján.
A kísérlet kifinomultabb változata jelzett operonokat használ a lac gének két példányának megkülönböztetésére, és megmutatja, hogy a nem szabályozott strukturális gén(ek) a mutáns operátor melletti gén(ek) (g panel). Tegyük fel például, hogy az egyik példányt a lacZ-t inaktiváló mutáció jelöli, így csak a LacY fehérjét képes termelni, míg a második példány a lacY-t érintő mutációt hordoz, és csak LacZ-t képes termelni. Ebben a változatban a lac operonnak csak a mutáns operátorral szomszédos példánya fejeződik ki IPTG nélkül. Azt mondjuk, hogy az operátor mutációja cisz-domináns, a vad típushoz képest domináns, de csak az operonnak a vele közvetlenül szomszédos példányát érinti.
Ez a magyarázat egy fontos értelemben félrevezető, mert a kísérlet leírásából indul ki, majd az eredményeket egy modellel magyarázza. Valójában azonban gyakran igaz, hogy a modell áll előbb, és a kísérletet kifejezetten a modell tesztelésére alakítják ki. Jacob és Monod először azt képzelték el, hogy a DNS-ben kell lennie egy olyan helynek, amely rendelkezik az operátor tulajdonságaival, majd ennek kimutatására tervezték meg a komplementációs tesztjeiket.
Az operátor mutánsok dominanciája egy olyan eljárást is sugall, amellyel célzottan kiválaszthatók. Ha a regulátor mutánsokat fenil-Gal segítségével szelektáljuk a vad típusú kultúrából, a fent leírtak szerint, az operátor mutációk ritkák a represszor mutánsokhoz képest, mert a célpont mérete olyan kicsi. Ha azonban ehelyett olyan törzzsel kezdünk, amely a teljes lac régió két példányát hordozza (azaz diploid a lac számára), a represszor mutációk (amelyek még mindig előfordulnak) nem nyerhetők ki, mert a második, vad típusú lacI gén általi komplementáció vad típusú fenotípust kölcsönöz. Ezzel szemben az operátor egyik példányának mutációja mutáns fenotípust kölcsönöz, mert domináns a második, vad típusú példányhoz képest.
A ciklikus AMPEdit szabályozása
A diauxia magyarázata a lac génekre ható további, a klasszikus modell által magyarázottaktól eltérő mutációk jellemzésétől függött. Később két másik gént, a cya-t és a crp-t azonosították, amelyek messze a lac-től térképeződtek le, és amelyek mutációjuk esetén csökkent expressziós szintet eredményeznek IPTG jelenlétében, sőt a represszort vagy operátort nélkülöző baktériumtörzsekben is. A cAMP felfedezése az E. coli-ban annak kimutatásához vezetett, hogy a cya gén hibás mutánsai, de a crp gén nem, a közegbe cAMP hozzáadásával visszaállítható a teljes aktivitás.
A cya gén kódolja az adenilát-ciklázt, amely cAMP-ot termel. A cya mutánsban a cAMP hiánya miatt a lacZYA gének expressziója több mint tízszer alacsonyabb a normálisnál. A cAMP hozzáadása korrigálja a cya mutánsokra jellemző alacsony Lac expressziót. A második gén, a crp egy katabolit aktivátor protein (CAP) vagy cAMP receptor protein (CRP) nevű fehérjét kódol.
A laktóz anyagcsere enzimek azonban glükóz és laktóz jelenlétében is kis mennyiségben keletkeznek (ezt néha szivárgó expressziónak nevezik), ami annak köszönhető, hogy a LacI represszor gyorsan asszociál/dissociál a DNS-hez, ahelyett, hogy szorosan kötődne hozzá, ami időt adhat az RNAP-nak a lacZYA mRNS-ek megkötésére és átírására. A szivárgó expresszióra azért van szükség, hogy a glükózforrás kimerülése után, de a lac expresszió teljes aktiválódása előtt lehetővé váljon némi laktóz metabolizmusa.
Összefoglalva:
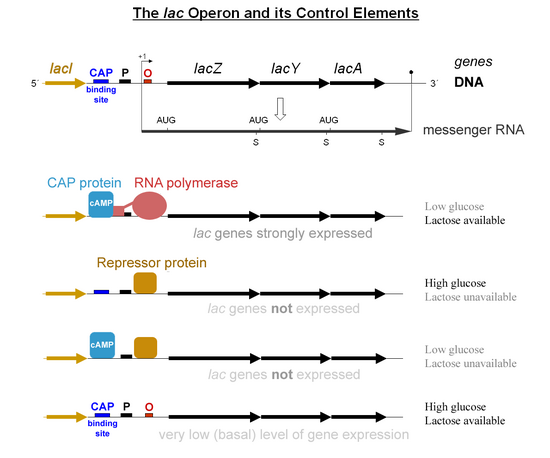
- Amikor nincs laktóz, akkor nagyon kevés Lac enzim termelődik (az operátorhoz Lac represszor kötődik).
- Ha a laktóz jelen van, de egy preferált szénforrás (pl. glükóz) is jelen van, akkor kis mennyiségű enzim termelődik (a Lac represszor nem kötődik az operátorhoz).
- Ha nincs glükóz, a CAP-cAMP a promóter előtt egy specifikus DNS-helyhez kötődik, és közvetlen fehérje-fehérje kölcsönhatást létesít az RNAP-pal, ami megkönnyíti az RNAP kötődését a promóterhez.
A növekedési fázisok közötti késés azt az időt tükrözi, ami a laktóz-metabolizáló enzimek megfelelő mennyiségű előállításához szükséges. Először a CAP szabályozó fehérjének kell összeállnia a lac promóteren, ami a lac mRNS termelésének növekedését eredményezi. A lac mRNS több rendelkezésre álló példánya a LacZ (β-galaktozidáz, a laktóz metabolizmushoz) és a LacY (laktózpermeáz a laktóz sejtbe szállítására) lényegesen több példányának termelését (lásd a transzlációt) eredményezi. A laktózt metabolizáló enzimek szintjének növeléséhez szükséges késleltetés után a baktériumok a sejtnövekedés új, gyors fázisába lépnek.
A katabolit-represszió két rejtélye azzal kapcsolatos, hogy a cAMP-szint hogyan kapcsolódik a glükóz jelenlétéhez, másodszor pedig azzal, hogy miért kell a sejteknek egyáltalán vesződniük. A laktóz hasítása után valójában glükóz és galaktóz (könnyen glükózzá alakítható) képződik belőle. Anyagcsere szempontjából a laktóz ugyanolyan jó szén- és energiaforrás, mint a glükóz. A cAMP-szint nem az intracelluláris glükózkoncentrációval, hanem a glükóztranszport sebességével függ össze, ami befolyásolja az adenilát-cikláz aktivitását. (Ezenkívül a glükóztranszport a laktózpermeáz közvetlen gátlásához is vezet.) Hogy miért működik így az E. coli, arról csak találgatni lehet. Minden bélbaktérium fermentálja a glükózt, ami arra utal, hogy gyakran találkoznak vele. Lehetséges, hogy a glükóz v. laktóz transzportjának vagy metabolizmusának hatékonysága közötti kis különbség miatt a sejtek számára előnyös a lac-operon ilyen módon történő szabályozása.