El microorganismo experimental utilizado por François Jacob y Jacques Monod fue la bacteria común de laboratorio, E. coli, pero muchos de los conceptos reguladores básicos que descubrieron Jacob y Monod son fundamentales para la regulación celular en todos los organismos. La idea clave es que las proteínas no se sintetizan cuando no son necesarias: E. coli conserva los recursos celulares y la energía al no fabricar las tres proteínas Lac cuando no hay necesidad de metabolizar la lactosa, como cuando hay otros azúcares como la glucosa. La siguiente sección analiza cómo E. coli controla ciertos genes en respuesta a las necesidades metabólicas.
Durante la Segunda Guerra Mundial, Monod estaba probando los efectos de las combinaciones de azúcares como fuentes de nutrientes para E. coli y B. subtilis. Monod estaba haciendo un seguimiento de estudios similares que habían realizado otros científicos con bacterias y levaduras. Descubrió que las bacterias cultivadas con dos azúcares diferentes solían mostrar dos fases de crecimiento. Por ejemplo, si se les suministraba glucosa y lactosa, primero se metabolizaba la glucosa (fase de crecimiento I, véase la figura 2) y luego la lactosa (fase de crecimiento II). La lactosa no se metabolizaba durante la primera parte de la curva de crecimiento diauxica porque la β-galactosidasa no se producía cuando tanto la glucosa como la lactosa estaban presentes en el medio. Monod denominó a este fenómeno diauxie.

Monod centró entonces su atención en la inducción de la formación de β-galactosidasa que se producía cuando la lactosa era el único azúcar en el medio de cultivo.
Clasificación de los mutantes reguladoresEditar
Un avance conceptual de Jacob y Monod fue reconocer la distinción entre las sustancias reguladoras y los sitios donde actúan para cambiar la expresión de los genes. Jacob, antiguo militar, utilizó la analogía de un bombardero que liberaría su carga letal al recibir una transmisión o señal de radio especial. Un sistema que funcione requiere un transmisor en tierra y un receptor en el avión. Ahora bien, supongamos que el transmisor habitual está averiado. Este sistema puede hacerse funcionar mediante la introducción de un segundo transmisor funcional. Por el contrario, dijo, considere un bombardero con un receptor defectuoso. El comportamiento de este bombardero no puede cambiarse mediante la introducción de un segundo avión funcional.
Para analizar los mutantes reguladores del operón lac, Jacob desarrolló un sistema mediante el cual se podía introducir una segunda copia de los genes lac (lacI con su promotor, y lacZYA con promotor y operador) en una sola célula. A continuación, se comprueba el fenotipo regulador de un cultivo de estas bacterias, que son diploides para los genes lac, pero que por lo demás son normales. En particular, se determina si LacZ y LacY se producen incluso en ausencia de IPTG (debido a que el represor de la lactosa producido por el gen mutante no es funcional). Este experimento, en el que se prueban genes o grupos de genes por parejas, se denomina prueba de complementación.
Esta prueba se ilustra en la figura (se omite lacA para simplificar). En primer lugar, se muestran ciertos estados haploides (es decir, la célula lleva una sola copia de los genes lac). El panel (a) muestra la represión, (b) muestra la inducción por IPTG, y (c) y (d) muestran el efecto de una mutación en el gen lacI o en el operador, respectivamente. En el panel (e) se muestra la prueba de complementación para el represor. Si una copia de los genes lac lleva una mutación en lacI, pero la segunda copia es de tipo salvaje para lacI, el fenotipo resultante es normal, pero lacZ se expresa cuando se expone al inductor IPTG. Se dice que las mutaciones que afectan al represor son recesivas con respecto al tipo salvaje (y que el tipo salvaje es dominante), y esto se explica por el hecho de que el represor es una proteína pequeña que puede difundirse en la célula. La copia del operón lac adyacente al gen lacI defectuoso está efectivamente apagada por la proteína producida a partir de la segunda copia de lacI.
Si se realiza el mismo experimento utilizando una mutación del operador, se obtiene un resultado diferente (panel (f)). El fenotipo de una célula que lleva un sitio operador mutante y otro de tipo salvaje es que LacZ y LacY se producen incluso en ausencia del inductor IPTG; porque el sitio operador dañado, no permite la unión del represor para inhibir la transcripción de los genes estructurales. La mutación del operador es dominante. Cuando el sitio operador donde debe unirse el represor está dañado por la mutación, la presencia de un segundo sitio funcional en la misma célula no supone ninguna diferencia en la expresión de los genes controlados por el sitio mutante.
Una versión más sofisticada de este experimento utiliza operones marcados para distinguir entre las dos copias de los genes lac y mostrar que el(los) gen(es) estructural(es) no regulado(s) es(son) el(los) que está(n) junto al operador mutante (panel (g). Por ejemplo, supongamos que una copia está marcada por una mutación que inactiva lacZ de modo que sólo puede producir la proteína LacY, mientras que la segunda copia lleva una mutación que afecta a lacY y sólo puede producir LacZ. En esta versión, sólo la copia del operón lac que es adyacente al operador mutante se expresa sin IPTG. Decimos que la mutación del operador es cis-dominante, es dominante para el tipo salvaje pero afecta sólo a la copia del operón que es inmediatamente adyacente a él.
Esta explicación es engañosa en un sentido importante, porque procede de una descripción del experimento y luego explica los resultados en términos de un modelo. Pero de hecho, a menudo es cierto que el modelo viene primero, y un experimento está diseñado específicamente para probar el modelo. Jacob y Monod primero imaginaron que debía haber un sitio en el ADN con las propiedades del operador, y luego diseñaron sus pruebas de complementación para demostrarlo.
La dominancia de los mutantes del operador también sugiere un procedimiento para seleccionarlos específicamente. Si los mutantes reguladores se seleccionan a partir de un cultivo de tipo salvaje utilizando fenil-Gal, como se ha descrito anteriormente, las mutaciones del operador son raras en comparación con los mutantes del represor porque el tamaño del objetivo es muy pequeño. Pero si, en cambio, partimos de una cepa que lleva dos copias de toda la región lac (es decir, diploide para lac), las mutaciones represoras (que aún se producen) no se recuperan porque la complementación por el segundo gen lacI de tipo salvaje confiere un fenotipo de tipo salvaje. Por el contrario, la mutación de una copia del operador confiere un fenotipo mutante porque es dominante con respecto a la segunda copia de tipo salvaje.
Regulación por AMP cíclicoEditar
La explicación de la diauxie dependía de la caracterización de mutaciones adicionales que afectaban a los genes lac distintas de las explicadas por el modelo clásico. Posteriormente se identificaron otros dos genes, cya y crp, que se mapean lejos de lac y que, al mutar, dan lugar a una disminución del nivel de expresión en presencia de IPTG e incluso en cepas de la bacteria que carecen del represor u operador. El descubrimiento del AMPc en E. coli condujo a la demostración de que los mutantes defectuosos del gen cya, pero no del gen crp, podían recuperar su plena actividad mediante la adición de AMPc al medio.
El gen cya codifica la adenilato ciclasa, que produce AMPc. En un mutante cya, la ausencia de AMPc hace que la expresión de los genes lacZYA sea más de diez veces inferior a la normal. La adición de AMPc corrige la baja expresión de Lac característica de los mutantes cya. El segundo gen, crp, codifica una proteína llamada proteína activadora de catabolitos (CAP) o proteína receptora de AMPc (CRP).
Sin embargo, las enzimas del metabolismo de la lactosa se producen en pequeñas cantidades en presencia tanto de glucosa como de lactosa (lo que a veces se denomina expresión con fugas) debido a que el represor LacI se asocia/disocia rápidamente del ADN en lugar de unirse fuertemente a él, lo que puede dar tiempo a que la RNAP se una y transcriba los ARNm de lacZYA. La expresión de lac es necesaria para permitir el metabolismo de algo de lactosa después de que se agote la fuente de glucosa, pero antes de que la expresión de lac se active por completo.
En resumen:
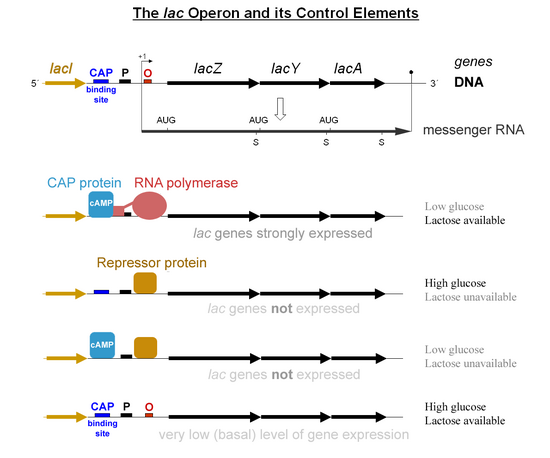
- Cuando la lactosa está ausente, hay muy poca producción de la enzima Lac (el operador tiene el represor Lac unido a él).
- Cuando la lactosa está presente pero una fuente de carbono preferida (como la glucosa) también está presente entonces se produce una pequeña cantidad de enzima (el represor Lac no está unido al operador).
- Cuando la glucosa está ausente, CAP-cAMP se une a un sitio específico del ADN aguas arriba del promotor y hace una interacción directa proteína-proteína con RNAP que facilita la unión de RNAP al promotor.
El retraso entre las fases de crecimiento refleja el tiempo necesario para producir cantidades suficientes de enzimas que metabolizan la lactosa. En primer lugar, la proteína reguladora CAP tiene que ensamblarse en el promotor lac, lo que resulta en un aumento de la producción de ARNm lac. Un mayor número de copias disponibles del ARNm lac da lugar a la producción (véase la traducción) de un número significativamente mayor de copias de LacZ (β-galactosidasa, para el metabolismo de la lactosa) y LacY (permeasa de la lactosa para transportarla al interior de la célula). Después de un retraso necesario para aumentar el nivel de las enzimas metabolizadoras de la lactosa, las bacterias entran en una nueva fase rápida de crecimiento celular.
Dos rompecabezas de la represión de catabolitos se relacionan con la forma en que los niveles de AMPc se acoplan a la presencia de glucosa, y en segundo lugar, por qué las células deberían siquiera molestarse. Después de que la lactosa se escinde, en realidad forma glucosa y galactosa (fácilmente convertida en glucosa). En términos metabólicos, la lactosa es tan buena fuente de carbono y energía como la glucosa. El nivel de AMPc no está relacionado con la concentración de glucosa intracelular, sino con la tasa de transporte de glucosa, que influye en la actividad de la adenilato ciclasa. (Además, el transporte de glucosa también provoca la inhibición directa de la permeasa de la lactosa). En cuanto a la razón por la que E. coli funciona así, sólo se puede especular. Todas las bacterias entéricas fermentan la glucosa, lo que sugiere que la encuentran con frecuencia. Es posible que una pequeña diferencia en la eficiencia del transporte o el metabolismo de la glucosa frente a la lactosa haga que sea ventajoso para las células regular el operón lac de esta manera.