Le micro-organisme expérimental utilisé par François Jacob et Jacques Monod était la bactérie de laboratoire commune, E. coli, mais beaucoup des concepts de régulation de base qui ont été découverts par Jacob et Monod sont fondamentaux pour la régulation cellulaire dans tous les organismes. L’idée clé est que les protéines ne sont pas synthétisées lorsqu’elles ne sont pas nécessaires – E. coli conserve les ressources cellulaires et l’énergie en ne fabriquant pas les trois protéines Lac lorsqu’il n’est pas nécessaire de métaboliser le lactose, par exemple lorsque d’autres sucres comme le glucose sont disponibles. La section suivante traite de la façon dont E. coli contrôle certains gènes en réponse aux besoins métaboliques.
Pendant la Seconde Guerre mondiale, Monod testait les effets de combinaisons de sucres comme sources nutritives pour E. coli et B. subtilis. Monod faisait suite à des études similaires qui avaient été menées par d’autres scientifiques avec des bactéries et des levures. Il a constaté que les bactéries cultivées avec deux sucres différents présentaient souvent deux phases de croissance. Par exemple, si l’on fournit du glucose et du lactose, le glucose est métabolisé en premier (phase de croissance I, voir figure 2), puis le lactose (phase de croissance II). Le lactose n’était pas métabolisé pendant la première partie de la courbe de croissance diauxique car la β-galactosidase n’était pas fabriquée lorsque le glucose et le lactose étaient tous deux présents dans le milieu. Monod a nommé ce phénomène diauxie.

Monod a ensuite porté son attention sur l’induction de la formation de β-galactosidase qui se produisait lorsque le lactose était le seul sucre du milieu de culture.
Classification des mutants régulateursModifié
Une avancée conceptuelle de Jacob et Monod a été de reconnaître la distinction entre les substances régulatrices et les sites où elles agissent pour modifier l’expression des gènes. Ancien soldat, Jacob a utilisé l’analogie d’un bombardier qui libérerait sa cargaison mortelle à la réception d’une transmission ou d’un signal radio spécial. Pour que le système fonctionne, il faut un émetteur au sol et un récepteur dans l’avion. Maintenant, supposons que l’émetteur habituel soit cassé. Il est possible de faire fonctionner ce système en introduisant un second émetteur fonctionnel. En revanche, dit-il, considérons un bombardier dont le récepteur est défectueux. Le comportement de ce bombardier ne peut être modifié par l’introduction d’un second avion fonctionnel.
Pour analyser les mutants régulateurs de l’opéron lac, Jacob a développé un système par lequel une seconde copie des gènes lac (lacI avec son promoteur, et lacZYA avec promoteur et opérateur) pouvait être introduite dans une seule cellule. Une culture de ces bactéries, qui sont diploïdes pour les gènes lac mais normales par ailleurs, est ensuite testée pour le phénotype de régulation. En particulier, on détermine si LacZ et LacY sont produits même en l’absence d’IPTG (en raison de la non-fonctionnalité du répresseur de lactose produit par le gène mutant). Cette expérience, dans laquelle les gènes ou les groupes de gènes sont testés par paire, est appelée test de complémentation.
Ce test est illustré dans la figure (lacA est omis pour plus de simplicité). Tout d’abord, certains états haploïdes sont montrés (c’est-à-dire que la cellule ne porte qu’une seule copie des gènes lac). Le panneau (a) montre la répression, (b) montre l’induction par IPTG, et (c) et (d) montrent l’effet d’une mutation du gène lacI ou de l’opérateur, respectivement. Dans le panneau (e), le test de complémentation pour le répresseur est montré. Si une copie des gènes lac porte une mutation du gène lacI, mais que la seconde copie est de type sauvage pour lacI, le phénotype résultant est normal, mais lacZ est exprimé lorsqu’il est exposé à l’inducteur IPTG. Les mutations affectant le répresseur sont dites récessives par rapport au type sauvage (et que le type sauvage est dominant), ce qui s’explique par le fait que le répresseur est une petite protéine qui peut se diffuser dans la cellule. La copie de l’opéron lac adjacente au gène lacI défectueux est effectivement éteinte par la protéine produite à partir de la seconde copie de lacI.
Si la même expérience est réalisée en utilisant une mutation opérateur, un résultat différent est obtenu (panneau (f)). Le phénotype d’une cellule portant un site opérateur mutant et un site opérateur de type sauvage est que LacZ et LacY sont produits même en l’absence de l’inducteur IPTG ; car le site opérateur endommagé, ne permet pas la liaison du répresseur pour inhiber la transcription des gènes de structure. La mutation de l’opérateur est dominante. Lorsque le site opérateur où doit se fixer le répresseur est endommagé par mutation, la présence d’un second site fonctionnel dans la même cellule ne fait aucune différence dans l’expression des gènes contrôlés par le site mutant.
Une version plus sophistiquée de cette expérience utilise des opérons marqués pour distinguer les deux copies des gènes lac et montrer que le ou les gènes structuraux non régulés sont ceux qui se trouvent à côté de l’opérateur mutant (panneau (g). Par exemple, supposons qu’une copie est marquée par une mutation inactivant lacZ de sorte qu’elle ne peut produire que la protéine LacY, tandis que la seconde copie porte une mutation affectant lacY et ne peut produire que LacZ. Dans cette version, seule la copie de l’opéron lac qui est adjacente à l’opérateur mutant est exprimée sans IPTG. On dit que la mutation de l’opérateur est cis-dominante, elle est dominante par rapport au type sauvage mais n’affecte que la copie de l’opéron qui lui est immédiatement adjacente.
Cette explication est trompeuse dans un sens important, car elle procède d’une description de l’expérience et explique ensuite les résultats en fonction d’un modèle. Mais en fait, il est souvent vrai que le modèle vient en premier, et qu’une expérience est façonnée spécifiquement pour tester le modèle. Jacob et Monod ont d’abord imaginé qu’il devait exister un site dans l’ADN ayant les propriétés de l’opérateur, puis ont conçu leurs tests de complémentation pour le démontrer.
La dominance des mutants opérateurs suggère également une procédure pour les sélectionner spécifiquement. Si les mutants régulateurs sont sélectionnés à partir d’une culture de type sauvage en utilisant le phényl-Gal, comme décrit ci-dessus, les mutations d’opérateurs sont rares par rapport aux mutants répresseurs parce que la taille de la cible est si petite. Mais si, au lieu de cela, nous commençons avec une souche qui porte deux copies de toute la région lac (c’est-à-dire diploïde pour lac), les mutations répresseurs (qui se produisent toujours) ne sont pas récupérées parce que la complémentation par le second gène lacI de type sauvage confère un phénotype de type sauvage. En revanche, la mutation d’une copie de l’opérateur confère un phénotype mutant car elle est dominante par rapport à la seconde copie de type sauvage.
Régulation par l’AMP cycliqueEdit
L’explication de la diauxie dépendait de la caractérisation de mutations supplémentaires affectant les gènes lac autres que celles expliquées par le modèle classique. Deux autres gènes, cya et crp, ont par la suite été identifiés qui se cartographient loin de lac, et qui, lorsqu’ils sont mutés, entraînent une diminution du niveau d’expression en présence d’IPTG et même dans des souches de la bactérie dépourvues du répresseur ou de l’opérateur. La découverte de l’AMPc chez E. coli a conduit à la démonstration que les mutants défectueux du gène cya mais pas du gène crp pouvaient retrouver leur pleine activité par l’ajout d’AMPc au milieu.
Le gène cya code pour l’adénylate cyclase, qui produit de l’AMPc. Chez un mutant cya, l’absence d’AMPc rend l’expression des gènes lacZYA plus de dix fois inférieure à la normale. L’ajout d’AMPc corrige la faible expression de lac caractéristique des mutants cya. Le second gène, crp, code une protéine appelée protéine activatrice de catabolite (CAP) ou protéine réceptrice de l’AMPc (CRP).
Cependant, les enzymes du métabolisme du lactose sont fabriquées en petites quantités en présence à la fois de glucose et de lactose (parfois appelée expression fuyante) en raison du fait que le répresseur LacI s’associe/dissocie rapidement de l’ADN plutôt que de s’y lier étroitement, ce qui peut laisser le temps à la RNAP de se lier et de transcrire les ARNm de lacZYA. L’expression de lac est nécessaire pour permettre le métabolisme d’une partie du lactose après que la source de glucose soit dépensée, mais avant que l’expression de lac soit complètement activée.
En résumé :
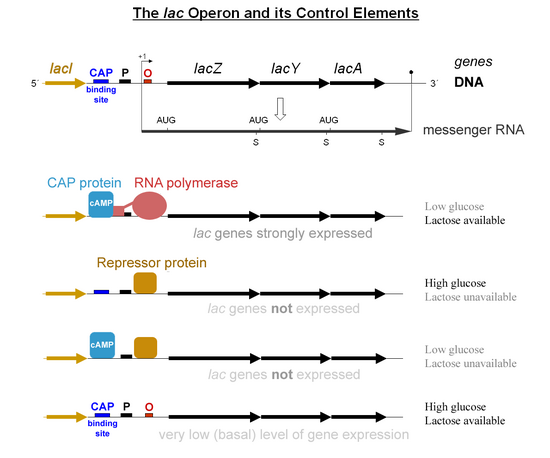
- Lorsque le lactose est absent alors il y a très peu de production d’enzyme Lac (l’opérateur a le répresseur Lac lié à lui).
- Lorsque le lactose est présent mais qu’une source de carbone préférée (comme le glucose) est également présente alors une petite quantité d’enzyme est produite (le répresseur Lac n’est pas lié à l’opérateur).
- Lorsque le glucose est absent, CAP-cAMP se lie à un site d’ADN spécifique en amont du promoteur et réalise une interaction protéine-protéine directe avec RNAP qui facilite la liaison de RNAP au promoteur.
Le délai entre les phases de croissance reflète le temps nécessaire pour produire des quantités suffisantes d’enzymes métabolisant le lactose. Tout d’abord, la protéine régulatrice CAP doit s’assembler sur le promoteur lac, ce qui entraîne une augmentation de la production de l’ARNm lac. Un plus grand nombre de copies disponibles de l’ARNm lac entraîne la production (voir traduction) de beaucoup plus de copies de LacZ (β-galactosidase, pour le métabolisme du lactose) et de LacY (lactose perméase pour transporter le lactose dans la cellule). Après un délai nécessaire pour augmenter le niveau des enzymes métabolisant le lactose, les bactéries entrent dans une nouvelle phase rapide de croissance cellulaire.
Deux énigmes de la répression des catabolites concernent la façon dont les niveaux d’AMPc sont couplés à la présence de glucose, et deuxièmement, pourquoi les cellules devraient même s’en soucier. Après que le lactose soit clivé, il forme en fait du glucose et du galactose (facilement converti en glucose). En termes métaboliques, le lactose est une source de carbone et d’énergie tout aussi bonne que le glucose. Le niveau d’AMPc n’est pas lié à la concentration intracellulaire de glucose mais à la vitesse du transport du glucose, qui influence l’activité de l’adénylate cyclase. (En outre, le transport du glucose entraîne également une inhibition directe de la perméase du lactose). Quant à savoir pourquoi E. coli fonctionne de cette manière, on ne peut que spéculer. Toutes les bactéries entériques fermentent le glucose, ce qui suggère qu’elles le rencontrent fréquemment. Il est possible qu’une petite différence dans l’efficacité du transport ou du métabolisme du glucose par rapport au lactose rende avantageux pour les cellules de réguler l’opéron lac de cette façon.