Mikroorganizmem doświadczalnym użytym przez François Jacoba i Jacquesa Monoda była zwykła bakteria laboratoryjna, E. coli, ale wiele z podstawowych koncepcji regulacyjnych odkrytych przez Jacoba i Monoda ma fundamentalne znaczenie dla regulacji komórkowej we wszystkich organizmach. Kluczową ideą jest to, że białka nie są syntetyzowane, gdy nie są potrzebne – E. coli oszczędza zasoby komórkowe i energię, nie wytwarzając trzech białek Lac, gdy nie ma potrzeby metabolizowania laktozy, np. gdy dostępne są inne cukry, takie jak glukoza. W dalszej części omówiono, w jaki sposób E. coli kontroluje pewne geny w odpowiedzi na potrzeby metaboliczne.
Podczas II wojny światowej Monod testował efekty kombinacji cukrów jako źródeł składników odżywczych dla E. coli i B. subtilis. Monod podążał za podobnymi badaniami, które były prowadzone przez innych naukowców z bakteriami i drożdżami. Odkrył on, że bakterie hodowane z dwoma różnymi cukrami często wykazywały dwie fazy wzrostu. Na przykład, jeśli dostarczono zarówno glukozę jak i laktozę, najpierw metabolizowana była glukoza (faza wzrostu I, patrz rysunek 2), a następnie laktoza (faza wzrostu II). Laktoza nie była metabolizowana podczas pierwszej części diauksycznej krzywej wzrostu, ponieważ β-galaktozydaza nie była wytwarzana, gdy zarówno glukoza, jak i laktoza były obecne w pożywce. Monod nazwał to zjawisko diauxie.

Monod skupił następnie swoją uwagę na indukcji tworzenia β-galaktozydazy, która zachodziła, gdy laktoza była jedynym cukrem w podłożu hodowlanym.
Klasyfikacja mutantów regulatorowychEdit
Koncepcyjnym przełomem Jacoba i Monoda było rozpoznanie rozróżnienia między substancjami regulatorowymi a miejscami, w których działają one w celu zmiany ekspresji genów. Jacob, były żołnierz, posłużył się analogią do bombowca, który uwalnia swój śmiercionośny ładunek po otrzymaniu specjalnej transmisji radiowej lub sygnału. Działający system wymaga zarówno nadajnika naziemnego, jak i odbiornika w samolocie. Załóżmy teraz, że zwykły nadajnik jest uszkodzony. System ten można uruchomić przez wprowadzenie drugiego, sprawnego nadajnika. Dla kontrastu, powiedział, rozważmy bombowiec z uszkodzonym odbiornikiem. Zachowanie tego bombowca nie może być zmienione przez wprowadzenie drugiego, funkcjonalnego samolotu.
Aby przeanalizować mutanty regulacyjne operonu lac, Jacob opracował system, za pomocą którego druga kopia genów lac (lacI z promotorem oraz lacZYA z promotorem i operatorem) może być wprowadzona do pojedynczej komórki. Hodowla takich bakterii, które są diploidalne dla genów lac, ale poza tym normalne, jest następnie badana pod kątem fenotypu regulacyjnego. W szczególności ustala się, czy LacZ i LacY są wytwarzane nawet przy braku IPTG (z powodu niefunkcjonalnego represora laktozy wytwarzanego przez zmutowany gen). Ten eksperyment, w którym geny lub grupy genów są testowane parami, nazywany jest testem komplementarności.
Test ten jest zilustrowany na rysunku (lacA jest pominięty dla uproszczenia). Po pierwsze, pokazane są pewne stany haploidalne (tzn. komórka nosi tylko jedną kopię genów lac). Panel (a) pokazuje represję, (b) pokazuje indukcję przez IPTG, a (c) i (d) pokazują efekt mutacji odpowiednio do genu lacI lub operatora. W panelu (e) pokazany jest test komplementarności dla represora. Jeśli jedna kopia genów lac nosi mutację w lacI, ale druga kopia jest typu dzikiego dla lacI, fenotyp jest normalny – ale lacZ ulega ekspresji, gdy jest wystawiony na działanie induktora IPTG. Mówi się, że mutacje wpływające na represor są recesywne w stosunku do typu dzikiego (i że typ dziki jest dominujący), co tłumaczy się tym, że represor jest małym białkiem, które może dyfundować w komórce. Kopia operonu lac sąsiadująca z uszkodzonym genem lacI jest efektywnie wyłączana przez białko produkowane z drugiej kopii lacI.
Jeśli ten sam eksperyment jest przeprowadzony z użyciem mutacji operatorowej, uzyskuje się inny wynik (panel (f)). Fenotyp komórki niosącej jedno zmutowane i jedno dzikie miejsce operatora jest taki, że LacZ i LacY są produkowane nawet przy braku induktora IPTG; ponieważ uszkodzone miejsce operatora, nie pozwala na wiązanie represora w celu zahamowania transkrypcji genów strukturalnych. Mutacja operatora jest dominująca. Kiedy miejsce operatora, gdzie represor musi się wiązać, jest uszkodzone przez mutację, obecność drugiego funkcjonalnego miejsca w tej samej komórce nie robi żadnej różnicy w ekspresji genów kontrolowanych przez zmutowane miejsce.
Bardziej wyrafinowana wersja tego eksperymentu wykorzystuje oznaczone operony, aby odróżnić dwie kopie genów lac i pokazać, że nieregulowany gen(y) strukturalny(e) jest(są) tym(i) obok zmutowanego operatora (panel (g). Na przykład, załóżmy, że jedna kopia jest oznaczona przez mutację inaktywującą lacZ, tak że może produkować tylko białko LacY, podczas gdy druga kopia nosi mutację wpływającą na lacY i może produkować tylko LacZ. W tej wersji, tylko ta kopia operonu lac, która sąsiaduje ze zmutowanym operatorem, ulega ekspresji bez IPTG. Mówimy, że mutacja operatora jest cis-dominująca, jest dominująca w stosunku do typu dzikiego, ale wpływa tylko na kopię operonu, która jest bezpośrednio z nią sąsiadująca.
To wyjaśnienie jest mylące w ważnym sensie, ponieważ wychodzi od opisu eksperymentu, a następnie wyjaśnia wyniki w kategoriach modelu. W rzeczywistości jednak często jest tak, że najpierw pojawia się model, a eksperyment jest tworzony specjalnie po to, by go przetestować. Jacob i Monod najpierw wyobrazili sobie, że musi istnieć miejsce w DNA z właściwościami operatora, a następnie zaprojektowali swoje testy komplementarne, aby to pokazać.
Dominacja mutantów operatora również sugeruje procedurę, aby wybrać je specjalnie. Jeśli mutanty regulatorowe są wybierane z hodowli typu dzikiego przy użyciu fenylo-Gal, jak opisano powyżej, mutacje operatorowe są rzadkie w porównaniu z mutacjami represorowymi, ponieważ rozmiar celu jest tak mały. Ale jeśli zamiast tego zaczniemy od szczepu, który niesie dwie kopie całego regionu lac (czyli diploidalnego dla lac), mutacje represorowe (które nadal występują) nie są odzyskiwane, ponieważ komplementacja przez drugi, dziki gen lacI nadaje fenotyp typu dzikiego. W przeciwieństwie do tego, mutacja jednej kopii operatora nadaje fenotyp mutanta, ponieważ jest dominująca w stosunku do drugiej kopii typu dzikiego.
Regulacja przez cykliczny AMPEdit
Wyjaśnienie diauxie zależało od scharakteryzowania dodatkowych mutacji wpływających na geny lac, innych niż te wyjaśnione przez model klasyczny. Następnie zidentyfikowano dwa inne geny, cya i crp, które mapują się daleko od lac, a których mutacje powodują obniżony poziom ekspresji w obecności IPTG, a nawet w szczepach bakterii pozbawionych represora lub operatora. Odkrycie cAMP w E. coli doprowadziło do wykazania, że mutanty z defektem genu cya, ale nie genu crp, mogą być przywrócone do pełnej aktywności przez dodanie cAMP do pożywki.
Gen cya koduje cyklazę adenylanową, która wytwarza cAMP. W mutancie cya, brak cAMP powoduje, że ekspresja genów lacZYA jest ponad dziesięciokrotnie niższa niż normalnie. Dodanie cAMP koryguje niską ekspresję Lac charakterystyczną dla mutantów cya. Drugi gen, crp, koduje białko zwane białkiem aktywatora katabolitu (CAP) lub białkiem receptora cAMP (CRP).
Jednakże enzymy metabolizmu laktozy są wytwarzane w niewielkich ilościach w obecności zarówno glukozy, jak i laktozy (czasami nazywane ekspresją nieszczelną) ze względu na fakt, że represor LacI szybko asocjuje/dysocjuje z DNA, zamiast ściśle się z nim wiązać, co może zapewnić czas dla RNAP na związanie i transkrypcję mRNA genów lacZYA. Nieszczelna ekspresja jest konieczna, aby umożliwić metabolizm pewnej ilości laktozy po wyczerpaniu źródła glukozy, ale zanim ekspresja lac zostanie w pełni aktywowana.
Podsumowując:
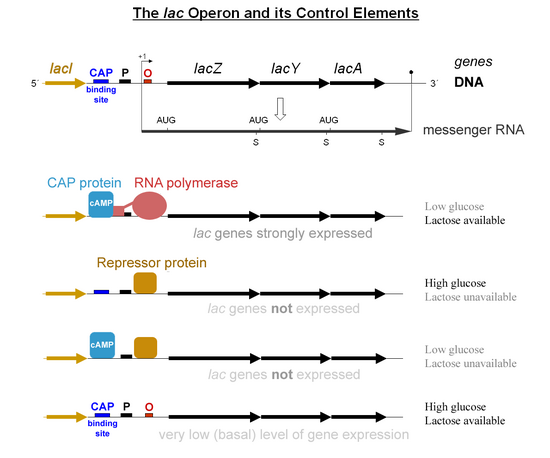
- Gdy laktoza jest nieobecna, wtedy jest bardzo mało produkcji enzymu Lac (operator ma represor Lac związany z nim).
- Gdy laktoza jest obecna, ale preferowane źródło węgla (jak glukoza) jest również obecne, wtedy produkowana jest niewielka ilość enzymu (represor Lac nie jest związany z operatorem).
- Gdy glukoza jest nieobecna, CAP-cAMP wiąże się ze specyficznym miejscem DNA powyżej promotora i tworzy bezpośrednią interakcję białko-białko z RNAP, która ułatwia wiązanie RNAP do promotora.
Opóźnienie między fazami wzrostu odzwierciedla czas potrzebny do wytworzenia wystarczającej ilości enzymów metabolizujących laktozę. Po pierwsze, białko regulatorowe CAP musi zgromadzić się na promotorze lac, co powoduje wzrost produkcji lac mRNA. Więcej dostępnych kopii lac mRNA skutkuje produkcją (patrz translacja) znacznie większej ilości kopii LacZ (β-galaktozydaza, do metabolizmu laktozy) i LacY (permeaza laktozowa do transportu laktozy do komórki). Po opóźnieniu potrzebnym do zwiększenia poziomu enzymów metabolizujących laktozę, bakterie wchodzą w nową, szybką fazę wzrostu komórek.
Dwie zagadki represji katabolitów dotyczą tego, jak poziomy cAMP są sprzężone z obecnością glukozy, a po drugie, dlaczego komórki w ogóle powinny się tym przejmować. Po rozszczepieniu laktozy faktycznie tworzy glukozę i galaktozę (łatwo przekształcaną w glukozę). W kategoriach metabolicznych laktoza jest tak samo dobrym źródłem węgla i energii jak glukoza. Poziom cAMP jest związany nie z wewnątrzkomórkowym stężeniem glukozy, ale z szybkością transportu glukozy, co wpływa na aktywność cyklazy adenylanowej. (Dodatkowo, transport glukozy prowadzi również do bezpośredniego hamowania permeazy laktozy). Co do tego, dlaczego E. coli działa w ten sposób, można tylko spekulować. Wszystkie bakterie jelitowe fermentują glukozę, co sugeruje, że często się z nią stykają. Możliwe, że niewielka różnica w wydajności transportu lub metabolizmu glukozy w stosunku do laktozy sprawia, że dla komórek korzystne jest regulowanie operonu lac w ten sposób.