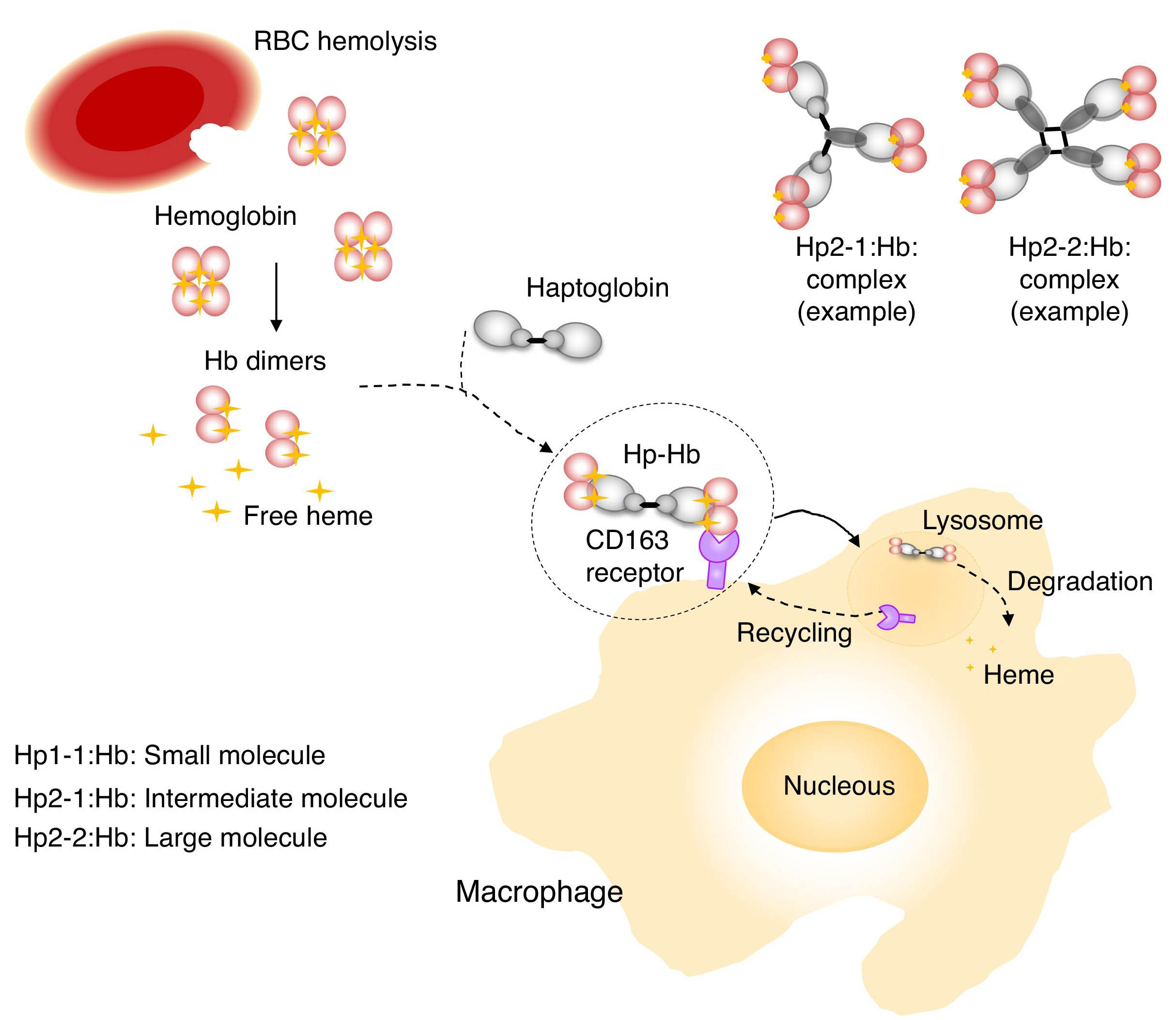
L’aptoglobina si lega all’emoglobina libera e riduce l’infiammazione e lo stress ossidativo. I medici testano l’emoglobina per controllare la distruzione anormale dei globuli rossi (anemia emolitica). Le varianti genetiche comuni nel gene dell’aptoglobina sono state associate a malattie cardiache, diabete e altri disturbi infiammatori e immunitari. Continua a leggere per saperne di più su questa proteina e sui modi in cui ti mantiene sano.
- Che cos’è l’aptoglobina?
- Produzione
- Funzione dell’aptoglobina
- 1) Rimuove l’emoglobina libera e protegge i tessuti dallo stress ossidativo
- 2) Può ridurre l’infiammazione
- 3) Può promuovere la crescita di nuovi vasi sanguigni. L’aumento dei livelli di aptoglobina in condizioni infiammatorie o ischemiche (poco ossigeno) può migliorare l’apporto di sangue e promuovere la crescita di vasi collaterali, che svolgono un ruolo importante nella riparazione dei tessuti.
- Esame del sangue dell’aptoglobina
- Intervallo normale
- Livelli bassi
- Anemia emolitica
- Livelli alti
- Genetica dell’aptoglobina
- Limitazioni
- Hp1-1
- Hp1-2
- Hp2-2
- Hp2-2 e malattie cardiache
- Le persone Hp2-2 possono beneficiare della supplementazione di vitamina E
- Hp2, Zonulina e “Leaky Gut”
- Hp0
- Haptoglobina (gene HP) SNPs
- rs5472
Che cos’è l’aptoglobina?
L’aptoglobina (Hp, abbreviazione medica: hpt) è una proteina prodotta principalmente nel fegato, ma anche in altri tessuti tra cui i polmoni, il tessuto grasso, la pelle, la milza, il cervello, l’intestino, i vasi arteriosi e i reni. Viene rilasciata nel flusso sanguigno.
Una delle principali funzioni dell’aptoglobina è quella di legare l’emoglobina libera nel flusso sanguigno.
L’emoglobina si trova normalmente nei globuli rossi, ma viene rilasciata quando si rompono – questo processo è chiamato emolisi. L’emolisi si verifica in alcune malattie, comprese le infezioni, la malaria e alcuni tipi di anemia.
Oltre a trovarsi normalmente nel corpo, l’aptoglobina può anche essere somministrata durante un intervento chirurgico o in alcune malattie in cui l’emolisi è aumentata.
Produzione
L’aptoglobina è prodotta principalmente dalle cellule del fegato (epatociti). La sua produzione è stimolata da citochine infiammatorie come IL-1, IL-6 e TNF.
Pertanto, l’aptoglobina è un reattivo di fase acuta che aumenta con l’infezione, l’infiammazione e la lesione.
Funzione dell’aptoglobina
1) Rimuove l’emoglobina libera e protegge i tessuti dallo stress ossidativo
L’emoglobina libera nel sangue causa danni ossidativi alle cellule e ai tessuti, contribuendo a una serie di problemi di salute, tra cui l’indurimento delle arterie e il malfunzionamento dei reni
L’aptoglobina lega l’emoglobina libera nel sangue. Un complesso stabile di aptoglobina-emoglobina si forma e viene eliminato dai globuli bianchi. Questo previene l’infiammazione indotta dall’emoglobina e i danni ossidativi ai tessuti.
L’aptoglobina previene le lesioni renali riciclando il ferro legato all’emoglobina e impedendo che si accumuli nei reni.
2) Può ridurre l’infiammazione
L’aptoglobina ha un potenziale antinfiammatorio grazie alla sua capacità di sopprimere la produzione di citochine infiammatorie: TNF-alfa, IL-10 e IL-12.
I topi senza aptoglobina hanno sviluppato un’infiammazione più grave in un modello di sclerosi multipla.
Al momento non ci sono studi sugli esseri umani che si concentrano sul ruolo dell’aptoglobina nell’infiammazione.
3) Può promuovere la crescita di nuovi vasi sanguigni. L’aumento dei livelli di aptoglobina in condizioni infiammatorie o ischemiche (poco ossigeno) può migliorare l’apporto di sangue e promuovere la crescita di vasi collaterali, che svolgono un ruolo importante nella riparazione dei tessuti.
La preaptoglobina-2, un precursore dell’aptoglobina, può promuovere la crescita di nuovi vasi sanguigni attraverso la via di segnalazione VEGF. La preaptoglobina-2 può aumentare la produzione di VEGF e dei recettori VEGF (VEGFR2), e aumentare la germinazione e la ramificazione di nuovi vasi sanguigni.
Esame del sangue dell’aptoglobina
È possibile controllare i livelli di aptoglobina con un esame del sangue.
Il medico di solito ordina un test dell’aptoglobina per controllare la distruzione anormale dei globuli rossi (anemia emolitica), e per distinguere questo tipo di anemia dall’anemia dovuta ad altre cause, come la carenza di ferro.
Anche se l’aptoglobina può rilevare l’anemia emolitica, non può dire cosa la causa. Se necessario, il medico eseguirà altri test di follow-up.
Inoltre, questo test è meno affidabile nelle infezioni e nelle condizioni infiammatorie.
Intervallo normale
L’intervallo normale per l’aptoglobina è circa 35-200 mg/dl. Gli intervalli variano tra i laboratori a causa delle differenze nelle attrezzature, nelle tecniche e nelle sostanze chimiche utilizzate.
Un risultato normale non significa che non ci sia una distruzione anormale dei globuli rossi. Il tuo medico interpreterà i tuoi risultati insieme ai tuoi sintomi, alla tua storia medica e ai risultati di altri test.
Livelli bassi
Le cause elencate di seguito sono comunemente associate a bassi livelli di aptoglobina. Collabora con il tuo medico o un altro operatore sanitario per ottenere una diagnosi accurata. Il tuo medico interpreterà i tuoi risultati, prendendo in considerazione i tuoi sintomi, la tua storia medica e i risultati di altri test, come la conta dei globuli rossi (RBC), l’emoglobina, l’ematocrito e la conta dei reticolociti.
Questi possono diminuire l’aptoglobina:
- Anemia emolitica
- Malattia del fegato
- Malnutrizione
- Reazione allergica
- Estrogeni
- Alcuni rari disturbi genetici (anaftoglobinemia)
I livelli di aptoglobina possono diminuire durante la gravidanza con test di laboratorio altrimenti normali. Di solito, i livelli di aptoglobina tornano alla normalità dopo il parto. Questo è probabilmente dovuto alla maggiore ritenzione di liquidi (altrimenti nota come emodiluizione).
La mancanza di aptoglobina nei neonati è comune. Entro i tre mesi di età, l’aptoglobina diventa presente nella maggior parte dei neonati.
Anemia emolitica
Una bassa aptoglobina, insieme a reticolociti alti e bassi RBC, emoglobina ed ematocrito indica un’anemia emolitica.
L’anemia emolitica è una condizione che si verifica quando i globuli rossi vengono prematuramente distrutti.
Durante la distruzione dei globuli rossi, quantità sostanziali di emoglobina vengono rilasciate in circolazione e assorbite dall’aptoglobina. Questa eliminazione dell’emoglobina in eccesso dal sangue impoverisce l’aptoglobina. La ricerca suggerisce che circa l’80% delle persone con anemia emolitica hanno bassi livelli di aptoglobina.
L’anemia emolitica può avere varie cause, tra cui :
- Infezioni, come la malaria
- Disordini autoimmuni, come il lupus
- Disordini genetici, come l’anemia falciforme, la talassemia e il deficit di G6PD
- Milza ingrossata
- Tossine, tra cui avvelenamento da piombo e rame, morsi di serpenti e ragni
- Danni ai vasi sanguigni, visti in disturbi come la porpora trombotica trombocitopenica
- Reazione ai farmaci
- Reazione alle trasfusioni
I sintomi associati all’anemia emolitica includono :
- Affaticamento
- Mancanza di respiro (dispnea)
- Anemia
- Jaundice
- Sangue nelle urine (ematuria)
- Veloce o irregolare (tachicardia)
- Pressione sanguigna bassa (ipotensione)
Livelli alti
L’aptoglobina è un reattivo di fase acuta. Questo significa che è elevata quando c’è un’infiammazione o un’infezione. Una volta che queste condizioni si risolvono, i livelli di solito tornano alla normalità entro diverse settimane.
Le cause elencate di seguito sono comunemente associate a livelli elevati di aptoglobina. Collabora con il tuo medico o un altro operatore sanitario per ottenere una diagnosi accurata.
Queste possono aumentare l’aptoglobina:
- Malattie infettive e infiammatorie
- Obesità (studi hanno scoperto che le cellule di grasso possono produrre aptoglobina)
- Danni ai tessuti dovuti a lesioni, ustioni, o chirurgia
- Milza ingrossata
- Androgeni
- Corticosteroidi
- Fumo
Genetica dell’aptoglobina
Negli umani, ci sono due varianti comuni di aptoglobina, Hp1 e Hp2. La maggior parte delle persone portano due copie di una delle due varianti o una copia di ciascuna :
- Genotipo Hp1-1 = due varianti Hp1
- Genotipo Hp1-2 = una variante Hp1 e una Hp2
- Genotipo Hp2-2 = due varianti Hp2
La variante Hp2 produce una proteina più grande e voluminosa.
Nei bianchi, Hp1-1 si trova nel 15%, Hp2-1 nel 50% e Hp2-2 nel 35% delle persone
La frequenza di Hp1 è bassa nel sud-est asiatico e in India (7%) e alta in parti dell’Africa occidentale e del Sud America (70%). Nel sud-est asiatico, circa il 90% di tutte le persone hanno Hp2-2.
Gli scienziati pensano che Hp1 fosse la variante originale. Si pensa che Hp2 abbia avuto origine in India circa 2 milioni di anni fa e che da allora si sia diffusa in tutto il mondo.
Hp1 è più efficiente nell’inibire i danni causati dall’emoglobina libera rispetto alla variante Hp2. L’attività per genotipi è la seguente:
- Hp1-1 è più efficace nel legare l’emoglobina libera e sopprimere le risposte infiammatorie
- Hp1-2 è moderatamente attiva
- Hp2-2 è meno attiva
Oltre alle varianti Hp1 e Hp2, ci sono altre mutazioni in questo gene che possono causare una mancanza (Hp0) o un eccesso di aptoglobina nell’uomo.
Limitazioni
Prima di immergerci nella ricerca associata a questo gene, tenete presente che gli studi che seguono sono in gran parte basati sull’associazione, suggerendo che alcune varianti genetiche, come Hp1-1 o Hp2-2, sono più o meno comuni nelle persone con queste condizioni. Sono necessarie ulteriori ricerche per sapere quale ruolo, se c’è, le varianti Hp1 e Hp2 giocano nel contribuire effettivamente a queste condizioni.
Inoltre, tutte queste condizioni dipendono da una moltitudine di fattori, e le varianti di aptoglobina possono avere solo un effetto minore. Pertanto, solo perché si può avere il genotipo Hp1-1, Hp1-2, o Hp2-2, questo non significa necessariamente che si è ad un rischio maggiore o minore di sviluppare una di queste condizioni!
Hp1-1
Gli studi suggeriscono che le persone con Hp1-1 possono avere una risposta Th1 più forte.
La ricerca suggerisce che Hp1-1 può essere utile contro:
- Malattie cardiache
- Colesterolo alto (totale e LDL)
- Infezioni
- Malattie infiammatorie e immunitarie (sclerosi sistemica, malattie infiammatorie intestinali o IBD)
Hp1-1 è stato associato ad un aumentato rischio di:
- Tropo nel diabete
- Peggiore funzione cognitiva nel diabete e dopo lesioni cerebrali
- Vermi parassiti
Hp1-2
Il genotipo Hp1-2 è stato associato a un aumentato rischio di:
- Resistenza all’insulina
- Malattia celiaca
- Parkinson
- Fertilità compromessa
Hp2-2
La ricerca suggerisce che H2-2 può essere utile contro:
- Malaria
Tuttavia, gli studi hanno trovato un legame tra Hp2-2 e un aumento del rischio di:
- Infezioni virali
- Indurimento delle arterie
- Malattie cardiache
- Pressione sanguigna elevata
- Colesterolo HDL basso
- Diabete e complicazioni legate al diabete (malattie cardiache e renali)
- Malattie immunitarie/infiammatorie (lupus, artrite reumatoide, diabete di tipo 1, IBD)
- “Leaky gut”
- Carenza di vitamina C
Hp2-2 e malattie cardiache
Uno studio su 400 persone ha scoperto che gli individui diabetici che erano Hp2-2 avevano 5 volte più probabilità di avere malattie cardiache rispetto agli individui diabetici Hp1-1 .
Gli scienziati sospettano che un tasso più lento di clearance dell’emoglobina libera in quelli con la variante Hp2 può aumentare l’indurimento delle arterie e quindi pone un rischio maggiore per le malattie cardiache.
Gli studi hanno trovato un’associazione tra Hp2-2 e un rischio maggiore di infarto, ictus e insufficienza cardiaca. Il genotipo Hp2-2 è stato anche associato ad altre complicazioni come aneurismi, rotture della placca carotidea e una minore sopravvivenza dopo il bypass coronarico.
Inoltre, gli studi suggeriscono che le persone con le varianti Hp 2-2 hanno livelli di aptoglobina nel sangue più bassi, che possono contribuire ulteriormente allo sviluppo delle malattie cardiache.
Le persone Hp2-2 possono beneficiare della supplementazione di vitamina E
Le persone Hp2-2 che hanno il diabete possono beneficiare di un’integrazione antiossidante come la vitamina E, chelanti del ferro, o una combinazione di entrambi per ridurre la gravità della malattia cardiaca.
Una meta-analisi di 8 studi con 3.939 pazienti ha mostrato che i portatori di Hp2-2 con il diabete hanno beneficiato della supplementazione di vitamina E.
Secondo revisioni scientifiche, l’integrazione di vitamina E negli individui Hp2-2 ha il potenziale di ridurre gli eventi cardiovascolari fino al 35 – 50% .
In uno studio su 20 diabetici, la vitamina E ha migliorato la funzione dei vasi sanguigni individui con Hp2-2 dopo otto settimane di trattamento .
L’integrazione di vitamina E ha rallentato la progressione della malattia renale nei topi Hp2-2 ma non ha influenzato la progressione nei topi Hp1-1 .
Ricorda, consulta sempre un medico o un altro operatore sanitario prima di utilizzare gli integratori in quanto possono interagire con le tue condizioni di salute o con i tuoi farmaci!
Hp2, Zonulina e “Leaky Gut”
Prehaptoglobin-2, un precursore di Hp2 (la proteina di cui è fatta la Hp2), è anche chiamato zonulina. La zonulina provoca l’apertura delle giunzioni strette nell’intestino, aumentando così la permeabilità intestinale.
La zonulina è aumentata nelle malattie immunitarie e infiammatorie legate all’aumento della permeabilità intestinale, come la malattia celiaca e il diabete di tipo 1 e 2.
Alcuni scienziati pensano che le persone con Hp2-2 (2 varianti di Hp2) possono avere un aumentato rischio di disturbi immunitari e infiammatori a causa di una maggiore permeabilità intestinale.
Hp0
Questa variante risulta in un gene non funzionale (nessun prodotto proteico). Le persone con due copie di questa variante non hanno livelli di aptoglobina rilevabili nel sangue. Hp0 si trova principalmente in Asia orientale (1-4%) .
Hp0 aumenta il rischio di reazione anafilattica dopo la trasfusione di sangue (a causa di anticorpi anti-aptoglobina) .
Haptoglobina (gene HP) SNPs
rs5472
La variante A di rs5472 è stata associata a livelli più alti di Hp .