- trans-Cinnamaldehida Proprietăți chimice, utilizări, producție
- Overview
- Farmacocinetică
- Aplicații
- Toxicitate
- Proprietăți chimice
- Proprietăți chimice
- Proprietăți chimice
- Definiție
- Referință(e) de sinteză
- Descriere generală
- Aer & Apă Reacții
- Profil de reactivitate
- Pericol de incendiu
- Expunere potențială
- Expediție
- Incompatibilități
- Eliminarea deșeurilor
trans-Cinnamaldehida Proprietăți chimice, utilizări, producție
Overview
Cinnamaldehida, un vechi aromatizant derivat din arborele de scorțișoară și din alte specii din genul Cinnamomum, a atras în prezent un interes crescând pentru capacitatea sa de a preveni apariția diabetului și a complicațiilor acestuia. Sub forma unui lichid galben și vâscos, cinamaldehida constituie 98% din uleiul esențial din scoarța de scorțișoară și a fost izolată pentru prima dată de Dumas și Péligot și apoi sintetizată în laborator de chimistul italian Luigi Chiozza (1828-1889) în 1854. În 2007, Subash et al. au raportat pentru prima dată un efect hipoglicemiant și hipolipemiant al cinamaldehidei asupra șobolanilor Wistar masculi diabetici indus de streptozotocină (STZ). De atunci, cinamaldehida a fost studiată pe scară largă în modele animale de diabet și obezitate.
Cassia sau scorțișoara chinezească este un condiment utilizat pe scară largă, extras din scoarța interioară a arborelui de scorțișoară. Cassia a fost folosită de mii de ani în scopuri medicinale și este considerată una dintre cele 50 de plante fundamentale în medicina tradițională chineză. Mai multe părți ale plantei Cassia sunt folosite în scopuri medicinale, inclusiv rădăcina, scoarța, frunzele și florile. S-a raportat că extractele de scorțișoară au diverse efecte benefice, inclusiv efecte antialergenice, antimicrobiene, antivirale, antioxidative, gastroprotectoare, antiangiogenice și anti-Alzheimer, precum și activități biologice asemănătoare insulinei . Extractele de scorțișoară conțin mai mulți compuși activi, inclusiv uleiuri esențiale (cinamaldehida și cinamil aldehida), taninuri, mucus și carbohidrați. În mod interesant, cinamaldehida, cunoscută și sub denumirea de aldehidă cinamică, prezintă efecte anti-obezitate prin reducerea acumulării de lipide și prin reglarea în jos a receptorului activat de proliferator de peroxisom-γ, a proteinei de legare a CCAAT/enhancerului α și a proteinei de legare a elementului de reglementare a sterolului 1. Mai mult, cinamaldehida inhibă activarea microglială indusă de lipopolizaharide prin direcționarea proteinei-1 legată de receptorul lipoproteinei cu densitate scăzută. De asemenea, s-a raportat că cinamaldehida are efecte antimutagenice în celulele canceroase.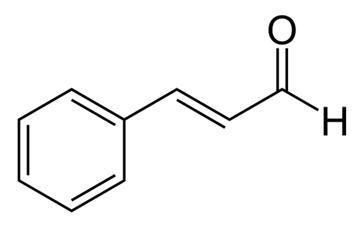
Figura 1 structura chimică a cinamaldehidei;
Farmacocinetică
Cinamaldehida există în mod natural sub formă de trans-cinamaldehidă. Într-un experiment realizat de Zhao et al. evaluează farmacocinetica cinamaldehidei la șobolani folosind o abordare relativ sensibilă a cromatografiei în fază gazoasă-spectrometrie de masă (GC-MS) prin administrare orală (500 mg/kg) și injecție intravenoasă (i.v.,20 mg/kg). Rezultatele arată că AUC0-t a cinamaldehidei prin administrare orală și prin administrare i.v. sunt 1984 ± 531 și, respectiv, 355 ± 53 ng h/ml. T1/2 și Tmax ale cinamaldehidei sunt mai lungi pentru administrarea orală (6,7 ± 1,5 h și 1,6 ± 0,5 h) decât pentru administrarea i.v. (1,7 ± 0,3 h și 0,033 h). Cmax este de 249±36 ng/ml pentru administrarea orală și, respectiv, 547±142 ng/ml pentru administrarea i.v.. Rezultatele indică faptul că biodisponibilitatea cinamaldehidei este mai bine îmbunătățită prin administrare i.v. decât prin administrare orală.
În plus, autorii demonstrează că Cmax și AUC0-t sunt proporționale cu doza (de la 125 la 500 mg), în timp ce Tmax și timpul mediu de rezidență nu se modifică ca răspuns la creșterea dozei. Având în vedere că cinamaldehida și alcoolul cinamilic s-ar putea transforma unul în celălalt la șobolani, autorii analizează, de asemenea, proprietatea farmacocinetică a alcoolului cinamilic în plasma șobolanilor. Datele farmacocinetice ale alcoolului cinamilic sunt de 1105±337 ng-h/ml pentru AUC0-t, 6,7±2,8 h pentru T1/2, 1,5±0,7 h pentru Tmax și 221±66 ng/ml pentru Cmax, la doza orală de 500 mg/kg. Interesant este faptul că în metaboliți a fost descoperit și cinamatul de metil. Pentru proprietatea farmacocinetică a cinamatului de metil, cititorii interesați sunt încurajați să consulte articolul lui Zhao et al. Pe scurt, cinamaldehida este bine distribuită în organism după absorbție. Cinnamaldehida are opțiunea de a se transforma în alcool cinamilic și, de asemenea, poate fi oxidată în acid cinamic după ce intră în organism. Pentru a înțelege pe deplin proprietățile farmacocinetice ale cinamaldehidei, ar trebui să se determine, de asemenea, cinnamatul de metil și alcoolul cinamilic în plasmă. Cu toate acestea, instabilitatea cinamaldehidei pune sub semnul întrebării faptul că bioactivitatea cinamaldehidei se datorează probabil sumei metaboliților săi. Prin urmare, se așteaptă încercări suplimentare pentru a aborda potențialele preocupări. În plus, noua SME-cinnamaldehidă dezvoltată, cu o biodisponibilitate îmbunătățită, necesită, de asemenea, investigații suplimentare privind efectul antidiabetic.
Aplicații
Extractele de scorțișoară au diverse efecte benefice, inclusiv efecte antialergenice, antimicrobiene, antivirale, antioxidative, gastroprotectoare, antiangiogenice și anti-Alzheimer, precum și activități biologice asemănătoare insulinei. Cinnamaldehida prezintă efecte anti-obezitate prin reducerea acumulării de lipide și prin reglarea în jos a receptorului activat de proliferator al peroxisomului-γ, a proteinei de legare a CCAAT/enhancerului α și a proteinei de legare a elementului de reglare a sterolului 1. Mai mult, cinnamaldehida inhibă activarea microglială indusă de lipopolizaharidă prin direcționarea către proteina-1 legată de receptorul lipoproteinei cu densitate scăzută. S-a raportat, de asemenea, că cinamaldehida are efecte antimutagenice în celulele canceroase. Efectul cinamaldehidei în tratamentul cancerului și al diabetului este evidențiat mai jos:
Anticancer
Kwon et al. au raportat pentru prima dată că extractele de scorțișoară induc moartea celulelor de melanom in vitro și in vivo prin inhibarea NF-κB și AP-1. Un studiu ulterior a arătat că HCA este principalul compus antitumorigen găsit în extractele de scorțișoară, exercitându-și efectele de inhibare a creșterii în 29 de tipuri de celule canceroase umane in vitro și în xenogrefele tumorale umane SW620 in vivo.
Alte echipe de cercetare au raportat, de asemenea, efecte antitumorigene ale extractelor de scorțișoară. Acestea inhibă celulele canceroase de melanom prin inducerea expresiei factorilor pro-angiogenici; de asemenea, au îmbunătățit activitățile antitumorigene ale celulelor T CD8 prin creșterea activității lor citolitice. Extractele de scorțișoară inhibă, de asemenea, factorul de creștere endotelială vasculară, care a fost descoperit prin depistarea compușilor pentru activitatea lor inhibitoare față de VEGFR2. Cea mai mare parte a efectelor antitumorigene ale extractelor de scorțișoară poate fi atribuită cinnamaldehidelor, principala componentă a uleiului esențial, responsabilă de gustul și aroma scorțișoarei întregi. S-a raportat că cinamaldehidele au inhibat proliferarea celulelor canceroase prin inhibarea ciclinei D1 în mai multe tipuri de tumori. Cinnamaldehidele induc, de asemenea, apoptoza prin generarea de specii reactive de oxigen în celulele leucemice HL-60 și prin activarea proteinelor pro-apoptotice din familia Bcl-2 și a căii de semnalizare MAPK în celulele de hepatom uman. Mai mult, cinamaldehidele dimerice derivate din HCA au prezentat efecte antitumorigene mai mari decât cinamaldehidele monomerice prin inducerea apoptozei și oprirea ciclului celular. În plus, o serie de studii au arătat că efectele antitumorigene ale HCA și ale derivaților săi sunt mediate prin mai multe mecanisme moleculare. Un studiu recent a arătat că polifenolii care poartă o schemă de cinnamaldehidă au declanșat oprirea ciclului celular în faza G2/M și moartea celulară apoptotică în celulele umane de cancer ovarian rezistente la cisplatin, sugerând că compușii cinnamaldehidei ar putea fi eficienți în chimioterapiile combinate pentru pacienții cu cancer. În general, mecanismele moleculare care stau la baza efectelor anticancerigene și antimetastatice ale cinamaldehidelor sunt diverse, sugerând că cinamaldehida este un compus cu ținte multiple. Receptivitatea diferențiată a diferitelor tipuri de cancer la diferiți derivați de cinamaldehidă trebuie evaluată pentru a permite selectarea celui mai eficient compus pentru fiecare tip de cancer.
Antidiabet
În ultimele decenii au fost efectuate studii emergente pentru a evalua rolul benefic al acesteia în gestionarea diabetului și a complicațiilor sale. S-a demonstrat că administrarea orală de cinamaldehidă pe cale orală de la 20 mg/kg-greutate corporală până la 40 mg/kg-greutate corporală pe zi, pe o durată cuprinsă între 21 și 60 de zile, a dus la o îmbunătățire semnificativă a nivelurilor de glucoză din sânge și de hemoglobină glicozilată, precum și a sensibilității la insulină la șobolanii diabetici induși de STZ. Și se presupune că 20 mg/kg-PC este doza eficientă pentru prevenirea apariției diabetului la animale. Mai mult, tratamentul cu cinamaldehidă timp de 4 săptămâni crește nivelul insulinei plasmatice și conținutul de glicogen din ficat, precum și scade nivelul trigliceridelor și al lipoproteinei colesterolului cu densitate scăzută la șobolanii Wistar masculi insultați cu STZ și/sau HFD. Mai mult, Camacho et al. au constatat că administrarea de cinamaldehidă timp de 5 săptămâni la șoarecii C57BL/6J hrăniți cu HFD a condus în mod semnificativ la o reducere a creșterii masei de grăsime corporală. Cu toate acestea, ei au susținut că tratamentul cu cinamaldehidă nu a modificat nivelurile plasmatice de insulină la post și consumul de hrană. Motivul neconcordanței în ceea ce privește reglarea insulinei ar putea fi atribuit faptului că fondul genetic al șoarecilor C57BL/6J este modificat în unele unități de producție. Diferitele rase de șoareci pot prezenta diferențe semnificative în ceea ce privește fenotipurile. În plus, cinamaldehida poate prezenta un efect de scădere a glucozei prin îmbunătățirea sensibilității la insulină la periferie în studiul lui Camacho.
Cinnamaldehida are capacitatea de a îmbunătăți țesuturile adipoase diabetice prin reducerea depunerii de grăsime viscerală și promovarea lipolizei și a oxidării acizilor grași și a termogenezei, care este asociată cu o creștere a genelor de cheltuieli energetice, o inhibiție a PPARγ/CEBP-α și SREBP1, o creștere a HSL și PNPLA2 și MGL, o inducție a fosforilării AMPK și o creștere a Cpt1a în WAT și a Acsl4 în BAT, precum și o stimulare a sistemului nervos simpatic. În plus, cinamaldehida previne expresia genelor inflamatorii și îmbunătățește expresia GLUT-urilor la animalele diabetice. Cinnamaldehida poate proteja împotriva diabetului prin îmbunătățirea sensibilității la insulină și a absorbției de glucoză prin reglarea căii PI3K/IRS-1 și RBP4-GLUT4 în țesutul muscular scheletic, precum și prin reglarea metabolismului mitocondriilor prin intermediul căii PGC-1α/MEF2/GLUT4 în celulele C2C12. Cinnamaldehida are, de asemenea, efecte pozitive asupra ficatului diabetic prin îmbunătățirea sintezei de glicogen prin reglarea activităților PK și PEPCK și prin scăderea nivelului RBP4, precum și prin normalizarea enzimelor hepatice aberante, sugerând un rol benefic al acestui compus în metabolismul glucozei și în sensibilitatea la insulină în ficatul diabetic.
Efecte antimicrobiene
Studiul a confirmat activitatea antimicrobiană a cinamaldehidei, cuișoarei, cimbrului și rozmarinului împotriva E. coli O157:H7 și Salmonella. Wendakoon și Sakaguchi au raportat că grupul carbonil al cinamaldehidei se leagă de proteine, împiedicând activitatea decarboxilazei aminoacizilor la Enterobacter aerogenes. Smid et al. au observat deteriorarea membranei citoplasmatice a Saccharomyces cerevisiae atunci când este tratată cu cinamaldehidă, ceea ce duce la o scurgere excesivă de metaboliți și enzime din celulă și, în final, la pierderea viabilității. Majoritatea studiilor au sugerat că modurile de acțiune ale uleiurilor esențiale depind de tipul de microorganisme, în principal de structura peretelui celular și de dispunerea membranei externe a acestora. Aceștia au observat daune datorate diferențelor semnificative dintre membranele exterioare ale bacteriilor gram-negative și gram-pozitive.
Toxicitate
Chiar și acum, cinamaldehida este încă presupusă a fi un agent ingredient natural sigur și bine tolerat la om și la animale. Conceptul este, de asemenea, bine acceptat de FDA și de consiliul Europei, cu sugestia de doză zilnică acceptabilă de 1,25 mg/kg.
Toxicitate acută
Cinnamaldehida este raportată ca având marja mare de siguranță, iar administrată de 20 de ori doza efectivă(20 mg/kg) a acestui compus nu a provocat semne comportamentale anormale și nu a deranjat valorile serico-chimice pe tot parcursul studiului. Toxicitatea acută a cinamaldehidei este scăzută, cu valori ale dozei letale mediane orale(LD50) care variază de la un nivel scăzut de 0,6 g/kg BW la un nivel ridicat de 3,4 g/kg BW la diferite specii.
Toxicitate pe termen lung
Rezultatele unui studiu de trei luni arată că greutatea corporală este redusă la șobolanii femele expuși la 16.500 sau 33.000 ppm și la șoarecii femele expuși la 8200 ppm sau mai mult. În plus, consumul de hrană este redus la toate grupurile de șobolani expuși și la grupul de șoareci cu cea mai mare doză. Mai mult decât atât, expunerea la cinamaldehidă crește incidența hiperplaziei epiteliale scuamoase a silvicomacului. În plus, șoarecii expuși la cinamaldehidă prezintă, de asemenea, o incidență crescută a degenerării epiteliale olfactive a cavității nazale. Toți șobolanii au supraviețuit pe toată durata studiului de trei luni.
Alte
Cinnamaldehida poate prezenta, de asemenea, efecte citotoxice în hepatocitele de șobolan F344, evidențiate prin epuizarea nivelurilor de glutation, și în celulele HepG2, evidențiate prin creșterea numărului de micronuclee. Behar et al. au studiat potențiala toxicitate a acestui produs în celulele embrionare și pulmonare umane. Rezultatele demonstrează că tratamentul cu cinamaldehidă depolimerizează microtubulii în fibroblastele pulmonare umane. De asemenea, cinamaldehida diminuează proliferarea și diferențierea celulară prin inhibarea creșterii și diferențierii celulare și prin alterarea morfologiei și motilității celulare, precum și prin creșterea rupturilor de șiruri de ADN și a morții celulare. Un studiu realizat de Olsen et al. arată că cinamaldehida provoacă iritații cutanate prin creșterea pragului durerii la rece și scăderea pragului durerii mecanice, precum și prin creșterea temperaturii pielii și a perfuziei la om.
- Zhou M, Chen Z, Shen S. Recent advanceson cinnamaldehyde. Journal of Economic Animal 2015;19:1-5.
- Khare P, Jagtap S, Jain Y, Baboota RK, Mangal P, Boparai RK, Bhutani KK, Sharma SS, Premkumar LS, Kondepudi KK, Chopra K, Bishnoi M. Suplimentarea cu cinamaldehidă previne hiperfagia indusă de post, acumularea de lipide și inflamația la șoarecii hrăniți cu o dietă bogată în grăsimi. BioFactors 2016;42:201-211.
- Ma R, Zhu R, Wang L, Guo Y, Liu C, Liu H, Liu F, Li H, Li Y, Fu M, Zhang D. Diabetic osteoporosis: O trecere în revistă a utilizării sale în medicina tradițională chineză și a cercetării clinice și preclinice. Evidence-based complementary and alternative medicine : eCAM 2016;2016:3218313.
- Dumas JP, E. Organic chemistry research – on cinnamon oil, the hippuric acid and sebacic acid. Annales de chimie et de physique 1834;57:305-334.
- Chiozza L. Sur la production artificielle de l´essence de cannelle”. Comptes rendus 1856;42:222-227.
- Subash Babu P, Prabuseenivasan S, Ignacimuthu S. Cinnamaldehyde–a potential antidiabetic agent. Phytomedicine : international journal of phytotherapy and phytopharmacology 2007;14:15-22.
- Hagenlocher Y, Bergheim I, Zacheja S, Schaffer M, Bischoff SC, Lorentz A. 2013. Extractul de scorțișoară inhibă degranularea și sinteza de novo a mediatorilor inflamatori în mastocite. Allergy 68: 490-497.
- Matan N, Rimkeeree H, Mawson AJ, Chompreeda P, Haruthaithanasan V, Parker M. 2006. Activitatea antimicrobiană a uleiurilor de scorțișoară și de cuișoare în condiții de atmosferă modificată. Int J Food Microbiol 107: 180-185.
- Fink RC, Roschek B Jr, Alberte RS. 2009. Inhibitori de intrare a HIV de tip 1 cu un nou mod de acțiune. Antivir Chem Chemother 19: 243-255.
- Yang CH, Li RX, Chuang LY. 2012. Activitatea antioxidantă a diferitelor părți de Cinnamomum cassia extrase cu diferite metode de extracție. Molecules 17: 7294-7304.
- Peterson DW et al. 2009. Extractul de scorțișoară inhibă agregarea tau asociată cu boala Alzheimer in vitro. J Alzheimers Dis 17: 585-597.
- Cheng DM, Kuhn P, Poulev A, Rojo LE, Lila MA, Raskin I. 2012. Efectele antidiabetice in vivo și in vitro ale extractului apos de scorțișoară și ale matricei alimentare îmbunătățite cu polifenoli de scorțișoară. Food Chem 135: 2994-3002.
- Kim JE et al. 2015a. Un nou produs natural legat de scorțișoară cu activitate inhibitoare Pim-1 inhibă leucemia și cancerul de piele. Cancer Res 75: 2716-2728.
- Hwang H et al. 2011. 2′-Hydroxycinnamaldehida țintește proteina-1 legată de receptorul de lipoproteine cu densitate scăzută pentru a inhiba activarea microglială indusă de lipopolizaharide. J Neuroimmunol2011 230: 52-56.
- Shaughnessy DT, Setzer RW, DeMarini DM. 2001. Efectul antimutagenic al vanilinei și al cinamaldehidei asupra mutației spontane în Salmonella TA104 se datorează unei reduceri a mutațiilor la situsurile GC, dar nu AT. Mutat Res 480: 55-69.
- Zhang LQ, Zhang ZG, Fu Y, Xu Y. Progresul cercetării efectelor farmacologice ale trans-cinnamaldehidei. Zhongguo Zhong yao za zhi = Zhongguo zhongyao zazhi = China journal of Chinese materia medica 2015;40:4568-4572.
- Zhao H, Xie Y, Yang Q, Cao Y, Tu H, Cao W, Wang S. Studiu farmacocinetic al cinnamaldehidei la șobolani prin gc-ms după administrare orală și intravenoasă. Journal of pharmaceutical and biomedical analysis 2014;89:150-157.
- Kwon BM et al. 1998. Sinteza și citotoxicitatea in vitro a cinamaldehidelor pentru celulele tumorale solide umane. Arch Pharm Res 21: 147-152.
- Lee CW și colab. 1999. Inhibarea creșterii tumorilor umane de către 2′-hidroxiși 2′-benzoyloxycinnamaldehide. Planta Med 65: 263-266
- Kwon HK și colab. 2009. Extractul de scorțișoară suprimă progresia tumorală prin modularea angiogenezei și a funcției efectoare a celulelor T CD8 +. Cancer Lett 278: 174-182.
- Lu J, Zhang K, Nam S, Anderson RA, Jove R,WenW. 2010. Noua activitate inhibitoare a angiogenezei în extractul de scorțișoară blochează kinaza VEGFR2 și semnalizarea în aval. Carcinogenesis 31: 481-488.
- Jeong HW și colab. 2000. Cinnamaldehidele inhibă kinaza dependentă de ciclină 4 / ciclină D1. Bioorg Med Chem Lett 10: 1819-1822.
- Ka H et al. 2003. Cinnamaldehida induce apoptoza prin tranziția permeabilității mitocondriale mediată de ROS în celulele de leucemie promielocitară umană HL-60. Cancer Lett 196: 143-152.
- Wu SJ, Ng LT, Lin CC. 2005. Apoptoza indusă de cinamaldehidă în celulele umane PLC / PRF / 5 prin activarea proteinelor proapoptotice din familia Bcl-2 și a căii MAPK. Life Sci 77: 938-951.
- Shin DS et al. 2006. Sinteza și evaluarea biologică a cinamaldehidelor dimerice ca agenți antitumorali puternici. Bioorg Med Chem 14: 2498-2506.
- Shin SY et al. 2014. Polifenoli purtând scheletul cinnamaldehidei care prezintă efecte inhibitoare de creștere celulară asupra celulelor de cancer ovarian A2780/Cis rezistente la cisplatin. Bioorg Med Chem 22: 1809-1820.
- Lee SC, Xu WX, Lin LY, Yang JJ, Liu CT. Compoziția chimică și efectul hipoglicemiant și pancreas-protector al uleiului esențial de frunze din scorțișoara indigenă. Journal of agricultural and food chemistry 2013;61:4905-4913.
- El-Bassossy HM, Fahmy A, Badawy D. Cinnamaldehyde protejează de hipertensiunea asociată cu diabetul. Food and chemical toxicology : an international journal published for the British Industrial Biological Research Association 2011;49:3007-3012.
- Li M, Xu Y, Zhang W. Efectele cinamaldehidei asupra nivelurilor de expresie ale irs-1 și p85 alfa în gastrocnemius de șobolani diabetici de tip 2. Medical Journal of Wuhan University 2009;30:723-726=731.
- Kumar S, Vasudeva N, Sharma S. Gc-ms analysis and screening of antidiabetic, antioxidant and hypolipidemic potential of cinnamomum tamala oil in streptozotocin induced diabetes mellitus in rats. Cardiovascular diabetology 2012;11:11:95.
- Camacho S, Michlig S, de Senarclens-Bezencon C, Meylan J, Meystre J, Pezzoli M, Markram H, le Coutre J. Efectele anti-obezitate și antihiperglicemice ale cinnamaldehidei prin intermediul secreției modificate de ghrelin și impactul funcțional asupra aportului alimentar și a golirii gastrice. Rapoarte științifice 2015;5:7919.
- Navarro SJ, Trinh T, Lucas CA, Ross AJ, Waymire KG, Macgregor GR. Fundalul tulpinii de șoareci c57bl/6j modifică efectul unei mutații în bcl2l2. G3 2012;2:99-102.
- Mekada K, Abe K, Murakami A, Nakamura S, Nakata H, Moriwaki K, Obata Y, Yoshiki A. Genetic differences among c57bl/6 substrains. Experimental animals 2009;58:141-149.
- Kiselycznyk C, Holmes A. All mice are not created equal. Frontiers in neuroscience 2011;5:10.
- Attane C, Peyot ML, Lussier R, Zhang D, Joly E, Madiraju SR, Prentki M. Secreția diferențială de insulină a șoarecilor c57bl/6nn și c57bl/6njj hrăniți cu o dietă bogată în grăsimi: Implicații ale fondului genetic mixt în studiile metabolice. PloS one 2016;11:e0159165.
- Nicholas P G, Schnuckc. JK, Mermierd. CM, Conne. CA, Vaughanc. RA. Trans-cinnamaldehida stimulează biogeneza mitocondrială prin pgc-1α și pparβ /δ, ceea ce duce la o expresie sporită a glut4. Biochimie 2015;119:45-51.
- Zhang W, Xu YC, Guo FJ, Meng Y, Li ML. Efectele antidiabetice ale cinnamaldehidei și berberinei și impactul lor asupra expresiei proteinei de legare a retinolului 4 la șobolani cu diabet zaharat de tip 2. Chin Med J 2008;121:2124-2128.
- Bandyopadhyay GK, Yu JG, Ofrecio J, Olefsky JM. Creșterea expresiei p85/55/50 și scăderea activității fosfotidilinositol 3-kinază în mușchiul scheletic uman rezistent la insulină. Diabetes 2005;54:2351-2359.
- Saraswathi V, Ramnanan CJ, Wilks AW, Desouza CV, Eller AA, Murali G, Ramalingam R, Milne GL, Coate KC, Edgerton DS. Impactul deficitului de ciclooxigenază-1 hematopoietică asupra inflamației țesutului adipos legat de obezitate și a tulburărilor metabolice la șoareci. Metabolism: clinic și experimental 2013;62:1673-1685.
- Ohaeri OC. Efectul uleiului de usturoi asupra nivelurilor diferitelor enzime în serul și țesutul șobolanilor diabetici streptozotocinici. Bioscience reports 2001;21:19-24.
- Mahfouz MH, Assiri AM, Mukhtar MH. Evaluarea lipocalinei asociate cu gelatinaza neutrofilă (ngal] și a proteinei 4 de legare a retinolului la pacienții diabetici de tip 2 cu nefropatie. Biomarker insights 2016;11:31-40.
- SHAN, B., CAY, Y.-Z., BROOKS, J.D. și CORKE, H. 2007. Proprietăți antibacteriene și componente bioactive majore ale batonului de scorțișoară: Activitate împotriva bacteriilor patogene de origine alimentară. J. Agric. Food Chem. 55, 5484-5490
- RHAYOUR, K., BOUCHIKHI, T., TANTAOUI-ELARAKI, A., SENDIDE, K. și REMMAL, A. 2003. Mecanismul de acțiune bactericidă a uleiurilor esențiale de oregano și de cuișoare a componentelor lor fenolice majore asupra Escherichia coli și Bacillus subtilis. J. Essent. Oil Res. 15, 356-362.
- KIM, H.-O., PARK, S.-W. și PARK, H.-D. 2004. Inactivarea Escherichia coli O157:H7 de către aldehida cinamică purificată din mugurii de Cinnamomum cassia. Food Microbiol. 21, 105-110
- WENDAKOON, C. și SAKAGUCHI, M. 1995. Inhibarea activității decarboxilazei de aminoacizi a Enterobacter aerogenes de către componentele active din condimente. J. Food Prot. 58, 280-283.
- SMID, E.J., KOEKEN, J.P.G. și GORRIS, L.G.M. 1996. Acțiunea fungicidă și fungistatică a metaboliților vegetali secundari cinnamaldehidă și carvonă. În Modern Fungicides and Antimicrobial Compounds pp. 173-180, Intercept, Andover, U.K.
- Dugoua JJ, Seely D, Perri D, Cooley K, Forelli T, Mills E, Koren G. From type 2 diabetes to antioxidant activity: O analiză sistematică a siguranței și eficacității scoarței de scorțișoară comună și de scorțișoară cassia. Jurnalul canadian de fiziologie și farmacologie 2007;85:837-847.
- Anand P, Murali KY, Tandon V, Murthy PS, Chandra R. Efectul insulinotropic al cinamaldehidei asupra reglării transcripționale a piruvat kinazei, fosfoenolpiruvat carboxikinazei și a translocației glut4 la șobolanii diabetici experimentali. Interacțiuni chimico-biologice 2010;186:72-81.
- Gowder SJT. Evaluarea siguranței a aromei alimentare -cinnamaldehidă. Biosafety 2014;3
- Hooth MJ, Sills RC, Burka LT, Haseman JK, Witt KL, Orzech DP, Fuciarelli AF, Graves SW, Johnson JD, Bucher JR. Studii de toxicologie și carcinogeneză a trans-cinnamaldehidei microîncapsulate la șobolani și șoareci. Food and chemical toxicology : an international journal published for the British Industrial Biological Research Association 2004;42:1757-1768.
- Swales NJ, Caldwell J. Studies on trans-cinnamaldehyde ii: Mechanisms of cytotoxicity in rat isolated hepatocytes. Toxicologie in vitro : o revistă internațională publicată în asociere cu BIBRA 1996;10:37-42.
- Sanyal R, Darroudi F, Parzefall W, Nagao M, Knasmuller S. Inhibarea efectelor genotoxice ale aminelor heterociclice în celulele hepatomului derivat uman prin bioantimutageni dietetici. Mutagenesis 1997;12:297-303.
- Behar RZ, Luo W, Lin SC, Wang Y, Valle J, Pankow JF, Talbot P. Distribution, quantification and toxicity of cinnamaldehyde in electronic cigarette refill fluids and aerosols. Tobacco control 2016
- Olsen RV, Andersen HH, Moller HG, Eskelund PW, Arendt-Nielsen L. Manifestări somatosenzoriale și vasomotorii ale stimulării individuale și combinate a trpm8 și trpa1 folosind l-mentol topic și trans-cinnamaldehidă la voluntari sănătoși. European journal of pain 2014;18:1333-1342.
Proprietăți chimice
trans-Cinnamaldehida este componenta principală a uleiului de cassia (aproximativ 90%) și a uleiului din scoarță de scorțișoară din Sri Lanka (aproximativ 75%). Cantități mai mici se găsesc în multe alte uleiuri esențiale. În natură, izomerul trans este predominant.
trans-Cinnamaldehida este un lichid gălbui cu un miros picant caracteristic,care amintește puternic de scorțișoară. Fiind o aldehidă ??,??-nesaturată, suferă numeroase reacții, dintre care este importantă hidrogenarea la alcool cinamic, dihidrocinamaldehidă și alcool dihidrocinamic. Acidul cinamic se formează prin autooxidare.
La scară industrială, cinamaldehida se prepară aproape exclusiv prin condensarea alcalină a benzaldehidei și acetaldehidei. Autocondensareaacetaldehidei poate fi evitată prin utilizarea unui exces de benzaldehidă și prin adăugarea lentă de acetaldehidă.
Cinnamaldehida este utilizată în multe compoziții pentru crearea de note picante și orientale (de exemplu, parfumuri de săpun). Este principalul component al uleiului artificial de scorțișoară. În plus, este un intermediar important în sinteza alcoolului cinamic și a alcoolului dihidrocinamic.
Proprietăți chimice
LICHID GALBEN CLAR
Proprietăți chimice
Lichid inflamabil, gălbui, uleios (se îngroașă la expunerea la aer). Miros puternic înțepător, picant, de scorțișoară.
Definiție
ChEBI: Stereoizomerul E (trans) al cinamaldehidei, părintele clasei de cinamaldehide.
Referință(e) de sinteză
Chemistry Letters, 12, p. 1207, 1983
Journal of the American Chemical Society, 93, p. 2080, 1971 DOI: 10.1021/ja00737a057
Tetrahedron Letters, 18, p. 1215, 1977
Descriere generală
Lichid galben deschis cu miros de scorțișoară și gust dulce.
Aer & Apă Reacții
Poate fi sensibil la expunerea prelungită la aer și la lumină. Insolubil în apă.
Profil de reactivitate
trans-Cinnamaldehida este incompatibilă cu agenții oxidanți puternici și cu bazele puternice. trans-Cinnamaldehida poate reacționa, de asemenea, cu hidroxidul de sodiu.
Pericol de incendiu
trans-Cinnamaldehida este combustibil.
Expunere potențială
Fungicid și insecticid botanic. Folosit ca agent antifungic, ca agent de atragere a viermelui rădăcinilor de porumb și ca repelent pentru câini și pisici. Poate fi utilizat pe învelișul solului pentru ciuperci, culturi în rânduri, gazon și toate produsele alimentare. Nu este listat pentru utilizare în țările UE.
Expediție
UN1989 Aldehide, n.s.a., Clasa de pericol: 3; Etichete: 3-Lichid inflamabil
Incompatibilități
Aldehidele sunt frecvent implicate în reacții de autocondensare sau de polimerizare. Aceste reacții sunt exotermice; ele sunt adesea catalizate de un acid. Aldehidele sunt ușor de oxidat pentru a da acizi carboxilici. Gazele inflamabile și/sau toxice sunt generate de combinarea aldehidelor cu compuși azoici, diazoici, ditiocarbamați, nitruri și agenți reducători puternici. Aldehidele pot reacționa cu aerul pentru a da mai întâi acizi peroxo și, în final, acizi carboxilici. Aceste reacții de autoxidare sunt activate de lumină, catalizate de săruri ale metalelor de tranziție și sunt autocatalitice (catalizate de produsele reacției). Adăugarea de stabilizatori (antioxidanți) la transporturile de aldehide întârzie autoxidarea. Incompatibil cu oxidanții (clorați, nitrați, peroxizi, permanganați, perclorați, clor, brom, fluor, etc.); contactul poate provoca incendii sau explozii. A se ține la distanță de materiale alcaline, baze puternice, acizi puternici, oxoacizi, epoxizi, cetone, coloranți azoici, substanțe caustice, borani, hidrazine
Eliminarea deșeurilor
Incinerare. În conformitate cu 40CFR165, urmați recomandările pentru eliminarea pesticidelor și a recipientelor de pesticide.