
L’origine dell’accoppiamento J può essere visualizzata da un modello vettoriale per una molecola semplice come il fluoruro di idrogeno (HF). In HF, i due nuclei hanno spin 1/2. Sono possibili quattro stati, a seconda dell’allineamento relativo degli spin nucleari H e F con il campo magnetico esterno. Le regole di selezione della spettroscopia NMR impongono che ΔI = 1, il che significa che un dato fotone (nella gamma delle radiofrequenze) può influenzare (“flip”) solo uno dei due spin nucleari.L’accoppiamento J fornisce tre parametri: la molteplicità (il “numero di linee”), la grandezza dell’accoppiamento (forte, medio, debole), e il segno dell’accoppiamento.
MultiplicityEdit
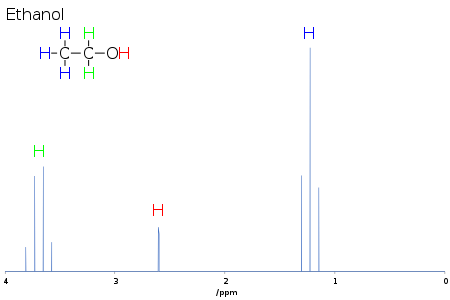
La molteplicità fornisce informazioni sul numero di centri accoppiati al segnale di interesse e sul loro spin nucleare. Per sistemi semplici, come nell’accoppiamento 1H-1H nella spettroscopia NMR, la molteplicità è uno in più del numero di protoni adiacenti che sono magneticamente non equivalenti ai protoni di interesse. Per l’etanolo, ogni protone di metile è accoppiato ai due protoni di metilene, quindi il segnale di metile è un tripletto. E ogni protone metilico è accoppiato ai tre protoni metilici, quindi il segnale metilico è un quartetto.
Nuclei con spin maggiore di 1/2, che sono chiamati quadrupolari, possono dare luogo a uno splitting maggiore, anche se in molti casi l’accoppiamento a nuclei quadrupolari non si osserva. Molti elementi sono composti da nuclei con spin nucleare e senza. In questi casi, lo spettro osservato è la somma degli spettri per ogni isotopomero. Una delle grandi convenienze della spettroscopia NMR per le molecole organiche è che molti importanti nuclei con spin 1/2 più leggeri sono monoisotopici, per esempio 31P e 19F, o hanno abbondanza naturale molto alta, per esempio 1H. Un’ulteriore convenienza è che 12C e 16O non hanno spin nucleare così questi nuclei, che sono comuni nelle molecole organiche, non causano modelli di scissione in NMR.
Magnitudine di J-accoppiamentoModifica
Per l’accoppiamento 1H-1H, la magnitudine di J fornisce informazioni sulla vicinanza dei partner di accoppiamento. In generale, l’accoppiamento a due legami (cioè 1H-C-1H) è più forte dell’accoppiamento a tre legami (1H-C-C-1H). La grandezza dell’accoppiamento fornisce anche informazioni sugli angoli diedri relativi ai partner di accoppiamento, come descritto dall’equazione di Karplus per le costanti di accoppiamento a tre legami.
Per l’accoppiamento eteronucleare, la grandezza di J è legata ai momenti magnetici nucleari dei partner di accoppiamento. 19F, con un alto momento magnetico nucleare, dà luogo a un grande accoppiamento con i protoni. 103Rh, con un momento magnetico nucleare molto piccolo, dà solo piccoli accoppiamenti con 1H. Per correggere l’effetto del momento magnetico nucleare (o equivalentemente il rapporto giromagnetico γ), viene spesso discussa la “costante di accoppiamento ridotta” K, dove
K = 4π2J/hγxγy.
Per l’accoppiamento di un nucleo 13C e un protone direttamente legato, il termine dominante nella costante di accoppiamento JC-H è l’interazione di contatto di Fermi, che è una misura del carattere s del legame ai due nuclei.
Dove il campo magnetico esterno è molto basso, ad es. come NMR campo terrestre, J-accoppiamento segnali dell’ordine di hertz di solito dominano spostamenti chimici che sono dell’ordine di millihertz e non sono normalmente risolvibile.
Segno di J-accoppiamentoModifica
Il valore di ogni costante di accoppiamento ha anche un segno, e costanti di accoppiamento di grandezza comparabile spesso hanno segni opposti. Se la costante di accoppiamento tra due rotazioni date è negativa, l’energia è più bassa quando queste due rotazioni sono parallele, e viceversa se la loro costante di accoppiamento è positiva. Per una molecola con una singola costante di accoppiamento J, l’aspetto dello spettro NMR è invariato se il segno della costante di accoppiamento è invertito, anche se le linee spettrali in determinate posizioni possono rappresentare transizioni diverse. Il semplice spettro NMR quindi non indica il segno della costante di accoppiamento, che non c’è un modo semplice di prevedere.
Tuttavia per alcune molecole con due distinte costanti di accoppiamento J, i segni relativi delle due costanti possono essere determinati sperimentalmente da un esperimento di doppia risonanza. Per esempio nello ione dietiltallio (C2H5)2Tl+, questo metodo ha mostrato che le costanti di accoppiamento metil-tallio (CH3-Tl) e metilene-tallio (CH2-Tl) hanno segni opposti.
Il primo metodo sperimentale per determinare il segno assoluto di una costante di accoppiamento J fu proposto nel 1962 da Buckingham e Lovering, che suggerirono l’uso di un forte campo elettrico per allineare le molecole di un liquido polare. Il campo produce un accoppiamento dipolare diretto dei due spin, che si aggiunge all’accoppiamento J osservato se i loro segni sono paralleli e si sottrae all’accoppiamento J osservato se i loro segni sono opposti. Questo metodo è stato applicato per la prima volta al 4-nitrotoluene, per il quale la costante di accoppiamento J tra due protoni adiacenti (o orto) dell’anello ha dimostrato di essere positiva perché la scissione dei due picchi per ogni protone diminuisce con il campo elettrico applicato.
Un altro modo per allineare le molecole per la spettroscopia NMR è di scioglierle in un solvente nematico a cristalli liquidi. Questo metodo è stato usato anche per determinare il segno assoluto delle costanti di accoppiamento J.
.