- Activation des cellules satellites et rétention du potentiel régénérateur musculaire après une dénervation à long terme
- Le lithium module les niveaux de miR-1906 des vésicules extracellulaires dérivées de cellules souches mésenchymateuses contribuant à la neuroprotection post-AVC par la régulation du récepteur 4 de type péage
- Les vésicules extracellulaires dérivées des fibroblastes favorisent la cicatrisation des plaies en optimisant les fonctions cellulaires fibroblastiques et endothéliales
- Coadministration de cellules endothéliales et musculaires lisses dérivées de cellules souches pluripotentes induites humaines comme thérapie pour l’ischémie critique des membres
Activation des cellules satellites et rétention du potentiel régénérateur musculaire après une dénervation à long terme
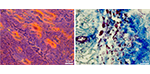
Alvin Wong, et al, STEM CELLS
La lésion du nerf moteur entraîne une atrophie de l’organe terminal qui est permanente si la réinnervation est retardée. Malgré l’énormité du problème clinique, la pathophysiologie empêchant la récupération musculaire est mal comprise. Les auteurs rapportent que, même après des périodes prolongées suivant une lésion nerveuse, les cellules souches du muscle dénervé conservent des capacités de régénération comparables à celles du muscle non lésé. Ces résultats indiquent que l’observation selon laquelle une dénervation prolongée entraîne une atrophie musculaire permanente n’est pas due à un changement intrinsèque du potentiel régénérateur des cellules souches musculaires et suggère que les efforts pour restaurer la fonction devraient se concentrer sur les signaux pour induire une régénération intrinsèque et la restauration de la continuité neuromusculaire.
Le lithium module les niveaux de miR-1906 des vésicules extracellulaires dérivées de cellules souches mésenchymateuses contribuant à la neuroprotection post-AVC par la régulation du récepteur 4 de type péage

Matteo Haupt, et al, STEM CELLS Translational Medicine
Le présent travail indique, pour la première fois, un potentiel thérapeutique accru des vésicules extracellulaires (EVs) dérivées de cellules souches mésenchymateuses préconditionnées au lithium contre l’ischémie cérébrale. En élucidant un nouveau mode d’action de ces VE enrichies, le présent travail démontre une augmentation des concentrations intravésiculaires de certains miARN tels que le miR-1906. Ce dernier régule le récepteur 4 de type péage et les cascades de signalisation pro-inflammatoires familières, contribuant à une meilleure récupération neurologique après un accident vasculaire cérébral. Par conséquent, ce travail fournit des preuves supplémentaires et nouvelles pour le potentiel thérapeutique des VE contre l’AVC, ouvrant la voie à des études translationnelles supplémentaires et à des essais cliniques dans des contextes d’AVC.
Les vésicules extracellulaires dérivées des fibroblastes favorisent la cicatrisation des plaies en optimisant les fonctions cellulaires fibroblastiques et endothéliales
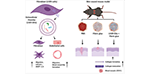
Eun Jung Oh, et al…, STEM CELLS
Les vésicules extracellulaires (EVs) ont été affichées comme des candidats capables de livrer des cargos thérapeutiques endogènes pour les thérapies régénératives. Les fibroblastes pourraient être des cellules sources candidates pour les EVs, afin d’étudier leurs effets thérapeutiques dans la guérison des blessures. À la connaissance des auteurs, il s’agit de la première étude à examiner les effets de cicatrisation in vitro des VE sécrétées par des fibroblastes murins. Cette étude a prouvé la cicatrisation de plaies de pleine épaisseur en utilisant un modèle de souris et les effets de cicatrisation in vivo en utilisant une combinaison de colle de fibrine disponible dans le commerce et d’EVs sécrétées par des fibroblastes.
Coadministration de cellules endothéliales et musculaires lisses dérivées de cellules souches pluripotentes induites humaines comme thérapie pour l’ischémie critique des membres
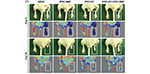
Jin Ju Park, et al…, STEM CELLS Translational Medicine
La maladie ischémique est une maladie des artères périphériques, qui indique une douleur au repos avec des nécroses et des ulcères conduisant à l’amputation. En raison de la capacité des cellules endothéliales et des cellules musculaires lisses vasculaires à régénérer l’artère périphérique dans les tissus ischémiques, les thérapies cellulaires constituent un moyen prometteur de traiter les patients atteints de maladie ischémique. Cette étude démontre que la cotransplantation de cellules endothéliales et de cellules musculaires lisses dérivées de cellules souches pluripotentes induites améliore la perfusion sanguine et le taux de récupération du membre en favorisant la néovascularisation du membre ischémique par un mécanisme paracrine médié par les exosomes dérivés des cellules musculaires lisses. Cette étude présente une nouvelle technique de thérapie cellulaire pour traiter les maladies vasculaires périphériques.