Klinisk journal
Två patienter med ornitintranskarbamylasbrist, en ureacykelstörning, överfördes till vår intensivvårdsavdelning inom 12 månader. Båda var tidigare friska män som inledningsvis presenterade sig med obestämda men progressiva neurologiska symtom efter mindre ingrepp (sammanfattningar av fallen i ruta 1).
Varje patient utvecklade sina första neurologiska symtom (huvudvärk, mental långsamhet, inkoordination) cirka 24-48 timmar efter den troliga utlösande faktorn, som i båda fallen var en engångsdos av en kortikosteroid. Hos patient 1 utvecklades sömnighet vid 48 timmar till inkoherens, suddig syn och allvarlig agitation som krävde intubering 2 dagar senare. Hos patient 2 utvecklades huvudvärk, illamående, suddig syn och epigastrisk smärta vid 48 timmar under de följande två dagarna till förvirring och långsamt tal.
När de presenterades för ett perifert sjukhus hade en omfattande panel av patologiska undersökningar genomförts för varje patient, inklusive blodprover (fullständig blodstatus, njurfunktionstester, leverenzymnivåer, koagulationsprofil och inflammatoriska markörer), lumbalpunktion och hjärnavbildningar (datortomografi och magnetresonanstomografi). Resultaten av dessa undersökningar var alla okej.
Identifiering av betydande hyperammonemi fördröjdes till cirka 36-48 timmar efter att man presenterades på sjukhuset. Patienterna var komatösa när de överfördes till vårt sjukhus. Patient 1 hade en långvarig vistelse på vår intensivvårdsavdelning, med ett ihållande minimalt medvetandetillstånd. Patient 2 gick vidare till hjärndöd och organdonation.
Läkare kommer att vara bekanta med de vanligaste orsakerna till hyperammonemi, inklusive en ökad proteinbelastning i samband med leversjukdom och enzymatisk dysfunktion i ureacykeln som orsakas av mediciner som till exempel natriumvalproat. Mindre vanliga men viktiga orsaker till förhöjda ammoniaknivåer i blodet är de ärftliga ureacykelstörningarna (UCD). De allvarligaste formerna uppträder tidigt i livet, men mildare former av dessa störningar kan visa sig i vuxen ålder.
UCD:er är en grupp av medfödda fel i ämnesomsättningen, med en uppskattad total incidens på mellan 1:80001 och 1:30 0002 födslar. De orsakas av dysfunktion hos något av de sex enzymer eller två transportproteiner som är involverade i ureabiosyntesen, en process som huvudsakligen sker i levern. Ureacykeln är den terminala vägen för bortskaffande av ammoniak som bildas vid katabolism av aminosyror. Ammoniak är neurotoxiskt, och varje akut ökning av blodnivåerna över 50 μmol/L kan orsaka neurologiska symtom. Ammoniaknivåer över 100 μmol/L kan orsaka obtundation, men mildare förhöjningar bör tolkas inom ramen för det kliniska sammanhanget för deras förekomst.
Den UCD som drabbade våra två patienter var ornitintranskarbamylas (OTC)-brist, den vanligaste av ureacykelstörningarna. OTC-brist är ett X-bundet drag och uttrycks därför oftare hos män, även om kvinnliga bärare kan dekompensera efter en betydande påfrestning, t.ex. en förlossning.3 De andra UCD:erna är autosomalt recessiva drag.4
Den första uppvisningen i vuxen ålder kan tillskrivas den lindrigare graden av bristen, och ofta också till självbegränsning av proteinintaget som ett inlärt beteende, vilket möjliggör stabilitet tills en miljöstressfaktor inträffar. Förhållanden som leder till ökade krav på ureacykeln, t.ex. proteinbelastning, infektion, systemiska kortikosteroider, snabb viktnedgång, kirurgi, trauma och kemoterapi5 , kan alla påskynda dekompensation hos personer med UCD. Fallet med en 44-årig man som dog av en tidigare odiagnostiserad OTC-brist efter koronar bypass-kirurgi rapporterades i denna tidning 2007.6
I de två patienter som beskrivs i vår artikel var en enstaka men betydande tillfällig dos av kortikosteroid den första utlösande händelsen, med långvarig fasta som vidmakthöll en ond metabolisk cykel som kulminerade i allvarlig hyperammonemi.
Hyperammonemi hos vuxna kan visa sig med psykiatriska eller neurologiska symtom, inklusive huvudvärk, förvirring, agitation med stridbart beteende, dysartri, ataxi, hallucinationer och synnedsättning,3 symtom som återspeglar toxisk metabolisk encefalopati. Buksymtom (illamående, kräkningar) kan åtfölja fenomenen i nervsystemet.
Våra två fall illustrerar förloppet av progressiv hyperammonemi om behandlingen inte inleds tidigt: förvärrad kognitiv nedsättning och cerebralt ödem, med utveckling av koma, kramper och död på grund av intrakraniell hypertension.
När det inte finns någon alternativ förklaring till den oproportionerliga och progressiva karaktären hos en patients kognitiva störning bör detta tas som en viktig ledtråd för att undersöka möjligheten av en metabolisk etiologi. Eftersom nedgången sker under flera dagar finns det ett fönster för livräddande ingrepp om tillståndet uppmärksammas i tid.
Mätning av ammoniaknivån i blodet som en del av en metabolisk screening bör i ett sådant fall utföras vid tidigast möjliga tillfälle. Om ammoniaknivån är förhöjd bör en metabol specialist konsulteras, en aminosyreprofil i plasma utarbetas, organiska syror och oroticsyra i urinen mätas och akut behandling av hyperammonemi inledas.
De tre delarna av behandlingen av ett ureacykelbundet hyperammonaemiskt koma omfattar:
-
fysiskt avlägsnande av ammoniak genom hemodialys eller hemodiafiltrering;
-
omvändning av det katabola tillståndet genom infusion av insulin/dextros och intralipid; och
-
tillfälligt innehållande av protein och påbörjande av kväveavskiljare, när de är tillgängliga.
Dessa åtgärder bör inledas under ledning av en metabolisk läkare och på en intensivvårdsavdelning där agitation eller koma kan hanteras. Ammoniaknivåerna kan snabbt sänkas genom dialys; avlägsnandet är beroende av flödeshastigheten, vilket gör intermittent hemodialys till den mest effektiva metoden för clearance, se ruta 2. Av denna anledning förespråkar vi intermittent dialys snarare än kontinuerlig venvenös hemodiafiltrering för tidig ammoniakkontroll i akutsituationer.
Vänligt allvarlig neurologisk försämring vid behandlingsstart är ett stort bekymmer, men detta bör i sig inte vara ett skäl att avstå från behandling, eftersom god neurologisk återhämtning är möjlig. Detta illustreras av fallrapporten om en medelålders patient som återhämtade sig, trots dekorticate posturing när behandlingen inleddes.5
Vi förespråkar en tidig bedömning av ammoniaknivåerna hos patienter med oförklarligt förändrat medvetandetillstånd, eller när deras kognitiva störning verkar oproportionerlig i förhållande till någon samtidig systemisk sjukdom. Många av de nödvändiga delarna av vården kan inledas på icke-tertiära intensivvårdsavdelningar. Det är viktigt att behandlingen inleds på det sjukhus där patienten presenteras, eftersom detta är en medicinsk nödsituation. Det neurologiska utfallet och överlevnaden är kritiskt beroende av tidpunkten för ingripandet. Om det upptäcks tidigt och behandlas på lämpligt sätt är prognosen för neurologisk återhämtning god.
Lärdomar för praktiken
-
Ureacykelstörningar kan först uppträda i vuxen ålder och avslöjas av utlösande faktorer som systemisk sjukdom, ökad proteinbelastning, kirurgi eller kortikosteroider.
-
Bedömning av ammoniaknivåerna är ett enkelt men kritiskt test hos patienter med oförklarlig medvetandeförsämring.
-
En session intermittent hemodialys är mycket effektiv för snabb ammoniakkontroll och överlägsen kontinuerlig hemodiafiltrering för snabb korrigering.
-
En akut behandling av hyperammonemi bör påbörjas tidigt för att förhindra förödande neurologiska skador.
Box 1 – Fallbeskrivningar för de två patienterna
Patient 1: 24 år gammal, man
Medicinsk historia
- Obstruktiv sömnapné; ingen anmärkningsvärd familjehistoria; högfungerande individ
- Sannolikt utlösande faktor: intraoperativt dexametason (8 mg) under nasal septoplasty
Progress
- Vaghet och letargi 48 timmar efter operationen, övergick under 24 timmar till inkoherens
- Intuberades 12 timmar senare på grund av allvarlig agitation
- GCS sjönk till 5-6 under de följande 48 timmarna; Ammoniaknivå, 334 μmol/L (RR, < 50 μmol/L); Sjukdomsspecifik behandling inleddes
- Höjt intrakraniellt tryck 6 timmar senare (dilaterade pupiller med cerebralt ödem på CT av hjärnan), vilket ledde till dekompressiv kraniektomi som komplicerades av frontalt hematom, som krävde evakuering
- Långvarig intensivvårdsavdelning och sjukhusvistelse
Utfall
- Persisterande minimalt medvetet tillstånd (vid 22 månader)
- Utskrivs till vårdinrättning
- Biokemisk analys av plasma och urin som stämmer överens med OTC-brist (förhöjd orotikasyra i urinen; Plasmaglutaminnivå hög, låga nivåer av ornitin, citrullin och arginin i plasma)
- Genetisk testning bekräftade OTC-genmutation i samband med OTC-brist
Patient 2: 39 år gammal, man
Medicinsk historia
- Kronisk knäsmärta; ingen anmärkningsvärd familjehistoria; högfungerande individ
- Sannolikt utlösande faktor: Kortisoninjektion i knäet för knäsmärta
Förlopp
- Huvudvärk, illamående, epigastrisk smärta, suddig syn och inkoordination 48 timmar efter injektionen
- Fortsatte under de följande 48 timmarna till förvirring, långsamt tal
- Progressiv nedgång i GCS, vilket krävde intubation
- Krampaktivitet
- Upprepad CT av hjärnan visade cerebralt ödem
- Ammoniaknivå: 652 μmol/L (RR, < 50 μmol/L); sjukdomsspecifik behandling påbörjad; intrakraniell tryckmätare insatt; bristande kontroll av intrakraniell hypertoni; beslut om palliation
Outcome
- Fortsattes till hjärndöd och organdonation (med undantag för leverdonation: Biokemiska fynd överensstämmer med OTC-brist (kraftig förhöjning av orotic acid i urinen, hög nivå av plasmaglutamin, låg nivå av arginin)
- Genetiska tester bekräftade OTC-genmutation som är associerad med OTC-brist
GCS = Glasgow coma score; RR = referensintervall; CT = datortomografi; OTC = ornitintranskarbamylas.
Box 2 – Ammoniaknivåer hos våra två patienter och deras svar på behandling*
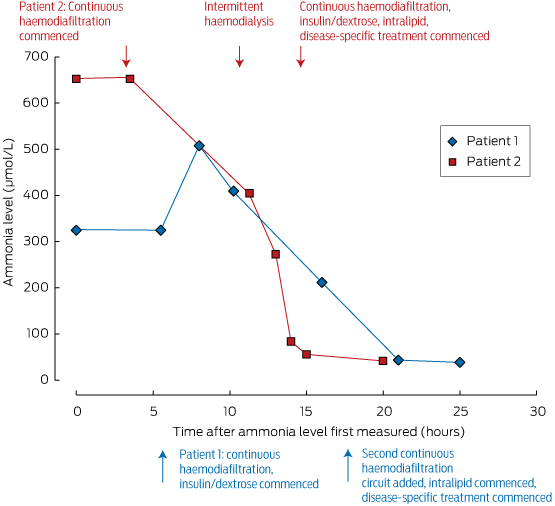
* Notera den snabba minskningen av serumammoniaknivåerna hos patient 2 som uppnåddes efter det att intermittent hemodialys inletts (cirka 10 timmar efter första mätningen).