Lärandemål
- Att definiera och ge exempel på de viktigaste typerna av radioaktivitet.
Atomer består av subatomära partiklar – protoner, neutroner och elektroner. Protoner och neutroner finns i atomkärnan och står för större delen av atomens massa, medan elektroner kretsar kring atomkärnan i skal och underskal och står för atomens storlek. Kom ihåg notationen för att kortfattat representera en isotop av en viss atom:
\
Elementet i detta exempel, som representeras av symbolen C, är kol. Dess atomnummer, 6, är det nedre vänstra tecknet på symbolen och är antalet protoner i atomen. Massatalet, det översta ledet till vänster på symbolen, är summan av antalet protoner och neutroner i kärnan i just denna isotop. I det här fallet är masstalet 12, vilket innebär att antalet neutroner i atomen är 12 – 6 = 6 (dvs. atomens masstal minus antalet protoner i kärnan är lika med antalet neutroner). Ibland utelämnas atomnumret i denna notation eftersom själva symbolen för grundämnet förmedlar dess karakteristiska atomnummer. De två isotoperna av väte, 2H och 3H, har fått egna namn: deuterium (D) respektive tritium (T). Ett annat sätt att uttrycka en viss isotop är att ange masstalet efter grundämnets namn, som kol-12 eller väte-3.
Atomteorin på 1800-talet utgick från att atomkärnorna hade fasta sammansättningar. Men 1896 upptäckte den franske vetenskapsmannen Henri Becquerel att en uranförening som placerades nära en fotografisk platta gav en bild på plattan, även om föreningen var insvept i svart tyg. Han resonerade att uranföreningen avgav någon form av strålning som passerade genom tyget för att exponera den fotografiska plattan. Ytterligare undersökningar visade att strålningen var en kombination av partiklar och elektromagnetiska strålar, med atomkärnan som yttersta källa. Dessa emanationer kallades slutligen, kollektivt, för radioaktivitet.
Det finns tre huvudformer av radioaktiva utsläpp. Den första kallas alfapartikel,som symboliseras av den grekiska bokstaven α. En alfapartikel består av två protoner och två neutroner och är alltså samma sak som en heliumkärna. (Vi använder ofta \(\ce{^{4}_{2}He}\) för att representera en alfapartikel). Den har en laddning på 2+. När en radioaktiv atom avger en alfapartikel minskar den ursprungliga atomens atomnummer med två (på grund av förlusten av två protoner) och dess masstal minskar med fyra (på grund av förlusten av fyra kärnpartiklar). Vi kan representera avgivningen av en alfapartikel med en kemisk ekvation – till exempel är alfapartikelavgivningen av uran-235 följande:
\
Hur vet vi att en produkt av reaktionen är \(\ce{^{231}_{90}Th}\)? Vi använder oss av lagen om materiens bevarande, som säger att materia inte kan skapas eller förstöras. Detta innebär att vi måste ha samma antal protoner och neutroner på båda sidor av den kemiska ekvationen. Om vår urankärna förlorar 2 protoner finns det 90 protoner kvar, vilket identifierar grundämnet som torium. Om vi dessutom förlorar 4 kärnpartiklar av de ursprungliga 235, återstår 231 kärnpartiklar. Vi använder alltså subtraktion för att identifiera thoriumatomens isotop – i detta fall \(\ce{^{231}_{90}Th}\).
Kemister använder ofta namnen moderisotop och dotterisotop för att representera den ursprungliga atomen och den produkt som inte är alfapartikeln. I det föregående exemplet är \(\ce{^{235}_{92}U}\) moderisotopen och \(\ce{^{231}_{90}Th}\) dotterisotopen. När ett grundämne förändras till ett annat på detta sätt genomgår det radioaktivt sönderfall.
Exempel \(\(\PageIndex{1}\): Radon-222
Skriv kärnekvationen som representerar det radioaktiva sönderfallet av radon-222 genom alfapartikelemission och identifiera dotterisotopen.
Lösning
Radon har atomnumret 86, så moderisotopen representeras som \(\ce{^{222}_{86}Rn}\). Vi representerar alfapartikeln som \(\ce{^{4}_{2}He}\) och använder subtraktion (222 – 4 = 218 och 86 – 2 = 84) för att identifiera dotterisotopen som en isotop av polonium, \(\mathrm{^{218}_{84}Po}\):
\(\ce{_{86}^{222}Rn\rightarrow \, _2^4He + \, _{84}^{218}Po}\})
Övning \(\PageIndex{1}\): Polonium-209
Skriv den nukleära ekvation som representerar det radioaktiva sönderfallet av polonium-209 genom alfapartikelemission och identifiera dotterisotopen.
Svar
\(\ce{_{_{84}^{209}Po\rightarrow \, _2^4He + \, _{82}^{205}Pb}\)
Den andra stora typen av radioaktiv emission kallas för en betapartikel, som symboliseras med den grekiska bokstaven β. En betapartikel är en elektron som kastas ut från atomkärnan (inte från elektronskalen kring atomkärnan) och har laddningen 1-. Vi kan också representera en betapartikel som \(\ce{^0_{-1}e}\) eller β-. Nettoeffekten av betapartikelavgivningen på en atomkärna är att en neutron omvandlas till en proton. Det totala masstalet förblir detsamma, men eftersom antalet protoner ökar med en, ökar atomnumret med en. Kol-14 sönderfaller genom att emittera en betapartikel:
\
Även här är summan av atomtalen densamma på båda sidor av ekvationen, liksom summan av masstal. (Observera att elektronen tilldelas ett ”atomnummer” på 1-, vilket är lika med dess laddning.)
Den tredje stora typen av radioaktiv strålning är inte en partikel utan snarare en mycket energirik form av elektromagnetisk strålning som kallas gammastrålning och som symboliseras av den grekiska bokstaven γ. Gammastrålning i sig bär inte på någon övergripande elektrisk laddning, men den kan slå ut elektroner ur atomer i ett materieprov och göra det elektriskt laddat (varför gammastrålning benämns som joniserande strålning). Vid det radioaktiva sönderfallet av radon-222 avges till exempel både alfa- och gammastrålning, där den senare har en energi på 8,2 × 10-14 J per sönderdelad atomkärna:
\
Detta kan tyckas vara lite energi, men om 1 mol radonatomer skulle sönderfalla skulle gammastrålningsenergin vara 49 miljoner kJ!
Exempel \(\PageIndex{2}\): Boron-12
Skriv den nukleära ekvation som representerar det radioaktiva sönderfallet av boron-12 genom betapartikelemission och identifiera dotterisotopen. En gammastråle avges samtidigt med betapartikeln.
Lösning
Moderisotopen är \(\ce{^{12}_{5}B}\) medan en av produkterna är en elektron, \(\ce{^{{0}_{-1}e}\). För att massa- och atomnumren ska ha samma värde på båda sidor måste massnumret för dotterisotopen vara 12, och dess atomnummer måste vara 6. Det grundämne som har atomnumret 6 är kol. Den fullständiga kärnämnesekvationen är alltså följande:
\
Dotterisotopen är \(\ce{^{12}_6 C}\).
Övningsuppgift \(\PageIndex{2}\): Jod-131
Skriv kärnekvationen som representerar det radioaktiva sönderfallet av jod-131 genom betapartikelemission och identifiera dotterisotopen. En gammastråle avges samtidigt med betapartikeln.
Svar
Alpha-, beta- och gammastrålar har olika förmåga att tränga igenom materia. Den relativt stora alfapartikeln stoppas lätt av materia (även om den kan överföra en betydande mängd energi till den materia den kommer i kontakt med). Betapartiklar penetrerar svagt in i materia, kanske högst några centimeter. Gammastrålar kan tränga djupt in i materia och överföra en stor mängd energi till den omgivande materian. I tabell \(\PageIndex{1}\) sammanfattas egenskaperna hos de tre huvudtyperna av radioaktiva utsläpp.
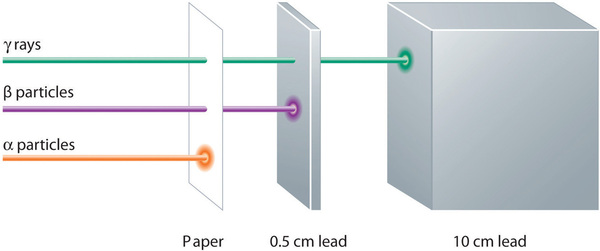
| Karakteristik | Alphapartiklar | Betapartiklar | Gammastrålar | |
|---|---|---|---|---|
| symboler | α, \(\mathrm{_{2}^{4}He}\) | β, \(\ce{^{0}_{-1} e}\) | γ | |
| identitet | heliumkärna | elektron | elektronisk | elektromagnetisk strålning |
| laddning | 2+ | 1- | ingen | |
| massetal | 4 | 0 | 0 | |
| penetrerande kraft | minimal (tränger inte in i huden) | kort (tränger in i huden och vissa vävnader något) | djup (tränger in i vävnader djupt) |
Enstaka gånger, en atomkärna sönder i mindre bitar i en radioaktiv process som kallas spontan fission (eller klyvning). Vanligtvis är de dotterisotoper som produceras av fission en varierad blandning av produkter, snarare än en specifik isotop som vid alfa- och betapartikelemission. Ofta producerar fission ett överskott av neutroner som ibland fångas in av andra atomkärnor, vilket eventuellt leder till ytterligare radioaktiva händelser. Uran-235 genomgår spontan fission i liten utsträckning. En typisk reaktion är
\
där \(\ce{_0^1n}\) är en neutron. Som vid alla kärntekniska processer måste summorna av atomnummer och masstal vara desamma på båda sidor av ekvationen. Spontan klyvning förekommer endast i stora kärnor. Den minsta kärnan som uppvisar spontan fission är bly-208.
Fission är den radioaktiva process som används i kärnkraftverk och en typ av atombomb.
Nyckeluppfattning
De viktigaste typerna av radioaktivitet är alfapartiklar, betapartiklar och gammastrålar.
Konceptgenomgångsövning
-
Vilka är de viktigaste typerna av radioaktivitet? Skriv kemiska ekvationer som visar varje typ.
Svar
-
De viktigaste typerna av radioaktivitet är alfadegörelse, betadegörelse och gammastrålning; alfadegörelse med gammastrålning: \(\(\mathrm{_{86}^{222}Rn \rightarrow \, _{84}^{218}Po + \, ^4_2He + \gamma}\): \(\ce{_6^{14}C \rightarrow _7^{14}N + ^0_{-1}e}\) (svaren varierar)