- Key Points
- Wprowadzenie
- Metody
- Results
- Sample and Participants’ Experience
- Średnia całkowita szkodliwość
- Różnica między oceniającymi ze szpitali ostrych i rehabilitacyjnych?
- Porównanie z ostatnią analizą europejską
- Sprawdzenie wiarygodności i test wrażliwości
- Dyskusja
- Podsumowanie
- Oświadczenie o dostępności danych
- Oświadczenie o etyce
- Wkład autorów
- Konflikt interesów
- Podziękowania
- Materiały uzupełniające
Key Points
Narkotyki nielegalne, takie jak metamfetamina, heroina i kokaina, a także alkohol zostały uznane za szczególnie szkodliwe.
Leki wydawane na receptę, w tym opioidy (w przeciwieństwie do USA, Kanady i Australii) oraz nieopioidowe leki przeciwbólowe, w tym gabapentynoidy, zostały uznane za mniej szkodliwe.
Obecne przepisy są w pewnym stopniu niezgodne z tymi rankingami szkodliwości.
Wprowadzenie
Nadużywanie uzależniających substancji psychoaktywnych charakteryzuje się negatywnymi konsekwencjami zdrowotnymi i społecznymi nie tylko dla użytkownika, ale także dla osób nieużywających w danej społeczności lub społeczeństwie (1, 2). W DSM-5 zdefiniowano różne specyficzne stany zależności i uzależnienia od substancji (3), a kodowanie ICD-10 odzwierciedla odrębne zaburzenia psychiczne i behawioralne związane z alkoholem, tytoniem, opiatami, kokainą, stymulantami, halucynogenami, środkami uspokajającymi i hipnotycznymi, konopiami indyjskimi i kannabinoidami oraz lotnymi rozpuszczalnikami (4).
W ciągu ostatnich 15 lat w Anglii (5), Holandii (6), Szkocji (7), Francji (8), a ostatnio w Australii (9) eksperci medyczni i niemedyczni ds. uzależnień określili względny potencjał szkód zdrowotnych i społecznych różnych substancji uzależniających. Średnią ogólną szkodliwość różnych substancji podaje się zazwyczaj w rankingach względnych, opartych na analizach wielodecyzyjnych (5, 9) lub na ocenach „ad-hoc” (6-8) z wykorzystaniem zatwierdzonych wymiarów zdrowotnych i społecznych (5). Rankingi te niekoniecznie wykazują zgodność z priorytetami ustawodawczymi i w zakresie egzekwowania prawa w odniesieniu do względnej regulacji i kontroli substancji, przy czym alkohol jest doskonałym przykładem dysonansu między ogólnymi szkodami a wysiłkami na rzecz kontroli (5-9). Nutt i wsp. jako pierwsi wykazali tę niespójność (5).
W 2014 r. grupa 40 medycznych i niemedycznych ekspertów ds. uzależnień z 21 krajów UE doszła do tego samego wniosku (10). Badanie to obejmowało 20 substancji (10). W międzyczasie, podobnie jak w innych krajach zachodnich, w Niemczech nastąpiła zmiana wzorców tendencji w zakresie nadużywania substancji, jak również politycznych warunków ramowych, w szczególności
– Wzrost nadużywania metamfetaminy głównie w regionach graniczących z Republiką Czeską (11-13).
– Coraz częstsze występowanie nowych substancji psychoaktywnych (NPS), w szczególności mnogość syntetycznych kannabinoidów i stymulantów (głównie katynonów) (12-14).
– Wzrost śmiertelnych przedawkowań heroiną/morfiną, opioidowymi i nieopioidowymi lekami przeciwbólowymi, syntetycznymi opioidami, narkotykami, amfetaminą, pochodnymi amfetaminy, metamfetaminą i NPS, przy jednoczesnym spadku liczby zgonów z powodu przedawkowania lekami stosowanymi w leczeniu uzależnienia od opioidów, takimi jak metadon i buprenorfina (11, 15).
– Rosnąca dostępność silnie działających produktów z konopi indyjskich o zwiększonym ryzyku psychozy i uzależnienia (11, 13, 16, 17).
– Legalizacja leczniczej marihuany i kannabinoidów na receptę (18).
W związku z tymi zmianami staraliśmy się zaktualizować ocenę szkód zdrowotnych i społecznych związanych z substancjami, które są powszechnie nadużywane w Niemczech i innych krajach, a także z substancjami rzadziej nadużywanymi w naszym kraju, ale już pojawiającymi się (11, 12). W tym kontekście syntetyczne kannabinoidy (14) zostały po raz pierwszy uwzględnione w rankingach szkód. Do badań indeksowych rankingów szkodliwości włączyliśmy również propofol – anestetyk dożylny (19) oraz niektóre nieopioidowe leki przeciwbólowe (NOA), tj. gabapentynoidy, niesteroidowe leki przeciwzapalne (NLPZ), flupirtynę i tryptany (20-24). Zdecydowaliśmy się na włączenie NOAs razem z opioidowymi lekami przeciwbólowymi do naszej klasyfikacji, ponieważ gabapentyna i pregabalina (gabapentynoidy) znalazły się ostatnio w centrum zainteresowania medycyny uzależnień. W ostatniej dekadzie w kilku bazach danych dotyczących nadzoru nad bezpieczeństwem farmakoterapii, badaniach populacyjnych i opisach przypadków ostrzegano o ich potencjalnym ryzyku nadużywania i przypuszczalnym udziale w śmiertelnych przedawkowaniach, zwłaszcza w połączeniu z opioidami (22, 23). Chociaż powszechnie uważa się, że NLPZ nie uzależniają, ostatnie opisy przypadków (25, 26) i dane epidemiologiczne (27, 28) oraz kliniczne (24) budzą pewne obawy co do bezpieczeństwa tego tradycyjnego poglądu. Inne NOA również wykazały możliwość nadużywania i uzależnienia, np. flurpirtyna (21) lub tryptany (20). Dlatego też uznaliśmy za rozsądne włączenie po raz pierwszy do tego rodzaju badania również wyżej wymienionych NOAs. To badanie jest pierwszym tego rodzaju, które obejmuje porównawcze rankingi szkodliwości kilku nowych substancji nadużywanych, zarówno legalnych/recepturowych, jak i nielegalnych.
Metody
To przekrojowe badanie kwestionariuszowe składało się z dwóch kolejnych etapów (ankieta 1 i ankieta 2, patrz poniżej), w których kwestionariusze ilościowe były rozprowadzane w formie pisemnej wśród niemieckich ekspertów w dziedzinie medycyny uzależnień. Eksperci ci zostali zrekrutowani na niemieckich kongresach i konferencjach dotyczących uzależnień. Dodatkowo kwestionariusze zostały wysłane pocztą elektroniczną do 40 kierowników niemieckich ośrodków leczenia uzależnień od narkotyków, którzy zostali poproszeni o rozprowadzenie ich w swojej strefie wpływów wśród innych specjalistów medycyny uzależnień. W analizie uwzględniono tylko te kwestionariusze, które zostały wypełnione przez lekarzy, którzy (i) byli specjalistami, tj. posiadali dodatkową wiedzę w zakresie co najmniej jednej specjalności medycznej oraz (ii) pracowali dłużej niż 5 lat w szpitalach opieki podstawowej w dziedzinie leczenia zaburzeń związanych z używaniem substancji (SUD). Zachowano anonimowość tożsamości ekspertów z wyjątkiem informacji o ich wieku, płci, specjalnościach, latach doświadczenia zawodowego, latach pracy w trzeciorzędowej opiece nad SUD oraz głównym kierunku pracy zawodowej (szpital ostrej opieki lub rehabilitacyjny) (Tabela 1).
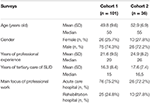
Tabela 1. Charakterystyka uczestników.
Pierwsze badanie zostało przeprowadzone od marca 2016 r. do września 2017 r. i oceniało średnią szkodliwość 33 substancji w 5 wymiarach (szkodliwość fizyczna dla użytkowników, szkodliwość psychologiczna dla użytkowników, szkodliwość społeczna dla użytkowników, szkodliwość fizyczna i psychologiczna dla innych oraz szkodliwość społeczna dla innych). Jak przedstawiono na rysunku uzupełniającym 1, wymiary te określono za pomocą 16 kryteriów, które zostały zatwierdzone w kilku badaniach tego rodzaju (5, 9, 10) (zob. sekcja Materiały uzupełniające-Metody). Ogólna szkoda dla użytkowników i ogólna szkoda dla innych obejmowały odpowiednio 3 wymiary (fizyczny, psychologiczny, społeczny) i 2 wymiary (fizyczny & psychologiczny, społeczny) (szczegóły – zob. rysunek uzupełniający 1). Oceny dokonywano przy użyciu 5-punktowych skal (od „nieszkodliwe” do „bardzo szkodliwe”).
Kwestionariusz odesłało 122 lekarzy, z których oceniono 101, ponieważ 21 ekspertów nie spełniało kryteriów włączenia. Lekarze mogli sami decydować, czy oceniać daną substancję, czy nie, i zostali poinstruowani, aby oszacować swoje doświadczenie zawodowe („brak/mało”, „umiarkowane” lub „dużo”) z każdą substancją, którą oceniali. Informacje te były potrzebne do oceny ważności ocen oraz do weryfikacji zdefiniowanych kryteriów wykluczenia, tj. substancja, która uzyskała <60% ocen lub ponad 60% ocen „brak/małe doświadczenie” została wykluczona z dalszej analizy. W związku z tym substancje ayahuasca, khat i kratom musiały zostać wyłączone z oceny szkód (ryciny uzupełniające 2 i 3).
Drugie badanie (ważenie wymiarów w celu określenia ogólnych szkód na rycinie 1) zostało przeprowadzone od września 2017 r. do maja 2018 r. przez kohortę 2, która została zrekrutowana wyłącznie z wiadomości e-mail do wspomnianych wcześniej 40 kierowników niemieckich ośrodków leczenia uzależnień od narkotyków. Ta ankieta uzupełniająca została podana później, ponieważ pierwsza ankieta była dość obszerna, a połączenie obu ankiet uznano za prawdopodobne przeciążenie respondentów kohorty 1, co zmniejszyło kwotę zwrotu. W drugiej ankiecie poproszono uczestników o oszacowanie względnej wagi (jako proporcji między 0 a 1) każdego z 5 wymiarów użytych w pierwszej ankiecie do określenia ogólnej szkodliwości substancji psychotropowych. Uwzględniono wszystkie z 36 zwróconych kwestionariuszy. W celu obliczenia ogólnej szkodliwości każdej substancji wykorzystaliśmy średnią względną wagę przypisaną przez 36 ekspertów każdemu wymiarowi (wykres 1). Dalsze szczegóły dotyczące obliczania ogólnej szkodliwości pozostałych 30 substancji i powiązanych analiz danych, w tym porównania z poprzednim rankingiem UE (rys. 3), przedstawiono w materiałach uzupełniających.
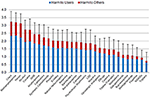
Rysunek 1. Średnia ogólna szkodliwość 30 substancji (wartości średnie i odchylenia standardowe) oceniona przez kohortę 1 w skali od 0 („nieszkodliwa”) do 4 („wyjątkowo szkodliwa”), przedstawiona jako szkodliwa dla użytkowników i szkodliwa dla innych. Względny wkład 5 wymiarów (rysunek uzupełniający 1, tabela uzupełniająca 1) został zważony przez kohortę 2.
Walidację rankingów przeprowadzono najpierw poprzez ocenę wielkości zmienności między ogólną oceną szkodliwości a którymkolwiek z pięciu wymiarów składowych. Różnica między ogólną oceną stopnia szkodliwości a dowolną z 5 oddzielnych ocen w wymiarach ≥8 rang została uznana za istotną i wymagającą wyjaśnienia wiarygodności (Tabela 2). Przeprowadzono dodatkowy test walidacji/wrażliwości, zastępując średnie wagi uzyskane w wyniku naszego badania ankietowego wagami opartymi na konsensusie z poprzedniego badania UE (tabela uzupełniająca 1) i porównując wynikowe rangi substancji na rysunku uzupełniającym 9 z rangami na rysunku 1 (tabela uzupełniająca 2).
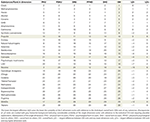
Tabela 2. Plausibility check of the overall harm ranks.
Results
Sample and Participants’ Experience
Lekarze specjaliści pracowali przez medianę 15 lat (kohorta 1) i 16,5 roku (kohorta 2) w trzeciorzędowej opiece nad pacjentami z SUD. Około trzech na czterech uczestników pracowało w szpitalach ostrej opieki, a pozostali w klinikach rehabilitacyjnych (Tabela 1).
Średnia całkowita szkodliwość
Oceny ekspertów w 5 oddzielnych wymiarach przedstawiono na (ryc. 4-8). Jeśli chodzi o ogólną szkodliwość, tradycyjne narkotyki, tj. kokaina (w tym crack), metamfetamina, heroina i alkohol zostały uznane za najbardziej szkodliwe. NPS, tj. katynony i syntetyczne kannabinoidy, zajmowały podrzędne pozycje w grupie o najwyższym poziomie szkodliwości. Ketamina, benzodiazepiny, marihuana, grzyby psychotropowe, LSD, nikotyna i opioidowe leki przeciwbólowe znalazły się w środkowej grupie. Metadon i buprenorfina (oba preferowane w Niemczech w leczeniu podtrzymującym uzależnienia od opioidów) znalazły się w dolnych przedziałach, podczas gdy metylofenidat (w Niemczech preferowany lek w leczeniu ADHD) i NOA znalazły się w najniższych przedziałach rankingu szkodliwości. Wśród NOAs, gabapentyna i pregabalina (gabapentynoidy) zostały uznane za bardziej szkodliwe niż flupirtyna, NLPZ i tryptany (ryc. 1).
Różnica między oceniającymi ze szpitali ostrych i rehabilitacyjnych?
Oceny specjalistów ze szpitali ostrych i rehabilitacyjnych były bardzo podobne, co przedstawiono na rycinie 2.
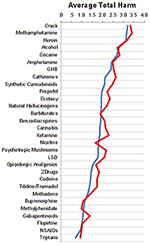
Rysunek 2. Porównanie ocen między specjalistami w szpitalach ostrych (n = 76, krzywa niebieska) vs. rehabilitacyjnych (n = 25, krzywa czerwona).
Porównanie z ostatnią analizą europejską
Ten zaktualizowany niemiecki sondaż ocenił metadon, nikotynę, marihuanę i alkohol jako mniej szkodliwe niż zrobili to oceniający z UE w 2014 roku (10), podczas gdy grzyby psychotropowe, katynony, ecstasy, GHB, metamfetaminę i crack oceniono jako bardziej szkodliwe – patrz rycina 3.
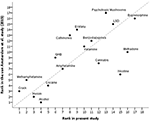
Rysunek 3. Korelacja obecnej oceny i ostatniej oceny UE (10) ogólnej szkodliwości nadużywania narkotyków (rs = 0,73). Dla lepszej orientacji dwusieczna wskazuje idealną korelację (rs = 1).
Sprawdzenie wiarygodności i test wrażliwości
Najmniejsze rozbieżności między średnią rangą szkód ogólnych a rangami w pięciu wymiarach zdrowotnych i społecznych stwierdzono w przypadku tradycyjnych nielegalnych narkotyków: cracku (i innych rodzajów kokainy), heroiny, metamfetaminy, a także alkoholu, które również znalazły się na najwyższych pozycjach pod względem szkód. Podobnie było w przypadku GHB i NPS, które uplasowały się blisko czołówki, ketaminy w środkowym przedziale, opioidów w niższych przedziałach i większości NOA (gabapentynoidy, flupirtyna, tryptany) na najniższych pozycjach. Uderzające rozbieżności zaobserwowano w przypadku propofolu, marihuany, nikotyny i NLPZ (tabela 2). W przypadku nikotyny i leków z grupy NLPZ nieproporcjonalnie duże obawy dotyczące szkód fizycznych (np. nowotwory, udar, choroba wieńcowa, POChP w przypadku tych pierwszych oraz krwawienia z przewodu pokarmowego, choroby nerek i układu krążenia w przypadku tych drugich) prawdopodobnie wyjaśniają większość rozbieżności w przypadku tych substancji. W przypadku konopi indyjskich w literaturze niemieckiej panuje obecnie powszechne przekonanie o stosunkowo niskiej szkodliwości fizycznej i odwrotnie – o wysokiej szkodliwości psychospołecznej dla osób używających tych substancji, a ta dychotomia potwierdza występujące tu rozbieżności (29-31). Rozbieżność w przypadku nikotyny (a być może także w pewnym stopniu w przypadku propofolu) może wynikać częściowo z niespodziewanie niskiej oceny szkód psychicznych u użytkowników, która odbiega od dowodów empirycznych. To potencjalne niedoszacowanie może zatem zagrozić ważności ogólnych rankingów szkód dla tych konkretnych substancji.
Gdy alternatywnie użyliśmy opartych na konsensusie wag z badania rankingowego UE (10) jako testu wrażliwości porównawczej, stwierdziliśmy, że wynikowy ranking ogólnych szkód (uzupełniająca rycina 9) był bardzo podobny do naszych rankingów ważonych uzyskanych w badaniu ankietowym przedstawionych na rycinie 1 (dla porównania zob. uzupełniająca tabela 2). Sugeruje to, że odstające/skośne wagi poszczególnych wymiarów (Tabela uzupełniająca 1) nie mają krytycznego wpływu na wynikowe ogólne rankingi szkód w naszym badaniu.
Dyskusja
Nasze dane potwierdzają występującą w wielu innych krajach (5-10) sytuację rozbieżności między eksperckimi rankingami szkód popularnych narkotyków i ich regulacjami prawnymi dotyczącymi narkotyków, co jest najbardziej widoczne w przypadku oceny alkoholu – uznawanego za jedną z najbardziej szkodliwych substancji nadużywanych w naszym kraju. Stosunkowo wysokie rozpowszechnienie używania/nadużywania alkoholu (w porównaniu z rzadziej używanymi, ale być może bardziej niebezpiecznymi substancjami) prawdopodobnie wpływa na jego ocenę w poszczególnych wymiarach, np. szkody dla innych, a także na jego ogólną pozycję. Podobnie malejące rozpowszechnienie używania nikotyny w Niemczech (ponieważ w ciągu ostatnich około 10 lat palenie tytoniu zostało zakazane w wielu miejscach publicznych, takich jak szpitale, placówki edukacyjne, transport publiczny, restauracje, puby i dyskoteki) może przyczynić się do niższej niż oczekiwano oceny szkodliwości. Ponadto należy wspomnieć, że używanie nikotyny, pomimo jej zdolności do wywoływania znacznej zależności behawioralnej, nie wiąże się z dramatycznymi skutkami psychiatrycznymi, np. w przeciwieństwie do używania alkoholu lub halucynogenów. Niniejsze badanie było pierwszym, w którym porównano szkody powodowane przez różne NOAs ze szkodami powodowanymi przez dobrze scharakteryzowane substancje nadużywane i zgodnie z oczekiwaniami stwierdzono, że szkody powodowane przez NOAs są znacznie niższe niż szkody powodowane przez tradycyjne substancje nadużywane. W niniejszym badaniu po raz pierwszy uwzględniono również syntetyczne kannabinoidy i propofol w schemacie klasyfikacji ogólnej szkodliwości, co może być korzystne dla psychoedukacji użytkowników, rozważań regulacyjnych lub określania obszarów działań politycznych na rzecz promocji zdrowia.
NPS (katynony i syntetyczne kannabinoidy) zostały tu przypisane do najwyższej grupy poziomu szkodliwości. Decydenci polityczni i klinicyści skorzystaliby z dalszych danych dotyczących zjawiska NPS, np. związanej z nim zachorowalności (32, 33) i śmiertelności, które mają tendencję wzrostową (33).
W porównaniu z oceną UE z 2014 roku (10), konopie indyjskie, metadon i nikotyna zostały ocenione jako mniej szkodliwe, natomiast crack, metamfetamina, GHB, katynony, ecstasy i grzyby psychotropowe były postrzegane jako bardziej szkodliwe (wykres 3). Konopie indyjskie i halucynogeny (tj. ketaminę, grzyby psychotropowe i LSD) uznano za substancje o szkodliwości zbliżonej do benzodiazepin lub barbituranów. Należy wspomnieć, że psylocybina (na wykresie 1 wymieniona jako grzyby psychotropowe) i LSD cieszą się ponownie odkrytym potencjałem terapeutycznym w chorobach psychiatrycznych i wydają się wykazywać niski potencjał nadużywania w tym kontekście (34).
Interesujące jest to, że opioidowe leki przeciwbólowe nie znalazły się w czołówce szkodliwych leków. Może to być związane z faktem, że „epidemia opioidowa” (taka jak w USA, Kanadzie i Australii) nie jest jeszcze widoczna w Niemczech ani w Europie Zachodniej (35-38). Stosunkowo niska szkodliwość opioidów wydawanych na receptę w naszym badaniu stoi w jaskrawej sprzeczności z wysokim poziomem stygmatyzacji nielegalnych opioidów. Wyniki te są zgodne z wielodecyzyjną analizą dziewięciu ekspertów (8 z Wielkiej Brytanii i 1 z Holandii) sugerującą, że ogólne szkody związane z opioidami wydawanymi na receptę i stosowanymi niemedycznie są o ponad połowę mniejsze niż w przypadku wstrzykiwanej heroiny ulicznej (39).
Metadon oceniono jako mniej szkodliwy niż standardowe opioidowe leki przeciwbólowe, przy czym ten punkt widzenia może być zniekształcony przez postrzeganie przez lekarzy zajmujących się medycyną uzależnień metadonu przede wszystkim jako standardowego leczenia podtrzymującego uzależnienie od opioidów, które w tym kontekście wielokrotnie wykazywało zmniejszenie zachorowalności i śmiertelności (15). W kontekście nielegalnego używania i nadużywania, szkody związane z metadonem (np. zgony w wyniku bezdechu i torsades-de-pointe, uzależnienie i przekierowanie) są oczywiście znacznie wyższe niż szkody związane z kilkoma innymi lekami, które znalazły się na wyższej pozycji. Obnaża to poważne ograniczenie badań dotyczących rankingu szkodliwości leków opartych na subiektywnych ocenach, ponieważ mogą one nie pozwalać na wyraźne rozróżnienie szkodliwości leku ze wskazaniami terapeutycznymi w kontekście medycznym i nielegalnego używania/niedozwolonego używania poza tym kontekstem. Te rozbieżności w rankingu leków przeciwbólowych wśród innych środków sugerują, że być może należało również zbadać doświadczenie oceniających w zakresie medycyny bólu.
Nie można wykluczyć, że nasze oceny mogą być tendencyjnie ukierunkowane na postrzeganie szkód związanych z używaniem substancji w miastach, a nie na wsi; wyjaśnienie tego wymagałoby dalszych badań na większych próbach. Nie zbadano tu również jednoznacznie możliwego wpływu płci na postrzeganie szkód związanych z używaniem narkotyków (40, 41). Ponieważ rozesłaliśmy kwestionariusze bez śledzenia wszystkich odbiorców, prosząc o przekazanie ich innym niemieckim ekspertom w dziedzinie medycyny uzależnień, nie jesteśmy w stanie podać informacji na temat dokładnej liczby ekspertów, którzy ostatecznie otrzymali nasze kwestionariusze. Taki modus operandi nie jest jednak rzadkością w tego typu badaniach (5). Inne ograniczenia, podobne do poprzednich badań (5-10) obejmują fakt, że niniejsza praca nie może twierdzić, że spełnia ścisłe wymagania dotyczące reprezentatywności. Staraliśmy się ograniczyć subiektywizm poprzez rekrutację dużej i jednorodnej grupy badawczej (wszyscy lekarze specjalizujący się w medycynie uzależnień). Nie ma jednak oficjalnych statystyk określających, ilu specjalistów z ponad 5-letnim doświadczeniem w leczeniu SUD pracowało w Niemczech w czasie przeprowadzania badania. Szacujemy, że liczba ta mieści się w przedziale od 250 do 500 lekarzy, dlatego też nasza próba może dawać obraz mniejszości. W Niemczech ekspertami w dziedzinie medycyny uzależnień są zazwyczaj psychiatrzy lub lekarze ogólni. W przeciwieństwie do badań angielskich (5), unijnych (10) i australijskich (9), nie korzystaliśmy z informacji zwrotnych dotyczących konsensusu. Chociaż ten dodatkowy krok mógł zwiększyć prawdopodobieństwo porozumienia uczestników badania (42), zrezygnowaliśmy z niego, ponieważ decyzje oparte na konsensusie same w sobie nie eliminują subiektywności (43) i nie istnieje „uniwersalna metoda” oceny korzyści i ryzyka (44). Co więcej, wcześniejsze badania oparte na konsensusie wykorzystywały mniejsze próby składające się z ekspertów w dziedzinie uzależnień reprezentujących różne zawody (5, 9, 10), których heterogeniczność doświadczeń w leczeniu SUD bardziej prawdopodobnie wymagała strategii decyzyjnej opartej na konsensusie niż nasza jednorodna grupa. Podobnie jak holenderskie (6), szkockie (7) i francuskie grupy badawcze (8) przeprowadziliśmy ocenę „ad-hoc”, wykorzystując zwalidowane wymiary zdrowotne i społeczne, które były wykorzystywane w poprzednich (5, 10) i ostatnich (9) badaniach empirycznych. Ta decyzja o zastosowaniu formatu „ad-hoc” zmaksymalizowała zwrot wypełnionych kwestionariuszy.
Oprócz nowatorskiego włączenia NOAs, syntetycznych kannabinoidów i propofolu, istnieje kilka mocnych stron obecnego badania: (i) wykorzystanie jednej z największych prób w tego typu badaniach; (ii) znaczne wielowymiarowe doświadczenie uczestników w zakresie medycyny uzależnień, w tym doświadczenie specjalistów z klinik rehabilitacyjnych (ryc. 2), które w Niemczech w dużym stopniu koncentruje się na wymiarach i wynikach psychospołecznych; (iii) porównanie z poprzednią klasyfikacją UE (ryc. 3); oraz (iv) dodanie do obecnej literatury porównań rankingów nielegalnych i legalnych narkotyków.
Wyniki tego przekrojowego badania kwestionariuszowego stanowią aktualizację średnich ogólnych szkód (ze szkodami składowymi w różnych wymiarach zdrowotnych i społecznych) wynikających z używania/nieużywania różnych substancji psychoaktywnych (w tym leków przeciwbólowych wydawanych na receptę) z perspektywy niemieckich specjalistów medycyny uzależnień. Należy jednak podkreślić, że te względne rankingi ogólne dotyczą zagrożeń na poziomie populacji, a w zależności od kontekstu indywidualnego i sytuacyjnego, jak również od intensywności indywidualnego nadużywania, prawie każda substancja psychoaktywna może być używana w bardzo niebezpieczny i szkodliwy sposób.
Podsumowanie
W niniejszym opracowaniu przedstawiono zaktualizowany ranking niemieckich ekspertów medycyny uzależnień dotyczący średnich szkód ogólnych, jak również szkód w poszczególnych wymiarach zdrowotnych i społecznych związanych z używaniem różnych substancji psychoaktywnych, w tym leków przeciwbólowych. Oceniono, że alkohol należy do najbardziej szkodliwych substancji uzależniających, obok heroiny, kokainy, metamfetaminy, GHB i NPS (tj. syntetycznych kannabinoidów, katynonów). Podwyższone ryzyko związane z alkoholem stoi w pewnej sprzeczności z niemieckim prawem narkotykowym, podobnie jak w większości krajów. Konopie indyjskie i ketamina znalazły się w połowie stawki, na równi z benzodiazepinami. Leki stosowane terapeutycznie, takie jak nieopioidowe leki przeciwbólowe, metylofenidat i opioidy, oceniono jako ogólnie najmniej szkodliwe w chwili obecnej. Takie względne postrzeganie bezpieczeństwa może jednak ulec zmianie, jeśli wzorce niewłaściwego stosowania i nadużywania zmienią się z czasem (45).
Oświadczenie o dostępności danych
Surowe dane potwierdzające wnioski zawarte w tym artykule zostaną udostępnione przez autorów bez zbędnych zastrzeżeń.
Oświadczenie o etyce
Badania z udziałem ludzi zostały przejrzane i zatwierdzone przez Ethik-Kommission der Medizinischen Fakultät der Universität Duisburg-Essen. Pisemna świadoma zgoda na udział nie była wymagana w tym badaniu zgodnie z ustawodawstwem krajowym i wymogami instytucjonalnymi.
Wkład autorów
UB: koncepcja i projekt. MSp: analiza danych. UB i MSp: zbieranie i interpretacja danych. UB: redagowanie artykułu. All authors: revising it criticly for important intellectual content.
Konflikt interesów
NS otrzymał honoraria za szereg działań (np. członkostwo w radach doradczych, wykłady, manuskrypty) od firm AbbVie, Camurus, Hexal, Janssen-Cilag, MSD, Medice, Mundipharma, Reckitt-Benckiser/Indivior i Sanofi-Aventis. W ciągu ostatnich 3 lat brał udział w badaniach klinicznych finansowanych przez przemysł farmaceutyczny. TA otrzymywał honoraria (np. członkostwo w komitetach doradczych) i/lub granty edukacyjne od firm Janssen-Cilag, Medice i Otsuka-Lundbeck NW otrzymywał honoraria za wykłady (niezwiązane z produktem) (Janssen-Cilag, mundipharma i Reckitt-Benckiser/Indivior), W ciągu ostatnich 3 lat uczestniczył w badaniach klinicznych finansowanych przez przemysł farmaceutyczny i otrzymał finansowanie publiczne (BayStMGP) na ocenę Take-Home Naloxone. TH otrzymywał honoraria za szereg działań (np. członkostwo w radach doradczych, wykłady) od firm Janssen-Cilag, Amomed, Shire, Takeda, Servier MSo pracował jako konsultant lub otrzymywał honoraria od firm Ammomed, Indivior, Camurus przez ostatnie 3 lata. JR otrzymywał honoraria za udział w radach doradczych, konsultacje i wykłady od AbbVie, Camurus, Gilead, Hexal, Indivior i Sanofi-Aventis. JK otrzymał honoraria od firm Bayer, Janssen, Lundbeck, Neuraxpharm, Otsuka Pharma, Schwabe i Servier za wygłaszanie wykładów na konferencjach oraz wsparcie finansowe na podróże. Otrzymywał wsparcie finansowe dla badań inicjowanych przez badaczy od firmy Medtronic GmbH. HM jest również związany z prywatną praktyką (Northern Anesthesia; Pain Medicine, LLC, Eagle River, AK, USA), która nie ma związku z tym badaniem.
Pozostali autorzy deklarują, że badania były prowadzone przy braku jakichkolwiek komercyjnych lub finansowych powiązań, które mogłyby być interpretowane jako potencjalny konflikt interesów.
Podziękowania
Serdecznie dziękujemy Jennifer Haverkemper, MSc (psychologia), za pomoc w opracowaniu kwestionariusza dla kohorty 1, oraz Ann-Christin Kanti, MD, za wprowadzenie i utrzymanie danych. Dziękujemy również Gabriele Lührmann, głównej sekretarce Wydziału Psychiatrii, Psychoterapii i Psychosomatyki w EVK Castrop-Rauxel za organizację korespondencji z kolegami. Dziękujemy również wielu lekarzom, którzy uprzejmie poświęcili swój czas na udział w tym projekcie.
Materiały uzupełniające
Materiały uzupełniające do tego artykułu można znaleźć online pod adresem: https://www.frontiersin.org/articles/10.3389/fpsyt.2020.592199/full#supplementary-material
1. Korpi ER, den Hollander B, Farooq U, Vashchinkina E, Rajkumar R, Nutt DJ, et al. Mechanisms of action and persistent neuroplasticity by drugs of abuse. Pharmacol Rev. (2015) 67:872-1004. doi: 10.1124/pr.115.010967
CrossRef Full Text | Google Scholar
2. Morgen K. Counseling and Professional Identity in the 21st Century. Substance use Disorders and Addictions. Thousand Oaks, CA: Sage Publications, Inc (2017).
Google Scholar
3. APA American Psychiatric Association. Diagnostic and Statistical Manual of Mental Disorders (Diagnostyczny i statystyczny podręcznik zaburzeń psychicznych). 5th ed. Washington, DC: APA (2013).
Google Scholar
4. Dilling H, Freyberger H. Taschenführer zur ICD-10-Klassifikation psychischer Störungen. Bern: Huber Verlag (2006).
Google Scholar
5. Nutt DJ, King LA, Phillips LD. Niezależny Komitet Naukowy ds. Narkotyków. Szkodliwość narkotyków w Wielkiej Brytanii: wielokryterialna analiza decyzyjna. Lancet. (2010) 376:1558-65. doi: 10.1016/S0140-6736(10)61462-6
CrossRef Full Text | Google Scholar
6. van Amsterdam J, Opperhuizen A, Koeter M, van den Brink W. Ranking the harm of alcohol, tobacco and illicit drugs for the individual and the population. Eur Addict Res. (2010) 16:202-7. doi: 10.1159/000317249
CrossRef Full Text | Google Scholar
7. Taylor M, Mackay K, Murphy J, McIntosh A, McIntosh C, Anderson S, et al. Quantifying the RR of harm to self and others from substance misuse: results from a survey of clinical experts across Scotland. BMJ Open. (2012) 2:e000774. doi: 10.1136/bmjopen-2011-000774
CrossRef Full Text | Google Scholar
8. Bourgain C, Falissard B, Blecha L, Benyamina A, Karila L, Reynaud M. A damage/benefit evaluation of addictive product use. Addiction. (2012) 107:441-50. doi: 10.1111/j.1360-0443.2011.03675.x
CrossRef Full Text | Google Scholar
9. Bonomo Y, Norman A, Biondo S, Bruno R, Daglish M, Dawe S, et al. The Australian drug harms ranking study. J Psychopharmacol. (2019) 33:759-68. doi: 10.1177/0269881119841569
CrossRef Full Text | Google Scholar
10. van Amsterdam J, Nutt D, Phillips L, van den Brink W. European rating of drug harms. J Psychopharmacol. (2015) 29:655-60. doi: 10.1177/0269881115581980
CrossRef Full Text | Google Scholar
11. DSB (Drogen und Suchtbericht 2018). Die Drogenbeauftragte der Bundesregierung. (2018). Dostępne online na: https://www.drogenbeauftragte.de/fileadmin/dateien-dba/Drogenbeauftragte/Drogen_und_Suchtbericht/pdf/DSB-2018.pdf (dostęp 6 stycznia 2020 r.).
Google Scholar
12. Atzendorf J, Rauschert C, Seitz N, Lochbühler K, Kraus L. The use of alcohol, tobacco, illegal drugs and medicines. Szacunkowe dane dotyczące konsumpcji i zaburzeń związanych z używaniem substancji w Niemczech. Dtsch Arztebl Int. (2019) 116:577-84. doi: 10.3238/arztebl.2019.0577
CrossRef Full Text | Google Scholar
13. Seitz NN, Lochbühler K, Atzendorf J, Rauschert C, Pfeiffer-Gerschel T, Kraus L. Trendy w używaniu substancji i zaburzeniach pokrewnych-analiza badania epidemiologicznego dotyczącego nadużywania substancji 1995 do 2018. Dtsch Arztebl Int. (2019) 116:585-91. doi: 10.3238/arztebl.2019.0585
CrossRef Full Text | Google Scholar
14. Scherbaum N, Schifano F, Bonnet U. Nowe substancje psychoaktywne (NPS) – wyzwanie dla służb zajmujących się leczeniem uzależnień. Pharmacopsychiatry. (2017) 50:116-22. doi: 10.1055/s-0043-102059
CrossRef Full Text | Google Scholar
15. Dematteis M, Auriacombe M, D’Agnone O, Somaini L, Szerman N, Littlewood R, et al. Recommendations for buprenorphine and methadone therapy in opioid use disorder: a European consensus. Expert Opin Pharmacother. (2017) 18:1987-99. doi: 10.1080/14656566.2017.1409722
CrossRef Full Text | Google Scholar
16. Chandra S, Radwan MM, Majumdar CG, Church JC, Freeman TP, ElSohly MA. New trends in cannabis potency in USA and Europe during the last decade (2008-2017). Eur Arch Psychiatry Clin Neurosci. (2019) 269:5-15. doi: 10.1007/s00406-019-00983-5
CrossRef Full Text | Google Scholar
17. Di Forti M, Quattrone D, Freeman TP, Tripoli G, Gayer-Anderson C, Quigley H, et al. The contribution of cannabis use to variation in the incidence of psychotic disorder across Europe (EU-GEI): a multicentre case-control study. Lancet Psychiatry. (2019) 6:427-36. doi: 10.1016/S2215-0366(19)30048-3
CrossRef Full Text | Google Scholar
18. EMCDDA Europejskie Centrum Monitorowania Narkotyków i Narkomanii. 2018 Medical use of Cannabis and Cannabinoids: Questions and Answers for Policymaking. Luksemburg: Urząd Publikacji Unii Europejskiej (2018). Dostępne online pod adresem: http://www.emcdda.europa.eu/system/files/publications/10171/20185584_TD0618186ENN_PDF.pdf (dostęp 6 stycznia 2020 r.).
Google Scholar
19. Bonnet U. Ocena ryzyka uzależniającego związanego z propofolem. Fortschr Neurol Psychiatry. (2011) 79:442-52. doi: 10.1055/s-0031-1273411
CrossRef Full Text | Google Scholar
20. Beau-Salinas F, Jonville-Béra AP, Cissoko H, Bensouda-Grimaldi L, Autret-Leca E. Drug dependence associated with triptans and ergot derivatives: a case/non-case study. Eur J Clin Pharmacol. (2010) 66:413-7. doi: 10.1007/s00228-009-0769-6
CrossRef Full Text | Google Scholar
21. Gahr M, Freudenmann RW, Connemann BJ, Hiemke C, Schönfeldt-Lecuona C. Abuse liability of flupirtine revisited: implications of spontaneous reports of adverse drug reactions. J Clin Pharmacol. (2013) 53:1328-33. doi: 10.1002/jcph.164
CrossRef Full Text | Google Scholar
22. Evoy KE, Morrison MD, Saklad SR. Nadużywanie i niewłaściwe stosowanie pregabaliny i gabapentyny. Drugs. (2017) 77:403-26. doi: 10.1007/s40265-017-0700-x
CrossRef Full Text | Google Scholar
23. Bonnet U, Scherbaum N. How addictive are gabapentin and pregabalin? A systematic review. Eur Neuropsychopharmacol. (2017) 27:1185-2015. doi: 10.1016/j.euroneuro.2017.08.430
CrossRef Full Text | Google Scholar
24. Bonnet U, Strasser JC, Scherbaum N. Screening for physical and behavioral dependence on non-opioid analgesics in a German elderly hospital population. Addict Behav. (2019) 90:265-71. doi: 10.1016/j.addbeh.2018.11.009
CrossRef Full Text | Google Scholar
25. Etcheverrigaray F, Grall-Bronnec M, Blanchet M, Jolliet P, Victorri-Vigneau C. Ibuprofen dependence: a case report. Pharmacopsychiatry. (2014) 47:115-7. doi: 10.1055/s-0034-1371868
CrossRef Full Text | Google Scholar
26. Godersky ME, Vercammen LK, Ventura AS, Walley AY, Saitz R. Identyfikacja zaburzeń związanych z używaniem niesteroidowych leków przeciwzapalnych: opis przypadku. Addict Behav. (2017) 70:61-4. doi: 10.1016/j.addbeh.2017.02.008
PubMed Abstract | CrossRef Full Text | Google Scholar
27. Cryer B, Barnett MA, Wagner J, Wilcox CM. Nadużywanie i błędne postrzeganie niesteroidowych leków przeciwzapalnych w Stanach Zjednoczonych. Am J Med Sci. (2016) 352:472-80. doi: 10.1016/j.amjms.2016.08.028
CrossRef Full Text | Google Scholar
28. Wójta-Kempa M, Krzyżanowski DM. Correlates of abusing and misusing over-the-counter pain relievers among adult population of Wrocław (Poland). Adv Clin Exp Med. (2016) 25:349-60. doi: 10.17219/acem/58887
CrossRef Full Text | Google Scholar
29. Hölscher F, Bonnet U, Scherbaum N. Zastosowanie ambulatoryjnego centrum leczenia w przypadku nadużywania konopi indyjskich. Nervenarzt. (2008) 79:571-6. doi: 10.1007/s00115-008-2412-7
CrossRef Full Text | Google Scholar
30. Bonnet U, Specka M, Scherbaum N. Częste używanie konopi indyjskich w celach niemedycznych: następstwa zdrowotne i skuteczność leczenia detoksykacyjnego. Dtsch Med Wochenschr. (2016) 141:126-31. doi: 10.1055/s-0041-106313
CrossRef Full Text | Google Scholar
31. Schneider D. Konsumfolgen und Behandlungsbedarf von Cannabis-Intensivkonsumenten/innen im ambulanten setting. Sucht. (2016) 62:23-30. doi: 10.1024/0939-5911/a000405
CrossRef Full Text | Google Scholar
32. Foti F, Marti M, Ossato A, Bilel S, Sangiorgi E, Botrè F, et al. Phenotypic effects of chronic and acute use of methiopropamine in a mouse model. Int J Legal Med. (2019) 133:811-20. doi: 10.1007/s00414-018-1891-8
CrossRef Full Text | Google Scholar
33. Corkery JM, Schifano F, Martinotti G. Jak zgony mogą pomóc klinicystom i decydentom zrozumieć ryzyko związane z nowymi substancjami psychoaktywnymi. Br J Clin Pharmacol. (2020) 86:482-98. doi: 10.1111/bcp.14183
CrossRef Full Text | Google Scholar
34. Chi T, Gold JA. Przegląd wyłaniającego się potencjału terapeutycznego leków psychodelicznych w leczeniu chorób psychiatrycznych. J Neurol Sci. (2020) 411:116715. doi: 10.1016/j.jns.2020.116715
CrossRef Full Text | Google Scholar
35. Häuser W, Schug S, Furlan AD. Epidemia opioidów i krajowe wytyczne dotyczące terapii opioidowej w przewlekłym bólu nienowotworowym: perspektywa z różnych kontynentów. Pain Rep. (2017) 2:e599. doi: 10.1097/PR9.00000000000599
CrossRef Full Text | Google Scholar
36. Kraus L, Seitz NN, Schulte B, Cremer-Schaeffer P, Braun B, Verthein U, et al. Estimation of the number of people with opioid addiction in Germany. Dtsch Arztebl Int. (2019) 116:137-43. doi: 10.3238/arztebl.2019.0137
CrossRef Full Text | Google Scholar
37. Rosner B, Neicun J, Yang JC, Roman-Urrestarazu A. Opioid prescription patterns in germany and the global opioid epidemic: systematic review of available evidence. PLoS ONE. (2019) 14: e0221153. doi: 10.1371/journal.pone.0221153
CrossRef Full Text | Google Scholar
38. Meyer A, LeClair C, McDonald JV. Przepisywanie opioidów na receptę w Europie Zachodniej i Stanach Zjednoczonych. R I Med J. (2020) 103:45-8.
Google Scholar
39. van Amsterdam J, Phillips L, Henderson G, Bell J, Bowden-Jones O, Hammersley R, et al. Ranking the harm of non-medically used prescription opioids in the UK. Regul Toxicol Pharmacol. (2015) 73:999-1004. doi: 10.1016/j.yrtph.2015.09.014
CrossRef Full Text | Google Scholar
40. Bodnar RJ, Kest B. Sex differences in opioid analgesia, hyperalgesia, tolerance and withdrawal: central mechanisms of action and roles of gonadal hormones. Horm Behav. (2010) 58:72-81. doi: 10.1016/j.yhbeh.2009.09.012
CrossRef Full Text | Google Scholar
41. Di Nicola M, Ferri VR, Moccia L, Panaccione I, Strangio AM, Tedeschi D, et al. Gender differences and psychopathological features associated with addictive behaviors in adolescents. Front Psychiatry. (2017) 8:256. doi: 10.3389/fpsyt.2017.00256
PubMed Abstract | CrossRef Full Text | Google Scholar
42. Phillips LD, Banae Costa CA. Transparent prioritisation, budgeting and resource allocation with multi-criteria decision analysis and decision conferencing. Ann Operat Res. (2007) 154:51-68. doi: 10.1007/s10479-007-0183-3
CrossRef Full Text | Google Scholar
43. Rolles S, Measham F. Questioning the method and utility of ranking drug harms in drug policy. Int J Drug Policy. (2011) 22:243-6. doi: 10.1016/j.drugpo.2011.04.004
CrossRef Full Text | Google Scholar
44. Mt-Isa S, Hallgreen CE, Wang N, Callréus T, Genov G, Hirsch I, Hobbiger SF, et al. Balancing benefit and risk of medicines: a systematic review and classification of available methodologies. Pharmacoepidemiol Drug Saf . (2014) 23:667-78. doi: 10.1002/pds.3636
PubMed Abstract | CrossRef Full Text | Google Scholar
45. Martinotti G, de Risio L, Vannini C, Schifano F, Pettorruso M, Di Giannantonio M. Substance related exogenous psychosis: a post-modern syndrome. CNS Spectr. (2020) 1-8. doi: 10.1017/S1092852920001479
CrossRef Full Text | Google Scholar
.