- trans-Cinnamaldehyde Chemische Eigenschappen, Gebruiken, Productie
- Overzicht
- Pharmacokinetiek
- Toepassingen
- Toxiciteit
- Chemische eigenschappen
- Chemische eigenschappen
- Chemische eigenschappen
- Definitie
- Syntheseverwijzing(en)
- Algemene beschrijving
- Air & Waterreacties
- Reactiviteitsprofiel
- Vuurgevaar
- Mogelijke blootstelling
- Verlading
- Onverenigbaarheden
- Verwijdering van afval
trans-Cinnamaldehyde Chemische Eigenschappen, Gebruiken, Productie
Overzicht
Cinnamaldehyde, een oude smaakstof afkomstig van kaneelbomen en andere soorten van het geslacht Cinnamomum, is nu in toenemende mate in de belangstelling gekomen vanwege zijn vermogen om de ontwikkeling van diabetes en de complicaties daarvan te voorkomen. Cinnamaldehyde, een gele en viskeuze vloeistof, maakt 98% uit van de essentiële olie van kaneelschors, en werd voor het eerst geïsoleerd door Dumas en Péligot en vervolgens in 1854 in het laboratorium gesynthetiseerd door de Italiaanse chemicus Luigi Chiozza (1828-1889). In 2007 meldden Subash et al. voor het eerst een hypoglycemisch en hypolipidemisch effect van cinnamaldehyde op streptozotocine (STZ)-geïnduceerde mannelijke diabetische Wistar-ratten. Cinnamaldehyde is sindsdien uitvoerig bestudeerd in diermodellen voor diabetes en zwaarlijvigheid.
Cassia of Chinese kaneel is een veelgebruikte specerij die wordt gewonnen uit de binnenbast van de kaneelboom. Cassia wordt al duizenden jaren voor medicinale doeleinden gebruikt en wordt beschouwd als een van de 50 basiskruiden in de traditionele Chinese geneeskunde. Verschillende delen van de kassiaplant worden voor medicinale doeleinden gebruikt, waaronder de wortel, de schors, de bladeren en de bloemen. Van kaneelextracten is bekend dat zij diverse gunstige effecten hebben, waaronder anti-allergene, antimicrobiële, antivirale, antioxidatieve, gastroprotectieve, antiangiogene en anti-Alzheimer effecten, alsmede insuline-achtige biologische activiteiten . Kaneelextracten bevatten verschillende actieve bestanddelen, waaronder etherische oliën (cinnamaldehyde en cinnamylaldehyde), tanninen, slijm en koolhydraten. Interessant is dat cinnamaldehyde, ook bekend als cinnamylaldehyde, anti-obesitas effecten vertoont door lipidenophoping te verminderen en de peroxisome proliferator-activated receptor-γ, CCAAT/enhancer-binding protein α, en sterol regulatory element-binding protein 1 te downreguleren. Bovendien remt cinnamaldehyde lipopolysaccharide-geïnduceerde microgliale activering door het low-density lipoprotein receptor-related protein-1 aan te pakken. Ook werd gemeld dat kaneelaldehyde antimutagene effecten heeft in kankercellen.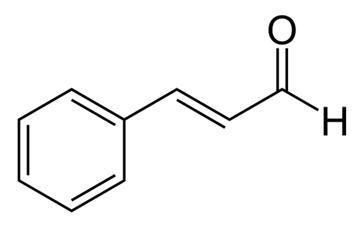
Figuur 1 de chemische structuur van kaneelaldehyde;
Pharmacokinetiek
Kaneelaldehyde bestaat van nature in de vorm van trans-cinnamaldehyde. In een experiment uitgevoerd door Zhao et al. wordt de farmacokinetiek van cinnamaldehyde bij ratten geëvalueerd met behulp van de relatief gevoelige benadering van gaschromatografie-massaspectrometrie (GC-MS) via orale (500 mg/kg) en intraveneuze injectie (i.v., 20 mg/kg) toediening. Uit de resultaten blijkt dat de AUC0-t van cinnamaldehyde via orale toediening en via i.v. toediening respectievelijk 1984 ± 531 en 355 ± 53 ng h/ml bedraagt. De T1/2 en Tmax van kaneelaldehyde zijn langer bij orale toediening (6,7 ± 1,5 uur en 1,6 ± 0,5 uur) dan bij i.v.-toediening (1,7 ± 0,3 uur en 0,033 uur). De Cmax is respectievelijk 249±36 ng/ml voor orale toediening, en 547±142 ng/ml voor i.v. toediening. De resultaten wijzen erop dat de biologische beschikbaarheid van cinnamaldehyde beter is bij i.v. toediening dan bij orale toediening.
Verder tonen de auteurs aan dat Cmax en AUC0-t evenredig zijn met de dosis (van 125 tot 500 mg), terwijl Tmax en gemiddelde verblijftijd niet veranderen als reactie op dosisescalatie. Aangezien cinnamaldehyde en cinnamylalcohol in ratten in elkaar kunnen overgaan, analyseren de auteurs ook de farmacokinetische eigenschappen van cinnamylalcohol in rattenplasma. De farmacokinetische gegevens van cinnamylalcohol zijn 1105±337 ng-h/ml voor AUC0-t, 6,7±2,8 h voor T1/2, 1,5±0,7 h voor Tmax, en 221±66 ng/ml voor Cmax, bij een orale dosering van 500 mg/kg. Interessant is dat methylcinnamaat ook in de metabolieten is ontdekt. Voor de farmacokinetische eigenschappen van methylcinnamaat worden geïnteresseerde lezers aangemoedigd het artikel van Zhao et al. te raadplegen. Kortom, cinnamaldehyde wordt na absorptie goed verdeeld in het lichaam. Cinnamaldehyde heeft een mogelijkheid om te transformeren in cinnamyl alcohol en kan ook worden geoxideerd tot kaneelzuur nadat het in het lichaam is gekomen. Om de farmacokinetische eigenschappen van cinnamaldehyde volledig te begrijpen, moeten ook methylcinnamaat en cinnamylalcohol in het plasma worden bepaald. De instabiliteit van cinnamaldehyde doet echter betwijfelen of de bioactiviteit van cinnamaldehyde waarschijnlijk te danken is aan de som van zijn metabolieten. Daarom wordt verwacht dat verdere pogingen zullen worden ondernomen om deze potentiële bezorgdheid weg te nemen. Bovendien moet het nieuw ontwikkelde KMO-cinnamaldehyde met verbeterde biologische beschikbaarheid ook verder onderzocht worden op zijn anti-diabetische werking.
Toepassingen
Kaneelextracten hebben verschillende gunstige effecten, waaronder anti-allergene, antimicrobiële, antivirale, antioxidatieve, gastroprotectieve, antiangiogene en anti-Alzheimer effecten, evenals insuline-achtige biologische activiteiten. Cinnamaldehyde vertoont anti-obesitas effecten door vermindering van lipide accumulatie en downregulering van de peroxisome proliferator-activated receptor-γ, CCAAT/enhancer-binding protein α, en sterol regulatory element-binding protein 1. Verder remt cinnamaldehyde lipopolysaccharide-geïnduceerde microgliale activering door targeting van de low-density lipoprotein receptor-related protein-1. Er werd ook gemeld dat kaneelaldehyde antimutagene effecten heeft in kankercellen. Het effect van kaneelaldehyde op de behandeling van kanker en diabetes wordt hieronder belicht:
Antikanker
Kwon et al. meldden voor het eerst dat kaneelextracten in vitro en in vivo de dood van melanoomcellen induceren door de remming van NF-κB en AP-1. Uit een latere studie bleek dat HCA de belangrijkste antitumorigene stof in kaneelextracten is, met een groeiremmende werking op 29 soorten menselijke kankercellen in vitro en op SW620 menselijke tumorxenograften in vivo.
Andere onderzoeksteams hebben ook antitumorigene effecten van kaneelextracten gemeld. Zij remmen melanoomkankercellen door de expressie van pro-angiogene factoren te induceren; zij verbeterden ook de antitumorigene activiteiten van CD8 T-cellen door hun cytolytische activiteit te verhogen. Kaneelextracten remmen ook de vasculaire endotheliale groeifactor, hetgeen werd ontdekt door verbindingen te screenen op hun remmende activiteit tegen VEGFR2. De meeste antitumorigene effecten van kaneelextracten kunnen worden toegeschreven aan cinnamaldehyden, het hoofdbestanddeel van de etherische olie, die verantwoordelijk is voor de smaak en het aroma van de hele kaneel. Er werd gerapporteerd dat kaneelamaldehyden de proliferatie van kankercellen remden door het remmen van cycline D1 in verschillende soorten tumoren. Kaneelaldehyden induceren ook apoptose door het genereren van reactieve zuurstofsoorten in HL-60 leukemiecellen en door activering van pro-apoptotische Bcl-2-familie-eiwitten en de MAPK-signaalroute in menselijke hepatoomcellen. Bovendien vertoonden dimere kaneelaldehyden van HCA een grotere antitumorigene werking dan monomere kaneelaldehyden door apoptose en celcyclusstilstand te induceren. Bovendien is uit een aantal studies gebleken dat de antitumorigene effecten van HCA en zijn derivaten via verschillende moleculaire mechanismen tot stand komen. Een recente studie toonde aan dat polyfenolen met een cinnamaldehyde scaffold celcyclusarrest in de G2/M fase en apoptotische celdood in cisplatine-resistente menselijke eierstokkankercellen teweegbrachten, wat suggereert dat cinnamaldehyde verbindingen effectief zouden kunnen zijn in combinatiechemotherapieën voor kankerpatiënten. In het algemeen zijn de moleculaire mechanismen die ten grondslag liggen aan de antikanker en antimetastatische effecten van cinnamaldehyden divers, wat suggereert dat cinnamaldehyde een multitargeting verbinding is. De differentiële respons van verschillende kankers op verschillende cinnamaldehyderivaten moet geëvalueerd worden om de selectie van de meest doeltreffende verbinding voor elk kankertype mogelijk te maken.
Anti-diabetes
Er zijn de laatste decennia steeds meer studies uitgevoerd om de gunstige rol van cinnamaldehyde bij de behandeling van diabetes en zijn complicaties te evalueren. Aangetoond is dat orale toediening van cinnamaldehyde variërend van 20 mg/kg lichaamsgewicht tot 40 mg/kg lichaamsgewicht per dag gedurende een periode van 21 tot 60 dagen resulteerde in een aanzienlijke verbetering van de bloedglucosewaarden en geglycosyleerde hemoglobinespiegels, evenals van de insulinegevoeligheid bij STZ-geïnduceerde diabetische ratten. En 20 mg/kg lichaamsgewicht wordt verondersteld de effectieve dosis te zijn om de ontwikkeling van diabetes bij dieren te voorkomen. Verder verhoogt behandeling met cinnamaldehyde gedurende 4 weken de plasma-insulinespiegel en het leverglycogeengehalte, en verlaagt het triglyceriden- en lagedichtheid-lipoproteïne-cholesterolgehalte bij met STZ en/of HFD besmette mannelijke Wistar-ratten. Verder ontdekten Camacho et al. dat toediening van cinnamaldehyde gedurende 5 weken aan met HFD gevoede C57BL/6J muizen aanzienlijk leidde tot een vermindering van de toename van de vetmassa in het lichaam. Zij stelden echter dat de behandeling met cinnamaldehyde de nuchtere insulinespiegel in het plasma en de voederconsumptie niet veranderde. De reden voor de inconsistentie met betrekking tot de insulineregulatie zou kunnen worden toegeschreven aan het feit dat de genetische achtergrond van C57BL/6J-muizen in sommige productiefaciliteiten is gewijzigd. De verschillende substammen van muizen kunnen aanzienlijke verschillen in fenotype vertonen. Bovendien kan cinnamaldehyde in de studie van Camacho een glucoseverlagend effect vertonen door de insulinegevoeligheid in de periferie te verbeteren.
Cinnamaldehyde heeft het vermogen om diabetisch vetweefsel te verbeteren door viscerale vetafzetting te verminderen, en lipolyse en vetzuuroxidatie en thermogenese te bevorderen, wat gepaard gaat met een upregulatie van energie-uitgavengenen, een remming van PPARγ/CEBP-α en SREBP1, een opregulatie van HSL en PNPLA2 en MGL, een inductie van AMPK-fosforylering, en een toename van Cpt1a in WAT en Acsl4 in BAT, alsmede een stimulering van het sympathische zenuwstelsel. Bovendien voorkomt cinnamaldehyde de expressie van ontstekingsgenen, en verbetert het de expressie van GLUTs in diabetische dieren. Cinnamaldehyde kan beschermen tegen diabetes door de insulinegevoeligheid en de glucoseopname te verbeteren door de PI3K/IRS-1 en RBP4-GLUT4 route in skeletspierweefsel te reguleren, en door het mitochondriaal metabolisme te reguleren via de PGC-1α/MEF2/GLUT4 route in C2C12 cellen. Cinnamaldehyde heeft ook positieve effecten op de diabetische lever door verbetering van de glycogeensynthese door regulering van de activiteiten van PK en PEPCK en verlaging van het RBP4-niveau, evenals het normaliseren van de afwijkende leverenzymen, wat wijst op een gunstige rol van deze verbinding in het glucosemetabolisme en de insulinegevoeligheid in de diabetische lever.
Antimicrobiële effecten
Studies hebben de antimicrobiële activiteit van cinnamaldehyde, kruidnagel, tijm en rozemarijn tegen E. coli O157:H7 en Salmonella bevestigd. Wendakoon en Sakaguchi meldden dat de carbonylgroep van kaneelaldehyde zich bindt aan de eiwitten, waardoor de aminozuurdecarboxylase-activiteit in Enterobacter aerogenes wordt verhinderd. Smid et al. constateerden dat het cytoplasmamembraan van Saccharomyces cerevisiae beschadigd raakt wanneer het met kaneelaldehyde wordt behandeld, wat leidt tot overmatige lekkage van metabolieten en enzymen uit de cel en uiteindelijk tot verlies van levensvatbaarheid. De meeste studies hebben gesuggereerd dat de werkingsmechanismen van etherische oliën afhankelijk zijn van het soort micro-organisme, voornamelijk van hun celwandstructuur en van de opstelling van hun buitenmembraan. Zij constateerden schade door de aanzienlijke verschillen in de buitenmembranen van gram-negatieve en gram-positieve bacteriën.
Toxiciteit
Zelfs nu nog wordt cinnamaldehyde verondersteld een veilig natuurlijk ingrediënt te zijn dat bij mens en dier goed wordt verdragen. Het concept wordt ook goed aanvaard door de FDA en de Raad van Europa met de suggestie van de aanvaardbare dagelijkse inname van 1,25 mg/kg.
Aute toxiciteit
Cinnamaldehyde zou een hoge veiligheidsmarge hebben, en toegediend 20 keer de effectieve dosis (20 mg/kg) van deze verbinding veroorzaakte geen abnormale gedragstekenen en verstoorde de serumchemische waarden gedurende de studie. De acute toxiciteit van kaneelaldehyde is laag, met orale mediane letale dosis (LD50) waarden variërend van een dieptepunt van 0,6 g/kg BW tot een hoogtepunt van 3,4 g/kg BW bij verschillende diersoorten.
Lange-termijn toxiciteit
De resultaten van een drie maanden durend onderzoek tonen aan dat het lichaamsgewicht vermindert bij vrouwelijke ratten blootgesteld aan 16.500 of 33.000 ppm en bij vrouwelijke muizen blootgesteld aan 8200 ppm of meer. Bovendien is de voedselconsumptie verminderd in alle blootgestelde groepen ratten en in de hoogste dosisgroep muizen. Verder verhoogt blootstelling aan cinnamaldehyde de incidentie van squameuze epitheliale hyperplasie van de voormaag. Bovendien vertonen muizen die aan cinnamaldehyde zijn blootgesteld een verhoogde incidentie van olfactorische epitheliale degeneratie van de neusholte. Alle ratten overleefden gedurende de studie van drie maanden.
Anderen
Cinnamaldehyde kan ook cytotoxische effecten vertonen in hepatocyten van F344 ratten, wat blijkt uit het uitputten van het glutathiongehalte, en in HepG2-cellen, wat blijkt uit het toenemend aantal micronucleus. Behar et al. onderzochten de potentiële toxiciteit van dit product in menselijke embryonale cellen en longcellen. De resultaten tonen aan dat de behandeling met kaneelaldehyde de microtubuli in menselijke longfibroblasten depolymeriseert. Cinnamaldehyde vermindert ook de celproliferatie en -differentiatie door de celgroei en -differentiatie te remmen, de celmorfologie en -motiliteit te veranderen en de DNA-strengbreuken en celdood te doen toenemen. Uit een studie van Olsen et al. blijkt dat cinnamaldehyde huidirriterend werkt door de pijndrempel bij koude te verhogen en de mechanische pijndrempel te verlagen, alsook door de huidtemperatuur en de doorbloeding bij de mens te verhogen.
- Zhou M, Chen Z, Shen S. Recent advanceson cinnamaldehyde. Journal of Economic Animal 2015;19:1-5.
- Khare P, Jagtap S, Jain Y, Baboota RK, Mangal P, Boparai RK, Bhutani KK, Sharma SS, Premkumar LS, Kondepudi KK, Chopra K, Bishnoi M. Cinnamaldehyde suppletie voorkomt vasten-geïnduceerde hyperfagie, lipide accumulatie, en ontsteking in hoog-vet dieet-gevoede muizen. BioFactors 2016;42:201-211.
- Ma R, Zhu R, Wang L, Guo Y, Liu C, Liu H, Liu F, Li H, Li Y, Fu M, Zhang D. Diabetische osteoporose: A review of its traditional chinese medicinal use and clinical and preclinical research. Evidence-based complementaire en alternatieve geneeskunde : eCAM 2016;2016:3218313.
- Dumas JP, E. Organisch chemisch onderzoek – naar kaneelolie, het hippurinezuur en sebacinezuur. Annales de chimie et de physique 1834;57:305-334.
- Chiozza L. Sur la production artificielle de l´essence de cannelle”. Comptes rendus 1856;42:222-227.
- Subash Babu P, Prabuseenivasan S, Ignacimuthu S. Cinnamaldehyde–een potentieel antidiabetisch middel. Phytomedicine : international journal of phytotherapy and phytopharmacology 2007;14:15-22.
- Hagenlocher Y, Bergheim I, Zacheja S, Schaffer M, Bischoff SC, Lorentz A. 2013. Cinnamon extract inhibits degranulation and de novo synthesis of inflammatory mediators in mast cells. Allergy 68: 490-497.
- Matan N, Rimkeeree H, Mawson AJ, Chompreeda P, Haruthaithanasan V, Parker M. 2006. Antimicrobiële activiteit van kaneel- en kruidnagelolie onder gemodificeerde atmosfeer. Int J Food Microbiol 107: 180-185.
- Fink RC, Roschek B Jr, Alberte RS. 2009. HIV type-1 entry inhibitors with a new mode of action. Antivir Chem Chemother 19: 243-255.
- Yang CH, Li RX, Chuang LY. 2012. Antioxidant activiteit van verschillende delen van Cinnamomum cassia geëxtraheerd met verschillende extractiemethoden. Molecules 17: 7294-7304.
- Peterson DW et al. 2009. Kaneel extract remt tau aggregatie geassocieerd met de ziekte van Alzheimer in vitro. J Alzheimers Dis 17: 585-597.
- Cheng DM, Kuhn P, Poulev A, Rojo LE, Lila MA, Raskin I. 2012. In vivo and in vitro antidiabetic effects of aqueous cinnamon extract and cinnamon polyphenol-enhanced food matrix. Food Chem 135: 2994-3002.
- Kim JE et al. 2015a. Een nieuw kaneelgerelateerd natuurlijk product met Pim-1 remmende activiteit remt leukemie en huidkanker. Cancer Res 75: 2716-2728.
- Hwang H et al. 2011. 2′-Hydroxycinnamaldehyde targets low-density lipoprotein receptor-related protein-1 to inhibit lipopolysaccharide-induced microglial activation. J Neuroimmunol2011 230: 52-56.
- Shaughnessy DT, Setzer RW, DeMarini DM. 2001. De antimutagene werking van vanilline en cinnamaldehyde op spontane mutatie in Salmonella TA104 is toe te schrijven aan een vermindering van mutaties op GC- maar niet op AT-locaties. Mutat Res 480: 55-69.
- Zhang LQ, Zhang ZG, Fu Y, Xu Y. Onderzoeksvoortgang van trans-cinnamaldehyde farmacologische effecten. Zhongguo Zhong yao za zhi = Zhongguo zhongyao zazhi = China journal of Chinese materia medica 2015;40:4568-4572.
- Zhao H, Xie Y, Yang Q, Cao Y, Tu H, Cao W, Wang S. Farmacokinetische studie van cinnamaldehyde bij ratten door gc-ms na orale en intraveneuze toediening. Journal of pharmaceutical and biomedical analysis 2014;89:150-157.
- Kwon BM et al. 1998. Synthesis and in vitro cytotoxicity of cinnamaldehydes to human solid tumor cells. Arch Pharm Res 21: 147-152.
- Lee CW et al. 1999. Inhibition of human tumor growth by 2′-hydroxyand 2′-benzoyloxycinnamaldehydes. Planta Med 65: 263-266
- Kwon HK et al. 2009. Cinnamon extract suppresses tumor progression by modulating angiogenesis and the effector function of CD8+ T cells. Cancer Lett 278: 174-182.
- Lu J, Zhang K, Nam S, Anderson RA, Jove R,WenW. 2010. Novel angiogenesis inhibitory activity in cinnamon extract blocks VEGFR2 kinase and downstream signaling. Carcinogenesis 31: 481-488.
- Jeong HW et al. 2000. Cinnamaldehydes inhibit cyclin dependent kinase 4/cyclin D1. Bioorg Med Chem Lett 10: 1819-1822.
- Ka H et al. 2003. Cinnamaldehyde induceert apoptose door ROS-gemedieerde mitochondriale permeabiliteitsovergang in menselijke promyelocytische leukemie HL-60 cellen. Cancer Lett 196: 143-152.
- Wu SJ, Ng LT, Lin CC. 2005. Cinnamaldehyde-geïnduceerde apoptose in menselijke PLC/PRF/5-cellen door activering van de proapoptotische Bcl-2-familie-eiwitten en de MAPK-route. Life Sci 77: 938-951.
- Shin DS et al. 2006. Synthesis and biological evaluation of dimeric cinnamaldehydes as potent antitumor agents. Bioorg Med Chem 14: 2498-2506.
- Shin SY et al. 2014. Polyfenolen dragende cinnamaldehyde scaffold tonen celgroei remmende effecten op de cisplatine-resistente A2780/Cis eierstokkankercellen. Bioorg Med Chem 22: 1809-1820.
- Lee SC, Xu WX, Lin LY, Yang JJ, Liu CT. Chemische samenstelling en hypoglykemisch en pancreas-beschermend effect van blad etherische olie van inheemse kaneel. Journal of agricultural and food chemistry 2013;61:4905-4913.
- El-Bassossy HM, Fahmy A, Badawy D. Cinnamaldehyde beschermt tegen de hypertensie geassocieerd met diabetes. Food and chemical toxicology : an international journal published for the British Industrial Biological Research Association 2011;49:3007-3012.
- Li M, Xu Y, Zhang W. Effecten van kaneelaldehyde op de expressieniveaus van irs-1 en p85 alpha in de gastrocnemius van type 2 diabetische ratten. Medical Journal of Wuhan University 2009;30:723-726=731.
- Kumar S, Vasudeva N, Sharma S. Gc-ms analyse en screening van antidiabetisch, antioxidant en hypolipidemisch potentieel van cinnamomum tamala olie bij streptozotocine geïnduceerde diabetes mellitus bij ratten. Cardiovasculaire diabetologie 2012;11:95.
- Camacho S, Michlig S, de Senarclens-Bezencon C, Meylan J, Meystre J, Pezzoli M, Markram H, le Coutre J. Anti-obesitas en anti-hyperglycemische effecten van cinnamaldehyde via veranderde ghrelinesecretie en functionele impact op voedselinname en maaglediging. Scientific reports 2015;5:7919.
- Navarro SJ, Trinh T, Lucas CA, Ross AJ, Waymire KG, Macgregor GR. De c57bl/6j muizenstam achtergrond wijzigt het effect van een mutatie in bcl2l2. G3 2012;2:99-102.
- Mekada K, Abe K, Murakami A, Nakamura S, Nakata H, Moriwaki K, Obata Y, Yoshiki A. Genetic differences among c57bl/6 substrains. Experimental animals 2009;58:141-149.
- Kiselycznyk C, Holmes A. All mice are not created equal. Frontiers in neuroscience 2011;5:10.
- Attane C, Peyot ML, Lussier R, Zhang D, Joly E, Madiraju SR, Prentki M. Differential insulin secretion of high-fat diet-fed c57bl/6nn and c57bl/6nj mice: Implicaties van gemengde genetische achtergrond in metabole studies. PloS one 2016;11:e0159165.
- Nicholas P G, Schnuckc. JK, Mermierd. CM, Conne. CA, Vaughanc. RA. Trans-cinnamaldehyde stimuleert mitochondriale biogenese via pgc-1α en pparβ/δ leidend tot verhoogde glut4 expressie. Biochimie 2015;119:45-51.
- Zhang W, Xu YC, Guo FJ, Meng Y, Li ML. Anti-diabetische effecten van cinnamaldehyde en berberine en hun effecten op retinol-bindend eiwit 4 expressie bij ratten met type 2 diabetes mellitus. Chin Med J 2008;121:2124-2128.
- Bandyopadhyay GK, Yu JG, Ofrecio J, Olefsky JM. Increased p85/55/50 expression and decreased phosphotidylinositol 3-kinase activity in insulin-resistant human skeletal muscle. Diabetes 2005;54:2351-2359.
- Saraswathi V, Ramnanan CJ, Wilks AW, Desouza CV, Eller AA, Murali G, Ramalingam R, Milne GL, Coate KC, Edgerton DS. Impact van hematopoietische cyclooxygenase-1 deficiëntie op obesitas-gelinkte vetweefselontsteking en metabole stoornissen bij muizen. Metabolism: clinical and experimental 2013;62:1673-1685.
- Ohaeri OC. Effect van knoflookolie op de niveaus van verschillende enzymen in het serum en weefsel van streptozotocine diabetische ratten. Bioscience reports 2001;21:19-24.
- Mahfouz MH, Assiri AM, Mukhtar MH. Beoordeling van neutrofiele gelatinase-geassocieerde lipocaline (ngal] en retinol-bindend eiwit 4 in type 2 diabetespatiënten met nefropathie. Biomarker insights 2016;11:31-40.
- SHAN, B., CAY, Y.-Z., BROOKS, J.D. and CORKE, H. 2007. Antibacteriële eigenschappen en belangrijkste bioactieve bestanddelen van kaneelstok: Activiteit tegen pathogene bacteriën in levensmiddelen. J. Agric. Food Chem. 55, 5484-5490
- RHAYOUR, K., BOUCHIKHI, T., TANTAOUI-ELARAKI, A., SENDIDE, K. and REMMAL, A. 2003. Het mechanisme van bactericide werking van oregano en kruidnagel essentiële oliën van hun fenolische hoofdcomponenten op Escherichia coli en Bacillus subtilis. J. Essent. Oil Res. 15, 356-362.
- KIM, H.-O., PARK, S.-W. and PARK, H.-D. 2004. Inactivation of Escherichia coli O157:H7 by cinnamic aldehyde purified from Cinnamomum cassia shoot. Food Microbiol. 21, 105-110
- WENDAKOON, C. and SAKAGUCHI, M. 1995. Inhibition of amino acid decarboxylase activity of Enterobacter aerogenes by active components in spices. J. Food Prot. 58, 280-283.
- SMID, E.J., KOEKEN, J.P.G. and GORRIS, L.G.M. 1996. Fungicidal and fungistatic action of the secondary plant metabolites cinnamaldehyde and carvone. In Modern Fungicides and Antimicrobial Compounds pp. 173-180, Intercept, Andover, U.K.
- Dugoua JJ, Seely D, Perri D, Cooley K, Forelli T, Mills E, Koren G. From type 2 diabetes to antioxidant activity: A systematic review of the safety and efficacy of common and cassia cinnamon bark. Canadian journal of physiology and pharmacology 2007;85:837-847.
- Anand P, Murali KY, Tandon V, Murthy PS, Chandra R. Insulinotroop effect van kaneelaldehyde op de transcriptieregulatie van pyruvaat kinase, fosfoenolpyruvaat carboxykinase, en glut4 translocatie bij experimentele diabetische ratten. Chemisch-biologische interacties 2010;186:72-81.
- Gowder SJT. Veiligheidsbeoordeling van voedingssmaakstof -cinnamaldehyde. Biosafety 2014;3
- Hooth MJ, Sills RC, Burka LT, Haseman JK, Witt KL, Orzech DP, Fuciarelli AF, Graves SW, Johnson JD, Bucher JR. Toxicology and carcinogenesis studies of microencapsulated trans-cinnamaldehyde in rats and mice. Food and chemical toxicology : an international journal published for the British Industrial Biological Research Association 2004;42:1757-1768.
- Swales NJ, Caldwell J. Studies on trans-cinnamaldehyde ii: Mechanisms of cytotoxicity in rat isolated hepatocytes. Toxicology in vitro : an international journal published in association with BIBRA 1996;10:37-42.
- Sanyal R, Darroudi F, Parzefall W, Nagao M, Knasmuller S. Inhibition of the genotoxic effects of heterocyclic amines in human derived hepatoma cells by dietary bioantimutagens. Mutagenesis 1997;12:297-303.
- Behar RZ, Luo W, Lin SC, Wang Y, Valle J, Pankow JF, Talbot P. Distributie, kwantificering en toxiciteit van cinnamaldehyde in navulvloeistoffen en aerosolen van elektronische sigaretten. Tobacco control 2016
- Olsen RV, Andersen HH, Moller HG, Eskelund PW, Arendt-Nielsen L. Somatosensory and vasomotor manifestations of individual and combined stimulation of trpm8 and trpa1 using topical l-menthol and trans-cinnamaldehyde in healthy volunteers. European journal of pain 2014;18:1333-1342.
Chemische eigenschappen
trans-Cinnamaldehyde is het hoofdbestanddeel van cassia-olie (ongeveer 90%) en Sri Lanka kaneelschorsolie (ongeveer 75%). Kleinere hoeveelheden worden aangetroffen in veel andere etherische oliën. In de natuur overheerst de trans-isomeer.
Trans-Cinnamaldehyde is een geelachtige vloeistof met een karakteristieke kruidige geur, die sterk aan kaneel doet denken. Omdat het een onverzadigd aldehyde is, ondergaat het vele reacties, waarvan hydrogenering tot cinnamalcohol, dihydrocinnamaldehyde en dihydrocinnamalcohol belangrijk is. Kaneelzuur wordt gevormd door autoxidatie.
Op industriële schaal wordt kaneelaldehyde bijna uitsluitend bereid door alkalische condensatie van benzaldehyde en aceetaldehyde. Zelfcondensatie van acetaldehyde kan worden vermeden door een overmaat benzaldehyde te gebruiken en langzaam acetaldehyde toe te voegen.
Cinnamaldehyde wordt gebruikt in veel samenstellingen voor het creëren van kruidige en oriëntaalse geuren (bijv. zeepparfums). Het is het hoofdbestanddeel van kunstmatige kaneelolie. Daarnaast is het een belangrijk tussenproduct bij de synthese van kaneelalcohol en dihydrocinnamalcohol.
Chemische eigenschappen
HELDERE GELE VLOEISTOF
Chemische eigenschappen
Brandbare, gelige, olieachtige vloeistof (wordt dikker bij blootstelling aan de lucht). Sterke doordringende, kruidige kaneelgeur.
Definitie
ChEBI: Het stereoisomeer E (trans) van cinnamaldehyde, de ouder van de klasse der cinnamaldehyden.
Syntheseverwijzing(en)
Chemistry Letters, 12, p. 1207, 1983
Journal of the American Chemical Society, 93, p. 2080, 1971 DOI: 10.1021/ja00737a057
Tetrahedron Letters, 18, p. 1215, 1977
Algemene beschrijving
Heldere gele vloeistof met een geur van kaneel en een zoete smaak.
Air & Waterreacties
Kan gevoelig zijn voor langdurige blootstelling aan lucht en licht. Onoplosbaar in water.
Reactiviteitsprofiel
trans-Cinnamaldehyde is onverenigbaar met sterke oxidatiemiddelen en sterke basen. trans-Cinnamaldehyde kan ook reageren met natriumhydroxide.
Vuurgevaar
trans-Cinnamaldehyde is brandbaar.
Mogelijke blootstelling
Botanisch fungicide en insecticide. Gebruikt als schimmelwerend middel, lokmiddel voor maïswortelboorders, en honden- en kattenafweermiddel. Kan worden gebruikt op bodembedekking voor champignons, rijgewassen, graszoden en alle voedingsmiddelen. Niet vermeld voor gebruik in EU-landen.
Verlading
UN1989 Aldehyden, n.e.g., Gevarenklasse: 3; Etiketten: 3-Ontvlambare vloeistof
Onverenigbaarheden
Aldehyden zijn vaak betrokken bij zelfcondensatie- of polymerisatiereacties. Deze reacties zijn exotherm; zij worden vaak gekatalyseerd door zuur. Aldehyden worden gemakkelijk geoxideerd om carboxylzuren te geven. Brandbare en/of giftige gassen ontstaan door de combinatie van aldehyden met azo-, diazoverbindingen, dithiocarbamaten, nitriden en sterke reductiemiddelen. Aldehyden kunnen met lucht reageren om eerst peroxozuren en uiteindelijk carboxylzuren te geven. Deze autoxidatiereacties worden geactiveerd door licht, gekatalyseerd door zouten van overgangsmetalen, en zijn autokatalytisch (gekatalyseerd door de producten van de reactie). De toevoeging van stabilisatoren (antioxidanten) aan vrachten aldehyden vertraagt de autoxidatie. Onverenigbaar met oxidatiemiddelen (chloraten, nitraten, peroxiden, permanganaten, perchloraten, chloor, broom, fluor, enz.); contact kan brand of explosies veroorzaken. Verwijderd houden van alkalische stoffen, sterke basen, sterke zuren, oxozuren, epoxiden, ketonen, azokleurstoffen, bijtende stoffen, boranen, hydrazinen
Verwijdering van afval
Verbranding. In overeenstemming met 40CFR165, volg de aanbevelingen voor de verwijdering van pesticiden en pesticidencontainers.