-
 Inleiding
Inleiding - Hoe werken serotonine-blokkerende medicijnen?
- Wat zijn de verschillende soorten serotonine-blokkerende medicijnen?
- Eerste generatie serotonine-blokkers
- Tweede generatie serotonine-blokkers
- Waarvoor worden serotonine-blokkerende geneesmiddelen gebruikt?
- Chemotherapie-geïnduceerde misselijkheid en braken (CINV)
- Radiation-geïnduceerde misselijkheid en braken (RINV)
- Post-operatieve misselijkheid en braken (PONV)
- Wat zijn de bijwerkingen van het gebruik van serotonine-blokkerende medicijnen?
- Is er een wisselwerking tussen serotonine-blokkerende geneesmiddelen en andere geneesmiddelen?
- Inleiding
- Hoe werken serotonine-blokkerende geneesmiddelen?
- Wat zijn de verschillende soorten serotonine-blokkerende geneesmiddelen?
- Waarvoor worden serotonine-blokkerende geneesmiddelen gebruikt?
- Wat zijn de bijwerkingen van het gebruik van serotonine-blokkerende medicijnen?
- Hebben serotonine-blokkerende geneesmiddelen een wisselwerking met andere geneesmiddelen?
- Meer informatie
Inleiding
5-hydroxytryptamine receptor antagonisten (5-HT3 RA’s) zijn een groep geneesmiddelen die worden gebruikt om misselijkheid en braken onder controle te houden. Zij ontlenen hun naam aan hun vermogen om 5-hydroxytryptamine (ook bekend als serotonine) te blokkeren van de activering van zenuwen die de braakreflex teweegbrengen. 5-HT3 RA’s, of serotonineblokkers, werden oorspronkelijk ontdekt in de jaren negentig en zijn een van de nieuwste soorten geneesmiddelen tegen braken op de markt. De effectiviteit van deze geneesmiddelen heeft een revolutie teweeggebracht in de behandeling van misselijkheid en braken, met name bij personen die chemotherapie of radiotherapie ondergaan en bij de behandeling van misselijkheid en braken na een operatie.
Er zijn momenteel vijf serotonineblokkers in de handel in Australië voor de behandeling of preventie van chemotherapie-geïnduceerde misselijkheid en braken (CINV), waaronder dolasetron (Anzemet), granisetron (Kytril), ondansetron (Zofran), tropisetron (Navoban) en palonosetron (Aloxi). Deze geneesmiddelen werken door het blokkeren van de werking van serotonine op zenuwen die braakimpulsen doorgeven van de darmen naar de hersenen.
Ondanks dat ze een verschillende chemische samenstelling en verschillende absorptieprofielen hebben, zijn de meeste geneesmiddelen in deze klasse even effectief. De bovengenoemde serotonineblokkers worden zeer goed verdragen met minimale bijwerkingen. Deze geneesmiddelen kunnen over het algemeen veilig worden ingenomen met andere voorgeschreven medicijnen, maar het is altijd verstandig om mogelijke interacties te bespreken met uw arts of apotheker voordat u twee geneesmiddelen tegelijk inneemt.
Hoe werken serotonine-blokkerende geneesmiddelen?
Overgeven en misselijkheid worden teweeggebracht door een complex proces dat verschillende stappen omvat. Uiteindelijk gaat het om de activering van een gebied in de hersenen dat bekend staat als het “braakcentrum”. Dit centrum is verantwoordelijk voor het coördineren van signalen van het lichaam, het verwerken ervan en het activeren van de braakreflex. Het braakcentrum ontvangt signalen uit verschillende delen van de hersenen, waaronder het evenwichtscentrum, naast de maag en de keel.
Serotonine (5-HT3) is de chemische boodschapper die verantwoordelijk is voor het overbrengen van braaksignalen. Het bindt zich aan receptoren op zenuwen in de maag en de hersenen, die impulsen naar het braakcentrum transporteren.
Chemotherapie en radiotherapie zouden braken veroorzaken door beschadiging van de cellen die de darmen bekleden. Deze cellen geven dan de serotonine vrij die in hen is opgeslagen en die zich vervolgens bindt aan zenuwen die een braakopwekkende impuls van de maag naar het braakcentrum overbrengen. Zodra dit signaal het braakcentrum bereikt, activeert serotonine andere zenuwen die betrokken zijn bij het activeren van de braakreflex.
Nausea en braken na een operatie worden minder goed begrepen, maar zijn waarschijnlijk het gevolg van een aantal verschillende factoren, waaronder de gebruikte anesthesie, het type en de duur van de operatie, en persoonsgebonden factoren. Hiervan wordt aangenomen dat bepaalde soorten anesthetica de sterkste risicofactor vormen.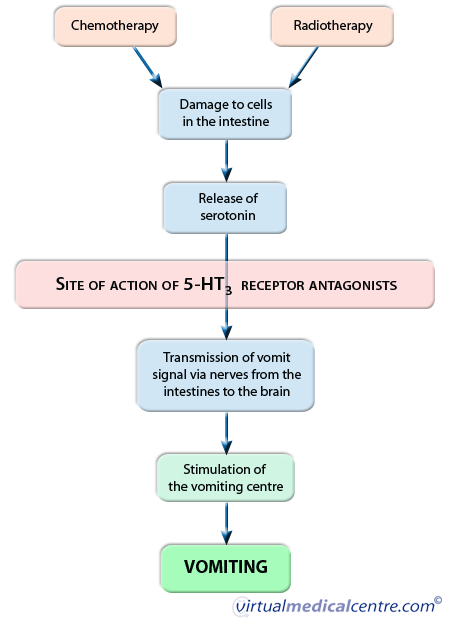
 |
Voor meer informatie over de maag, keel en darmen, zie Anatomie van het maag-darmstelsel. |
Wat zijn de verschillende soorten serotonine-blokkerende geneesmiddelen?
 Vijf serotonine-blokkerende middelen worden momenteel in Australië op de markt gebracht, waaronder dolasetron (Anzemet), granisetron (Kytril), ondansetron (Zofran), tropisetron (Navoban) en palonosetron (Aloxi). Palonosetron, in 2003 goedgekeurd door de Amerikaanse Food and Drug Administration (FDA), is de nieuwste serotonineblokker en wordt beschouwd als een middel van de tweede generatie, omdat het een andere chemische structuur heeft en op een iets andere manier werkt dan de andere middelen.
Vijf serotonine-blokkerende middelen worden momenteel in Australië op de markt gebracht, waaronder dolasetron (Anzemet), granisetron (Kytril), ondansetron (Zofran), tropisetron (Navoban) en palonosetron (Aloxi). Palonosetron, in 2003 goedgekeurd door de Amerikaanse Food and Drug Administration (FDA), is de nieuwste serotonineblokker en wordt beschouwd als een middel van de tweede generatie, omdat het een andere chemische structuur heeft en op een iets andere manier werkt dan de andere middelen.
Serotonineblokkers van de eerste generatie
Dolasetron, granisetron, ondansetron en tropisetron worden serotonineblokkers van de eerste generatie genoemd. Ondanks hun verschillende chemische structuur en absorptie door het lichaam, werken alle geneesmiddelen van de eerste generatie op dezelfde manier en hebben ze vergelijkbare bijwerkingen.
Er is enorm veel onderzoek gedaan naar de eerste-generatie serotonine-blokkers, met als resultaat de volgende hoofdpunten:
- De verschillende serotonineblokkerende middelen zijn even effectief en kunnen daarom door elkaar worden gebruikt;
- Deze middelen worden goed verdragen en hebben weinig bijwerkingen;
- De laagste eenmaal daagse dosis die misselijkheid en braken volledig voorkomt, moet worden gebruikt; en
- De tabletvorm van het middel (orale vorm) is net zo effectief in het voorkomen van braken als de intraveneuze vorm.
Serotonineblokkers van de tweede generatie
Palonosetron is in 2003 door de FDA goedgekeurd als serotonineblokker van de tweede generatie. Het bindt zich veel sterker aan zijn receptor dan de geneesmiddelen van de eerste generatie, en werkt daarom gedurende een langere periode. Terwijl van de eerste-generatie geneesmiddelen wordt gedacht dat ze alleen binden aan zenuwen in de darmen, wordt gedacht dat palonosetron ook werkt door direct te binden aan receptoren in de hersenen.
Palonosetron is het eerste geneesmiddel dat door de FDA is goedgekeurd voor de preventie van zowel acute als uitgestelde CINV.
Waarvoor worden serotonine-blokkerende geneesmiddelen gebruikt?
Chemotherapie-geïnduceerde misselijkheid en braken (CINV) Serotonine-blokkerende geneesmiddelen hebben een revolutie teweeggebracht in de behandeling van CINV, en deze middelen vormen nu de hoeksteen van de anti-misselijkheidstherapie bij deze aandoening. Vóór de ontdekking van deze geneesmiddelen was braken de meest gevreesde bijwerking van chemotherapie. Sinds de introductie van serotonine-blokkers is braken de op twee na meest gevreesde bijwerking geworden, na misselijkheid en haaruitval.
Serotonine-blokkerende geneesmiddelen hebben een revolutie teweeggebracht in de behandeling van CINV, en deze middelen vormen nu de hoeksteen van de anti-misselijkheidstherapie bij deze aandoening. Vóór de ontdekking van deze geneesmiddelen was braken de meest gevreesde bijwerking van chemotherapie. Sinds de introductie van serotonine-blokkers is braken de op twee na meest gevreesde bijwerking geworden, na misselijkheid en haaruitval.
CINV kan worden ingedeeld in acuut, vertraagd, anticiperend, doorbraak of refractair, op basis van wanneer het optreedt in relatie tot de toediening van chemotherapie.
CINV treft 70-80% van de mensen met kanker, en heeft een aanzienlijke impact op zowel het individu als de middelen in de gezondheidszorg.
Factoren die de kans vergroten dat u CINV krijgt, kunnen grofweg worden ingedeeld in geneesmiddelgerelateerde factoren en persoonsgerelateerde factoren. Geneesmiddelgerelateerde risicofactoren zijn onder meer de waarschijnlijkheid dat het chemotherapeutisch middel braken opwekt (de “emetogeniciteit”), de dosis van het geneesmiddel en de manier waarop het geneesmiddel wordt ingenomen (bv. via de mond of rechtstreeks in een ader geïnjecteerd). Individuele risicofactoren zijn leeftijd, geslacht, eerdere chemotherapie, geschiedenis van reisziekte of misselijkheid bij zwangerschap, en geschiedenis van zwaar alcoholgebruik.
De huidige richtlijnen die zijn ontwikkeld als resultaat van uitgebreid onderzoek pleiten voor het gebruik van serotonineblokkers bij de behandeling van zowel acute als uitgestelde CINV. Voor de preventie van acute misselijkheid en braken bij sterk braakverwekkende chemotherapie wordt een combinatie van een serotonineblokker, een corticosteroïd (zoals dexamethason) en een stof-P (NK-1)-blokker (aprepitant) aanbevolen. Deze middelen moeten worden toegediend voordat de chemotherapie wordt gestart.
Voor de preventie van acute CINV met matig braakinducerende chemotherapie wordt een combinatie van een serotonineblokker en dexamethason aanbevolen, al dan niet met een stof-P-blokker. Opgemerkt zij dat corticosteroïden zoals dexamethason weliswaar een nuttige aanvullende rol spelen bij het voorkomen van braken, maar dat zij aanzienlijke bijwerkingen hebben. Uit één onderzoek bleek dat sommige personen die dexamethason kregen voor matig braakverwekkende chemotherapie matige tot ernstige slapeloosheid, maagklachten of indigestie, agitatie, toegenomen eetlust, gewichtstoename of acne ervoeren in de week na de chemotherapie.
Palonosetron is de serotonineblokker bij uitstek voor het voorkomen van acute misselijkheid en braken na matig braakverwekkende chemotherapie. Een eenmalige dosis palonosetron wordt toegediend voor het begin van de chemotherapie, zonder noodzaak voor aanvullende dosering op dag 2 en 3.
De meest recente richtlijnen pleiten voor het gebruik van palonosetron geïnjecteerd in de ader bij de behandeling van vertraagde CINV op dag 1 van de chemotherapie alleen. Het is de enige serotonine-blokker die beschikbaar is voor de behandeling van uitgesteld braken. Het effect van extra doses palonosetron is nog niet volledig bekend.
Uw oncoloog zal uw chemotherapieregime en uw specifieke risicofactoren evalueren alvorens te bepalen wat voor u de beste behandeling tegen braken is.
 |
Voor meer informatie over CINV, zie Chemotherapy-Induced Nausea and Vomiting (CINV). |
Radiation-induced nausea and vomiting (RINV) Het mechanisme waarmee bestraling misselijkheid en braken opwekt, is hetzelfde als bij CINV. Uit de statistieken blijkt dat 50-80% van de mensen die radiotherapie krijgen, misselijkheid en/of braken zullen ervaren. Personen die bestraald worden in het hele lichaam of in de bovenbuik lopen het grootste risico om RINV te ontwikkelen. Het risico op RINV neemt toe naarmate de dagelijkse dosis radiotherapie, de totale dosis radiotherapie en de hoeveelheid aan straling blootgesteld lichaamsweefsel toeneemt.
Het mechanisme waarmee bestraling misselijkheid en braken opwekt, is hetzelfde als bij CINV. Uit de statistieken blijkt dat 50-80% van de mensen die radiotherapie krijgen, misselijkheid en/of braken zullen ervaren. Personen die bestraald worden in het hele lichaam of in de bovenbuik lopen het grootste risico om RINV te ontwikkelen. Het risico op RINV neemt toe naarmate de dagelijkse dosis radiotherapie, de totale dosis radiotherapie en de hoeveelheid aan straling blootgesteld lichaamsweefsel toeneemt.
Het voorkomen van RINV hangt af van welk deel van het lichaam wordt bestraald en of de bestraling al dan niet wordt gecombineerd met chemotherapie. Wanneer radiotherapie met chemotherapie wordt gecombineerd, moet de sterkte van de chemotherapiemiddelen bepalen welke anti-braakmiddelen worden gebruikt. Serotonine-blokkerende medicijnen zijn de voorkeursmedicijnen tegen braken om RINV te voorkomen. Personen die bestraald worden in de bovenste maagstreek en het hele bovenlichaam moeten een serotonineblokker (ondansetron of granisetron) krijgen met of zonder een corticosteroïde (dexamethason).
Uw oncoloog zal uw radiotherapieregime en uw specifieke risicofactoren evalueren alvorens te bepalen wat voor u de beste behandeling tegen braken is.
Postoperatieve misselijkheid en braken (PONV)
Ondanks de ontwikkelingen op het gebied van geneesmiddelen tegen braken, komt braken en misselijkheid nog steeds voor bij 20-30% van de mensen na een operatie. Risicofactoren voor de ontwikkeling van PONV kunnen grofweg worden onderverdeeld in factoren die verband houden met de anesthesie, factoren die verband houden met de persoon, en factoren die verband houden met het type en de duur van de operatie.
Serotonine-blokkerende geneesmiddelen worden sterk aanbevolen bij de preventie en behandeling van PONV. Preventie van misselijkheid en braken bij deze personen wordt geleid door risicofactoren die personen groeperen in hoog, matig of laag risico op het ontwikkelen van PONV. Personen die op basis van hun risicofactoren een matig of hoog risico lopen om PONV te ontwikkelen, moeten naast andere geneesmiddelen tegen braken ook een serotonineblokker krijgen. Serotonine-blokkerende geneesmiddelen werken het best wanneer ze aan het einde van de operatie worden toegediend.
Voor mensen met PONV die aan het einde van de operatie geen preventieve dosis 5-HT3 RA hebben gekregen, is de beste behandeling een kleine dosis van een serotonine-blokkerend geneesmiddel. Personen die binnen de eerste 6 uur na de operatie PONV ontwikkelen, moeten worden behandeld met een geneesmiddel uit een andere klasse dan het geneesmiddel dat werd gebruikt om de misselijkheid en het braken te voorkomen. Personen die meer dan 6 uur na hun operatie PONV ontwikkelen, kunnen worden behandeld met elk van de geneesmiddelen tegen braken, met uitzondering van dexamethason.
Uw chirurg of anesthesist zal uw specifieke risicofactoren evalueren alvorens te bepalen wat de beste behandeling tegen braken voor u is.
Wat zijn de bijwerkingen van het gebruik van serotonine-blokkerende medicijnen?
 Als groep worden serotonine-blokkerende medicijnen over het algemeen zeer goed verdragen met minimale, kortdurende bijwerkingen. De meest voorkomende bijwerkingen zijn hoofdpijn, duizeligheid, maagpijn, constipatie, vermoeidheid, verstoring van de leverfunctie en veranderingen in de elektrische geleiding van het hart. In een groot onderzoek onder personen die de tabletvorm van granisetron kregen, ervoer 15% hoofdpijn, 6% verlies van energie, 5% diarree, 5% overmatige slaperigheid en 7% constipatie. In tegenstelling tot andere klassen van geneesmiddelen tegen braken, is niet aangetoond dat serotonine-blokkerende geneesmiddelen neurologische bijwerkingen veroorzaken.
Als groep worden serotonine-blokkerende medicijnen over het algemeen zeer goed verdragen met minimale, kortdurende bijwerkingen. De meest voorkomende bijwerkingen zijn hoofdpijn, duizeligheid, maagpijn, constipatie, vermoeidheid, verstoring van de leverfunctie en veranderingen in de elektrische geleiding van het hart. In een groot onderzoek onder personen die de tabletvorm van granisetron kregen, ervoer 15% hoofdpijn, 6% verlies van energie, 5% diarree, 5% overmatige slaperigheid en 7% constipatie. In tegenstelling tot andere klassen van geneesmiddelen tegen braken, is niet aangetoond dat serotonine-blokkerende geneesmiddelen neurologische bijwerkingen veroorzaken.
Verschanderingen in de elektrische activiteit van het hart zoals vastgelegd op een elektrocardiogram (ECG) zijn gemeld bij deze klasse van geneesmiddelen. Er zijn echter geen ernstige voorvallen met betrekking tot de hartactiviteit toegeschreven aan deze klasse van geneesmiddelen. Wanneer u het gebruik van serotonine-blokkerende geneesmiddelen met uw arts bespreekt, dient u hem te informeren over elke vroegere of bestaande hartaandoening die u had of heeft.
Er is slechts beperkte informatie over het gebruik van deze geneesmiddelen bij zwangere vrouwen of vrouwen die borstvoeding geven, en u dient uw arts te raadplegen als u van plan bent zwanger te worden of borstvoeding te geven.
Hebben serotonine-blokkerende geneesmiddelen een wisselwerking met andere geneesmiddelen?
Alle geneesmiddelen in deze groep worden verwerkt via dezelfde route in de lever. Dit heeft de mogelijkheid om de absorptie van andere geneesmiddelen te beïnvloeden die dezelfde route gebruiken. Dit risico is groter bij personen die chemotherapie en radiotherapie ondergaan, en bij personen die in het ziekenhuis zijn opgenomen. Hoewel deze interacties de absorptie van andere geneesmiddelen kunnen beïnvloeden, zijn dergelijke gevallen niet gemeld. Het is van groot belang dat u uw arts vertelt welke geneesmiddelen u gebruikt, zodat deze het risico van mogelijke wisselwerkingen kan beoordelen.
Meer informatie
 |
Voor meer informatie over misselijkheid en braken, waaronder wat de oorzaak is, hoe het gebeurt, de gevolgen en het omgaan met en behandelen van misselijkheid en braken, zie Misselijkheid en braken (Emesis). |
 |
Voor meer informatie over geneesmiddelen, waaronder een inleiding in de farmacologie, generieke geneesmiddelen versus merkgeneesmiddelen, en de betekenis van geneesmiddelenschema’s en zwangerschapscategorieën, zie Geneesmiddelen. |
- Gregory RE, Ettinger DS. 5-HT3-receptorantagonisten voor de preventie van door chemotherapie veroorzaakte misselijkheid en braken. A comparison of their pharmacology and clinical efficacy. Drugs. 1998;55(2):173-89.
- Hesketh PJ. Chemotherapy-induced nausea and vomiting. N Engl J Med. 2008;358(23):2482-94.
- de Boer-Dennert M, de Wit R, Schmitz PI, et al. Patient perceptions of the side-effects of chemotherapy: De invloed van 5HT3 antagonisten. Br J Cancer. 1997;76(8):1055-61.
- 5HT3 receptoren. Adelaide, SA: Australian Medicines Handbook; januari 2011 . Available from: URL link
- Navari RM. Farmacologisch beheer van door chemotherapie veroorzaakte misselijkheid en braken: Focus op recente ontwikkelingen. Geneesmiddelen. 2009;69(5):515-33.
- Rubenstein EB. Palonosetron: A unique 5-HT3 receptor antagonist indicated for the prevention of acute and delayed chemotherapy-induced nausea and vomiting. Clin Adv Hematol Oncol. 2004;2(5):284-9.
- Dilly S. Granisetron (Kytril) klinische veiligheid en tolerantie. Semin Oncol. 1994;21(3 Suppl 5):10-4.
- Baker PD, Morzorati SL, Ellett ML. The pathophysiology of chemotherapy-induced nausea and vomiting. Gastroenterol Nurs. 2005;28(6):469-80.
- Maricq AV, Peterson AS, Brake AJ, et al. Primaire structuur en functionele expressie van de 5HT3 receptor, een serotonine-gated ion channel. Science. 1991;254(5030):432-7.
- Kovac AL. Prevention and treatment of postoperative nausea and vomiting. Drugs. 2000;59(2):213-43.
-
Apfel CC, Kranke P, Katz MH, et al. Volatile anaesthetics may be the main cause of early but not delayed postoperative vomiting: A randomized controlled trial of factorial design. Br J Anaesth. 2002;88(5):659-68.
- Billio A, Morello E, Clarke MJ. Serotonin receptor antagonists for highly emetogenic chemotherapy in adults. Cochrane Database Syst Rev. 2010;(1):CD006272.
- Jordan K, Sippel C, Schmoll HJ. Guidelines for antiemetic treatment of chemotherapy-induced nausea and vomiting: Verleden, heden en toekomstige aanbevelingen. Oncologist. 2007;12(9):1143-50.
- Perwitasari DA, Gelderblom H, Atthobari J, et al. Anti-emetic drugs in oncology: pharmacology and individualization by pharmacogenetics. Int J Clin Pharm. 2011;33(1):33-43.
- Rittenberg CN. De volgende generatie preventie en bestrijding van door chemotherapie veroorzaakte misselijkheid en braken: Een nieuwe 5-HT3 antagonist arriveert. Clin J Oncol Nurs. 2004;8(3):307-8, 310.
- Ettinger D, Armstrong K, Barbour S, et al. NCCN richtlijnen voor klinische praktijk in de oncologie: Antiemesis . Fort Washington, PA: National Comprehensive Cancer Care Network; 2011 . Available from: URL link
- Liau CT, Chu NM, Liu HE, et al. Incidence of chemotherapy-induced nausea and vomiting in Taiwan: Physicians’ and nurses’ estimation vs. patients’ reported outcomes. Support Care Kanker. 2005;13(5):277-86.
- Lohr L. Chemotherapy-induced nausea and vomiting. Cancer J. 2008;14(2):85-93.
- Pollera CF, Giannarelli D. Prognostische factoren die cisplatine-geïnduceerde emesis beïnvloeden. Definitie en validatie van een voorspellend logistisch model. Cancer. 1989;64(5):1117-22.
- Roila F, Herrstedt J, Aapro M, et al. Update van de richtlijnen voor MASCC en ESMO voor de preventie van door chemotherapie en radiotherapie veroorzaakte misselijkheid en braken: Resultaten van de Perugia consensus conferentie. Ann Oncol. 2010;21(Suppl 5):v232-43.
- Preventie van acute/vertraagde misselijkheid en braken (emesis) . Bethesda, MD: National Cancer Institute; 16 maart 2011 . Available from: URL link
- Grunberg SM, Warr D, Gralla RJ, et al. Evaluation of new antiemetic agents and definition of antineoplastic agent emetogenicity – state of the art. Support Care Cancer. 2011;19(Suppl 1):S43-7.
- Vardy J, Chiew KS, Galica J, et al. Side effects associated with the use of dexamethasone for prophylaxis of delayed emesis after moderately emetogenic chemotherapy. Br J Cancer. 2006;94(7):1011-5.
- Salvo N, Doble B, Khan L, et al. Prophylaxis of radiation-induced nausea and vomiting using 5-hydroxytryptamine-3 serotonin receptor antagonists: Een systematische review van gerandomiseerde trials. Int J Radiat Oncol Biol Phys. 2010 Nov 13.
- Cohen MM, Duncan PG, DeBoer DP, Tweed WA. Het postoperatieve interview: Assessing risk factors for nausea and vomiting. Anesth Analg. 1994;78(1):7-16.
-
Habib AS, Gan TJ. Evidence-based management of postoperative nausea and vomiting: Een overzicht. Can J Anaesth. 2004;51(4):326-41.
- Gan TJ, Meyer T, Apfel CC, et al. Consensus guidelines for managing postoperative nausea and vomiting. Anesth Analg. 2003;97(1):62-71.
- Keefe DL. The cardiotoxic potential of the 5-HT(3) receptor antagonist antiemetics: Is er reden tot bezorgdheid? Oncologist. 2002(7):65-72.
- Aapro M, Blower P. 5-hydroxytryptamine type-3 receptor antagonisten voor chemotherapie-geïnduceerde en radiotherapie-geïnduceerde nausea en emesis: Kunnen we de dosis van toegediende middelen veilig verminderen? Cancer. 2005;104(1):1-18.
- Navari RM, Koeller JM. Electrocardiographic and cardiovascular effects of the 5-hydroxytryptamine3 receptor antagonists. Ann Pharmacother. 2003;37(9):1276-86.
-
Aapro M. Granisetron: An update on its clinical use in the management of nausea and vomiting. Oncologist. 2004;9(6):673-86.