A legtöbb orvosi kezelést az “átlagpáciens” számára tervezték, egyféle megközelítéssel, amely egyes betegeknél sikeres lehet, másoknál viszont nem. A precíziós orvoslás, amelyet néha “személyre szabott orvoslásnak” is neveznek, a betegségek megelőzésének és kezelésének olyan innovatív megközelítése, amely figyelembe veszi az emberek génjeiben, környezetében és életmódjában rejlő különbségeket. A precíziós orvoslás célja, hogy a megfelelő kezeléseket a megfelelő betegekhez a megfelelő időben juttassa el.
A precíziós orvoslásban elért eredmények már olyan nagy hatású új felfedezésekhez és az FDA által jóváhagyott kezelésekhez vezettek, amelyeket az egyének sajátos jellemzőihez, például egy személy genetikai felépítéséhez vagy az egyén daganatának genetikai profiljához igazítottak. A különböző rákos megbetegedésekben szenvedő betegeknél a betegellátás részeként rutinszerűen végeznek molekuláris vizsgálatokat, amelyek lehetővé teszik az orvosok számára, hogy olyan kezeléseket válasszanak, amelyek javítják a túlélési esélyeket és csökkentik a káros hatásoknak való kitettséget.
- Újabb generációs szekvenáló (NGS) vizsgálatok
- Az FDA szerepe a precíziós orvoslás előmozdításában
- Streamlining FDA’s Regulatory Oversight of NGS Tests
- Klinikai adatbázisok útmutató
- Analitikai validációs útmutató
- FDA bioinformatikai platformja
- Kérdések?
- Mit mondanak az FDA tisztviselői
- NGS Final Guidances
- Beszámolók és vitairatok
- Múlt ülések
Újabb generációs szekvenáló (NGS) vizsgálatok
A precíziós ellátás csak annyira lesz jó, amennyire a diagnózist és a kezelést irányító vizsgálatok. Az újgenerációs szekvenáló (NGS) tesztek képesek gyorsan azonosítani vagy “szekvenálni” egy személy genomjának nagy szakaszait, és fontos előrelépést jelentenek a precíziós orvoslás klinikai alkalmazásaiban.
A betegek, orvosok és kutatók e tesztek segítségével olyan genetikai variánsokat találhatnak, amelyek segítenek diagnosztizálni, kezelni és jobban megérteni az emberi betegségeket.
Az FDA szerepe a precíziós orvoslás előmozdításában
Az FDA az NGS-tesztek pontosságának biztosításán dolgozik, hogy a betegek és a klinikusok pontos és klinikailag értelmezhető vizsgálati eredményeket kapjanak.
Az NGS által generált hatalmas mennyiségű információ új szabályozási kérdéseket vet fel az FDA számára. Míg a jelenlegi szabályozási megközelítések megfelelőek az egyetlen betegséget vagy állapotot (például a vércukor- vagy koleszterinszintet) kimutató hagyományos diagnosztikák esetében, addig ezek az új szekvenálási technikák több millió tesztnek felelnek meg egyben. Emiatt az FDA az ipar, a laboratóriumok, a tudományos élet, valamint a betegek és a szakmai társaságok érdekelt feleivel együttműködve rugalmas szabályozási megközelítést dolgozott ki e gyorsan fejlődő technológia befogadására, amely a konszenzusos szabványokat, a tömegesen gyűjtött adatokat és a legmodernebb nyílt forráskódú számítástechnikai technológiát használja fel az NGS-tesztek fejlesztésének támogatására. Ez a megközelítés lehetővé teszi az innovációt a tesztelés és a kutatás terén, és felgyorsítja a pontos, megbízható genetikai tesztekhez való hozzáférést.
Streamlining FDA’s Regulatory Oversight of NGS Tests
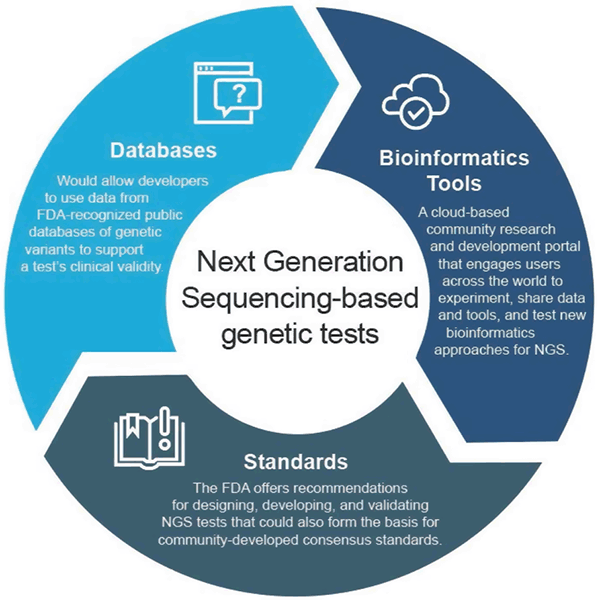
2018 áprilisában az FDA két végleges iránymutatást adott ki, amelyek megközelítéseket javasolnak az NGS-alapú tesztek klinikai és analitikai érvényességét alátámasztó adatok benyújtásának és felülvizsgálatának egyszerűsítésére. Ezen ajánlások célja, hogy hatékony és rugalmas szabályozási felügyeleti megközelítést biztosítsanak: a technológia fejlődésével a szabványok gyorsan fejlődhetnek és felhasználhatók a megfelelő mérőszámok meghatározására az olyan gyorsan fejlődő területeken, mint az NGS. Hasonlóképpen, a klinikai bizonyítékok javulásával új állítások is alátámaszthatók. Ez az adaptív megközelítés végső soron elősegítené az innovációt a tesztfejlesztők körében, és javítaná a betegek hozzáférését ezekhez az új technológiákhoz.
Klinikai adatbázisok útmutató
A végleges útmutató “A nyilvános humán genetikai variáns-adatbázisok használata a genetikai és genomikai alapú in vitro diagnosztika klinikai érvényességének alátámasztására” lehetővé teszi a fejlesztők számára, hogy az FDA által elismert nyilvános genetikai variáns-adatbázisokból származó adatokat használjanak a teszt klinikai érvényességének alátámasztására, és felvázolja, hogyan kérhetik az adatbázis-kezelők az adatbázisok elismerését, ha azok megfelelnek bizonyos minőségi ajánlásoknak. Ez a megközelítés ösztönzi az adatmegosztást, és hatékonyabb utat biztosít a piacra jutáshoz.
Az adatbázisok elismeréséről további információk az FDA Recognition of Public Human Genetic Variants Databases (Az emberi genetikai variánsok nyilvános adatbázisainak elismerése) című weboldalán találhatók.
Analitikai validációs útmutató
A “Considerations for Design, Development, and Analytical Validation of Next Generation Sequencing (NGS) – Based In Vitro Diagnostics (IVDs) Intended to Aid in the Diagnosis of Suspected Germline Diseases” című végleges útmutató ajánlásokat tesz az NGS-tesztek tervezéséhez, fejlesztéséhez és validálásához. Az iránymutatás ösztönzi továbbá a közösség részvételét az NGS-sel kapcsolatos szabványok kidolgozásában a szabványokat kidolgozó szervezetek (SDO-k) által, mivel a szabványok gyorsabban fejlődhetnek a technológia és a tudás változásával, és ezért megfelelő mérőszámok, például konkrét teljesítményküszöbök meghatározására használhatók az olyan gyorsan fejlődő területeken, mint az NGS.
FDA bioinformatikai platformja
Az FDA létrehozta a precisionFDA-t, egy felhőalapú közösségi kutatási és fejlesztési portált, amely világszerte bevonja a felhasználókat az adatok és eszközök megosztásába az NGS-feldolgozás meglévő és új bioinformatikai megközelítéseinek tesztelése, kísérleti alkalmazása és validálása érdekében. A genomikai közösségben dolgozó magánszemélyek és szervezetek további információkat találnak és regisztrálhatnak a részvételre a http://precision.fda.gov.
Kérdések?
Az FDA precíziós gyógyászati erőfeszítéseivel kapcsolatos kérdéseivel forduljon hozzánk a [email protected] címen.
Mit mondanak az FDA tisztviselői
- A FDA véglegesíti a megbízható fejlesztést felgyorsító iránymutatásokat, hasznos újgenerációs szekvenáláson alapuló tesztek gyorsabbá tételét
NGS Final Guidances
- Use of Public Human Genetic Variant Databases to Support Clinical Validity for Genetic and Genomic-Based In Vitro Diagnostics – Guidance for Stakeholders and Food and Drug Administration Staff (PDF – 444KB)
- Considerations for Design, Development, és analitikai validálása az újgenerációs szekvenáláson (NGS) alapuló, a feltételezett csíravonal-betegségek diagnózisának segítésére szánt in vitro diagnosztikák (IVD-k) tervezése és analitikai validálása – Útmutató az érdekeltek és az Élelmiszer- és Gyógyszerügyi Hivatal munkatársai számára (PDF. 869KB)
Beszámolók és vitairatok
- Optimizing FDA’s Regulatory Oversight of Next Generation Sequencing Diagnostic Tests (PDF – 424KB)
- Report: (archiválva)
Múlt ülések
- 07/27/16: Webinar – Next Generation Sequencing (NGS) Draft Guidances: Implikációk a betegekre és a szolgáltatókra
- 07/27/16: Webinar – Next Generation Sequencing (NGS) Draft Guidances: Technikai és szabályozási szempontok
- 2015.11.13: Nyilvános munkaértekezlet – Adatbázisok használata az emberi genetikai variánsok klinikai relevanciájának megállapításához
- 11/12/2015: Szabványokon alapuló megközelítés az újgenerációs szekvenálással végzett in vitro diagnosztikai tesztek analitikai teljesítményértékeléséhez
- 2015. 02. 20: Az FDA újgenerációs szekvenáló diagnosztikai tesztek szabályozási felügyeletének optimalizálása nyilvános munkaértekezlet