
A J-kapcsolás eredete egy egyszerű molekula, például a hidrogén-fluorid (HF) vektoros modelljével szemléltethető. A HF-ben a két atommag spinje 1/2. Négy állapot lehetséges, attól függően, hogy a H és F magspinek hogyan igazodnak egymáshoz a külső mágneses térrel. Az NMR-spektroszkópia kiválasztási szabályai szerint ΔI = 1, ami azt jelenti, hogy egy adott foton (a rádiófrekvenciás tartományban) a két magspin közül csak az egyikre hathat (“flip”).A J-kapcsolás három paramétert ad meg: a multiplicitást (a “vonalak számát”), a csatolás nagyságát (erős, közepes, gyenge) és a csatolás előjelét.
MultiplicityEdit
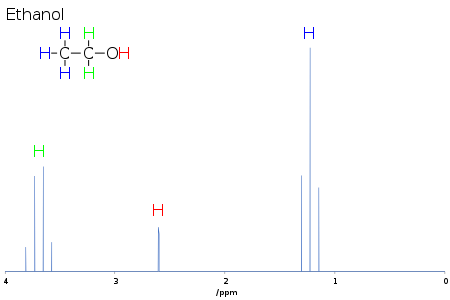
A multiplicitás információt nyújt a vizsgált jelhez kapcsolt centrumok számáról és azok nukleáris spinjéről. Egyszerű rendszerek esetén, mint például az NMR-spektroszkópiában az 1H-1H-kapcsolásnál, a multiplicitás eggyel több, mint a szomszédos protonok száma, amelyek mágnesesen nem egyenértékűek az érdeklődő protonokkal. Az etanol esetében minden metilproton a két metilénprotonhoz kapcsolódik, így a metiljel egy triplett. És minden metilénproton a három metilprotonhoz kapcsolódik, így a metilénjel kvartett.
A 1/2-nél nagyobb spinű atommagok, amelyeket kvadrupolárisnak nevezünk, nagyobb felhasadást eredményezhetnek, bár sok esetben a kvadrupoláris atommagokhoz való kapcsolódás nem figyelhető meg. Sok elem magspinnel rendelkező és magspinnel nem rendelkező atommagokból áll. Ezekben az esetekben a megfigyelt spektrum az egyes izotopomerek spektrumainak összege. A szerves molekulák NMR-spektroszkópiájának egyik nagy előnye, hogy számos fontos könnyebb, 1/2 spinű atommag vagy egyizotópos, pl. 31P és 19F, vagy nagyon nagy természetes gyakoriságú, pl. 1H. További könnyebbség, hogy a 12C és a 16O nem rendelkezik magspinnel, így ezek a szerves molekulákban gyakori atommagok nem okoznak hasadási mintázatot az NMR-ben.
A J-kapcsolás nagyságaSzerkesztés
Az 1H-1H-kapcsolás esetében a J nagysága információt nyújt a kapcsolási partnerek közelségéről. Általánosságban elmondható, hogy a kétkötéses csatolás (azaz 1H-C-1H) erősebb, mint a háromkötéses (1H-C-C-C-1H). A csatolás nagysága információt szolgáltat a csatolási partnerek közötti diéderes szögekről is, amint azt a háromkötéses csatolási állandókra vonatkozó Karplus-egyenlet leírja.
Heteronukleáris csatolás esetén a J nagysága a csatolási partnerek nukleáris mágneses nyomatékával függ össze. A nagy nukleáris mágneses nyomatékkal rendelkező 19F a protonokkal való nagymértékű csatolást eredményez. A 103Rh, amelynek nagyon kicsi a magmágneses nyomatéka, csak kis csatolásokat eredményez az 1H-val. A magmágneses nyomaték (vagy ennek megfelelően a γ gyromágneses arány) hatásának korrigálására gyakran beszélnek a K “redukált csatolási állandóról”, ahol
K = 4π2J/hγxγy.
Egy 13C atommag és egy közvetlenül kötött proton csatolásánál a JC-H csatolási állandóban a domináns kifejezés a Fermi-kontakt kölcsönhatás, amely a két atommagnál lévő kötés s-jellegének mértékegysége.
Ahol a külső mágneses tér nagyon alacsony, pl. mint a földi tér NMR, a hertzes nagyságrendű J-kapcsolási jelek általában dominálnak a millihertzes nagyságrendű, általában nem felbontható kémiai eltolódások felett.
A J-kapcsolás előjeleSzerkesztés
Az egyes csatolási állandók értékének előjele is van, és a hasonló nagyságú csatolási állandók gyakran ellentétes előjelűek. Ha két adott spin közötti csatolási állandó negatív, akkor a két spin párhuzamossága esetén kisebb az energia, és fordítva, ha a csatolási állandójuk pozitív. Egyetlen J-kapcsolási állandóval rendelkező molekula esetében az NMR-spektrum megjelenése nem változik, ha a kapcsolási állandó előjele megfordul, bár az adott pozíciókban lévő spektrális vonalak különböző átmeneteket képviselhetnek. Az egyszerű NMR-spektrum tehát nem jelzi a csatolási állandó előjelét, amelyet nem lehet egyszerűen megjósolni.
Néhány olyan molekula esetében azonban, amelynek két különböző J-kapcsolási állandója van, a két állandó relatív előjele kísérletileg meghatározható kettős rezonanciakísérlettel. Például a dietil-talliumion (C2H5)2Tl+ esetében ez a módszer kimutatta, hogy a metil-tallium (CH3-Tl) és a metilén-tallium (CH2-Tl) csatolási állandói ellentétes előjelűek.
A J-kapcsolási állandó abszolút előjelének meghatározására az első kísérleti módszert 1962-ben Buckingham és Lovering javasolta, akik erős elektromos tér alkalmazását javasolták egy poláris folyadék molekuláinak összehangolására. A mező a két spin közvetlen dipoláris csatolását idézi elő, ami hozzáadódik a megfigyelt J-kapcsoláshoz, ha az előjelük párhuzamos, és levonja a megfigyelt J-kapcsolást, ha az előjelük ellentétes. Ezt a módszert először a 4-nitrotoluolra alkalmazták, amely esetében a két szomszédos (vagy orto) gyűrűproton közötti J-kapcsolási állandó pozitívnak bizonyult, mivel a két csúcs felhasadása minden proton esetében csökken az alkalmazott elektromos térrel.
A molekulák NMR-spektroszkópiához való igazításának másik módja, hogy nematikus folyadékkristályos oldószerben oldjuk fel őket. Ezt a módszert használták a J-kapcsolási állandók abszolút előjelének meghatározására is.