-
 Bevezetés
Bevezetés - Hogyan hatnak a szerotonin blokkoló gyógyszerek?
- Milyen típusú szerotonin blokkoló gyógyszerek vannak?
- Első generációs szerotoninblokkolók
- Második generációs szerotoninblokkolók
- Milyen betegségek esetén alkalmazhatóak a szerotoninblokkoló gyógyszerek?
- Chemoterápia okozta hányinger és hányás (CINV)
- Sugárzás okozta hányinger és hányás (RINV)
- Posztoperatív hányinger és hányás (PONV)
- Milyen mellékhatásai vannak a szerotonin-blokkoló gyógyszerek alkalmazásának?
- A szerotonin-blokkoló gyógyszerek kölcsönhatásba lépnek más gyógyszerekkel?
- Bevezetés
- Hogyan hatnak a szerotonin-blokkoló gyógyszerek?
- Melyek a szerotonin-blokkoló gyógyszerek különböző típusai?
- Mire használják a szerotonin-blokkoló gyógyszereket?
- Milyen mellékhatásai lehetnek a szerotonin-blokkoló gyógyszerek alkalmazásának?
- A szerotonin-blokkoló gyógyszerek kölcsönhatásba lépnek más gyógyszerekkel?
- Bővebb információ
Bevezetés
Az 5-hidroxi-triptamin receptor antagonisták (5-HT3 RA-k) a hányinger és hányás kezelésére használt gyógyszerek csoportja. Nevüket onnan kapták, hogy képesek blokkolni az 5-hidroxi-triptamin (más néven szerotonin) működését a hányási reflexet kiváltó idegek aktiválásában. Az 5-HT3 RA-kat, vagy szerotoninblokkolókat eredetileg az 1990-es években fedezték fel, és a piacon lévő hányás elleni gyógyszerek egyik legújabb típusát jelentik. E gyógyszerek hatékonysága forradalmasította a hányinger és hányás kezelését, különösen a kemoterápiában vagy sugárterápiában részesülő egyéneknél, valamint a műtét utáni hányinger és hányás kezelésében.
Az Ausztráliában jelenleg öt szerotoninblokkolót forgalmaznak a kemoterápia okozta hányinger és hányás (CINV) kezelésére vagy megelőzésére, köztük a dolasetron (Anzemet), a granisetron (Kytril), az ondansetron (Zofran), a tropisetron (Navoban) és a palonosetron (Aloxi). Ezek a gyógyszerek úgy hatnak, hogy gátolják a szerotonin hatását az idegeken, amelyek a hányási impulzusokat továbbítják a belekből az agyba.
Az eltérő kémiai összetétel és az eltérő felszívódási profil ellenére a legtöbb gyógyszer ebben az osztályban egyformán hatékony. A fenti szerotoninblokkolók nagyon jól tolerálhatók, minimális mellékhatásokkal. Ezek a gyógyszerek általában biztonságosan szedhetők más vényköteles gyógyszerekkel együtt, de mindig bölcs dolog megbeszélni a lehetséges kölcsönhatásokat orvosával vagy gyógyszerészével, mielőtt két gyógyszert egyszerre szedne.
Hogyan hatnak a szerotonin-blokkoló gyógyszerek?
A hányingert és a hányingert egy összetett, több lépésből álló útvonal hozza létre. Végső soron ez az útvonal magában foglalja az agyban egy olyan terület aktiválódását, amelyet “hányásközpontnak” neveznek. Ez a központ felelős a testből érkező jelek koordinálásáért, feldolgozásáért és a hányási reflex aktiválásáért. A hányásközpont a gyomor és a torok mellett az agy különböző részeiből, többek között az egyensúlyközpontból is kap jeleket.
A hányásjelek továbbításáért felelős kémiai hírvivő a szerotonin (5-HT3). Ezt úgy teszi, hogy a gyomorban és az agyban található idegeken található receptorokhoz kötődik, amelyek az impulzusokat a hányásközpontba továbbítják.
A kemoterápia és a sugárterápia feltehetően a beleket bélelő sejtek károsítása révén váltja ki a hányást. Ezek a sejtek ekkor felszabadítják a bennük tárolt szerotonint, amely ezt követően olyan idegekhez kötődik, amelyek a gyomorból a hányást kiváltó impulzust továbbítják a hányásközpontba. Amint ez a jel eléri a hányásközpontot, a szerotonin aktiválja a hányási reflex aktiválásában részt vevő más idegeket.
A műtét utáni hányinger és hányás kevésbé jól ismert, de valószínűleg számos különböző tényező következménye, beleértve az alkalmazott érzéstelenítést, a műtét típusát és időtartamát, valamint az egyénhez kapcsolódó tényezőket. Ezek közül a legerősebb kockázati tényezőnek az altatószerek bizonyos típusait tartják.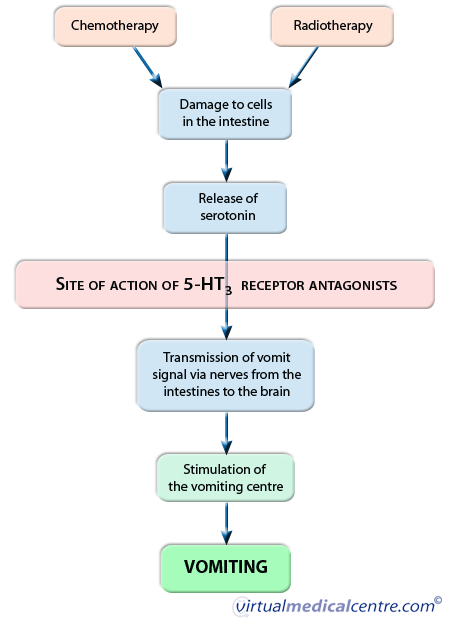
 |
A gyomorról, a torokról és a belekről bővebben lásd: A gyomor-bélrendszer anatómiája. |
Melyek a szerotonin-blokkoló gyógyszerek különböző típusai?
 Öt szerotonin-blokkolót forgalmaznak jelenleg Ausztráliában, köztük a dolasetron (Anzemet), a granisetron (Kytril), az ondansetron (Zofran), a tropisetron (Navoban) és a palonosetron (Aloxi). Az amerikai Élelmiszer- és Gyógyszerügyi Hivatal (FDA) által 2003-ban engedélyezett palonozetron a legújabb szerotonin-blokkoló, és második generációs hatóanyagnak tekinthető, mivel más kémiai szerkezete van, és a többi hatóanyagtól némileg eltérő módon hat.
Öt szerotonin-blokkolót forgalmaznak jelenleg Ausztráliában, köztük a dolasetron (Anzemet), a granisetron (Kytril), az ondansetron (Zofran), a tropisetron (Navoban) és a palonosetron (Aloxi). Az amerikai Élelmiszer- és Gyógyszerügyi Hivatal (FDA) által 2003-ban engedélyezett palonozetron a legújabb szerotonin-blokkoló, és második generációs hatóanyagnak tekinthető, mivel más kémiai szerkezete van, és a többi hatóanyagtól némileg eltérő módon hat.
Első generációs szerotonin-blokkolók
A dolasetron, granisetron, ondansetron és tropisetron az úgynevezett első generációs szerotonin-blokkolók. Annak ellenére, hogy eltérő a kémiai szerkezetük és a szervezetben való felszívódásuk, minden első generációs gyógyszer ugyanúgy működik és hasonló mellékhatásokkal rendelkezik.
Az első generációs szerotoninblokkolókkal kapcsolatban hatalmas mennyiségű kutatást végeztek, amelynek eredményeképpen a következő főbb pontokat állapították meg:
- A különböző szerotoninblokkolók egyformán hatékonyak, ezért felcserélhetők egymással;
- A gyógyszerek jól tolerálhatók és kevés mellékhatásuk van;
- A legkisebb napi egyszeri adagot kell alkalmazni, amely teljesen megelőzi a hányingert és a hányást; és
- A gyógyszer tablettás formája (orális forma) ugyanolyan hatékony a hányás megelőzésében, mint az intravénás forma.
Második generációs szerotoninblokkolók
A palonozetront 2003-ban hagyta jóvá az FDA második generációs szerotoninblokkolóként. Sokkal erősebben kötődik a receptorához, mint az első generációs gyógyszerek, ezért hosszabb ideig hat. Míg az első generációs gyógyszerek feltehetően csak a bélben lévő idegekhez kötődnek, a palonozetron feltehetően az agyban lévő receptorokhoz közvetlenül kötődve is hat.
A palonozetron az első gyógyszer, amelyet az FDA mind az akut, mind a késleltetett CINV megelőzésére jóváhagyott.
Mire használják a szerotonin-blokkoló gyógyszereket?
Chemoterápia okozta hányinger és hányás (CINV) A szerotonin-blokkoló gyógyszerek forradalmasították a CINV kezelését, és ezek a szerek ma már a hányás elleni terápia sarokkövét képezik ebben az állapotban. E gyógyszerek felfedezése előtt a hányás volt a kemoterápia legrettegettebb mellékhatása. A szerotoninblokkolók bevezetése óta a hányás a hányinger és a hajhullás után a harmadik legrettegettebb mellékhatássá vált.
A szerotonin-blokkoló gyógyszerek forradalmasították a CINV kezelését, és ezek a szerek ma már a hányás elleni terápia sarokkövét képezik ebben az állapotban. E gyógyszerek felfedezése előtt a hányás volt a kemoterápia legrettegettebb mellékhatása. A szerotoninblokkolók bevezetése óta a hányás a hányinger és a hajhullás után a harmadik legrettegettebb mellékhatássá vált.
A CINV-t akut, késleltetett, anticipatív, áttöréses vagy refrakter mellékhatásként lehet osztályozni aszerint, hogy mikor jelentkezik a kemoterápia beadásához képest.
A CINV a daganatos betegek 70-80%-át érinti, és jelentős hatással van az egyénre, valamint az egészségügyi erőforrásokra.
A CINV előfordulásának valószínűségét növelő tényezők nagyjából a gyógyszerrel kapcsolatos és az egyénhez kapcsolódó tényezőkre oszthatók. A gyógyszerekkel kapcsolatos kockázati tényezők közé tartozik, hogy a kemoterápiás szer milyen valószínűséggel vált ki hányást (“emetogenitása”), a gyógyszer dózisa és a gyógyszer bevételi módja (pl. szájon át vagy közvetlenül vénába injekciózva). Az egyénhez kapcsolódó kockázati tényezők közé tartozik az életkor, a nem, a korábbi kemoterápia, a terhességgel járó utazási betegség vagy hányinger, valamint az erős alkoholfogyasztás.
A kiterjedt kutatások eredményeként kidolgozott jelenlegi irányelvek a szerotoninblokkolók alkalmazását javasolják mind az akut, mind a késleltetett CINV kezelésében. Az erősen hányást kiváltó kemoterápiával járó akut hányinger és hányás megelőzésére egy szerotoninblokkoló, egy kortikoszteroid (például dexametazon) és egy P-anyag (NK-1) blokkoló (aprepitant) kombinációja ajánlott. Ezeket a szereket a kemoterápia megkezdése előtt kell adni.
A mérsékelten hányást kiváltó kemoterápiával járó akut CINV megelőzésére szerotoninblokkoló és dexametazon kombinációja ajánlott, P-szubsztanciablokkolóval vagy anélkül. Érdemes megjegyezni, hogy bár az olyan kortikoszteroidok, mint a dexametazon hasznos kiegészítő szerepet játszanak a hányás megelőzésében, jelentős mellékhatásaik vannak. Egy tanulmány szerint a mérsékelten hányást kiváltó kemoterápia miatt dexametazonban részesülő egyeseknél a kemoterápiát követő héten mérsékelt vagy súlyos álmatlanság, gyomorpanaszok vagy emésztési zavarok, nyugtalanság, fokozott étvágy, súlygyarapodás vagy pattanások jelentkeztek.
A palonozetron az előnyben részesített szerotoninblokkoló a mérsékelten hányást kiváltó kemoterápia utáni akut hányinger és hányás megelőzésére. A palonozetron egyszeri adagját a kemoterápia megkezdése előtt kell beadni, a 2. és 3. napon nincs szükség további adagolásra.
A legújabb irányelvek a vénába injektált palonozetron alkalmazását csak a kemoterápia 1. napján késleltetett CINV kezelésére javasolják. Ez az egyetlen szerotoninblokkoló, amely a késleltetett hányás kezelésére rendelkezésre áll. A palonoszetron további adagjainak hatása még nem teljesen ismert.
Onkológusa értékelni fogja az Ön kemoterápiás kezelését és az Ön sajátos kockázati tényezőit, mielőtt meghatározza, hogy mi a legjobb hányás elleni kezelés az Ön számára.
 |
A CINV-vel kapcsolatos további információkért lásd: Kemoterápia által kiváltott hányinger és hányás (CINV). |
Sugárzás által kiváltott hányinger és hányás (RINV) A sugárzás által kiváltott hányinger és hányás mechanizmusa ugyanaz, mint a CINV esetében. A statisztikák szerint a sugárterápiában részesülők 50-80%-a émelygést és/vagy hányást tapasztal. A RINV kialakulásának legnagyobb kockázata az egész testet vagy a gyomor felső részét érő sugárkezelésben részesülő egyéneknél áll fenn. A RINV kockázata a sugárterápia napi dózisának, a sugárterápia teljes dózisának és a sugárzásnak kitett testszövet mennyiségének növekedésével nő.
A sugárzás által kiváltott hányinger és hányás mechanizmusa ugyanaz, mint a CINV esetében. A statisztikák szerint a sugárterápiában részesülők 50-80%-a émelygést és/vagy hányást tapasztal. A RINV kialakulásának legnagyobb kockázata az egész testet vagy a gyomor felső részét érő sugárkezelésben részesülő egyéneknél áll fenn. A RINV kockázata a sugárterápia napi dózisának, a sugárterápia teljes dózisának és a sugárzásnak kitett testszövet mennyiségének növekedésével nő.
A RINV megelőzése attól függ, hogy a test mely részét fogják besugározni, és hogy a sugárkezelést kemoterápiával kombinálják-e vagy sem. Ha a sugárterápiát kemoterápiával kombinálják, a kemoterápiás gyógyszerek erősségének kell meghatároznia, hogy milyen hányáscsillapító gyógyszereket használnak. A szerotonin-blokkoló gyógyszerek az előnyben részesített hányáscsillapító gyógyszerek a RINV megelőzésére. A felső gyomor környékét és az egész felsőtestet érintő sugárkezelésben részesülő egyéneknek szerotoninblokkolót (ondansetron vagy granisetron) kell kapniuk kortikoszteroiddal (dexametazon) vagy anélkül.
Onkológusa értékelni fogja az Ön sugárterápiás kezelését és az Ön egyedi kockázati tényezőit, mielőtt meghatározza, hogy mi a legjobb hányás elleni kezelés az Ön számára.
Posztoperatív hányinger és hányás (PONV)
A hányás elleni gyógyszerek fejlődése ellenére a hányás és hányinger még mindig előfordul az egyének 20-30%-ánál műtét után. A PONV kialakulásának kockázati tényezői nagyjából az altatással kapcsolatosakra, az egyénnel kapcsolatosakra, valamint a műtét típusával és időtartamával kapcsolatosakra oszthatók.
A PONV megelőzésében és kezelésében erősen javasoltak a szerotonin-blokkoló gyógyszerek. A hányinger és hányás megelőzését ezeknél az egyéneknél a rizikófaktorok irányítják, amelyek az egyéneket a PONV kialakulásának magas, közepes vagy alacsony kockázatába csoportosítják. Azoknak az egyéneknek, akiknél a kockázati tényezők alapján közepes vagy magas a PONV kialakulásának kockázata, más hányás elleni gyógyszerek mellett szerotonin-blokkolót is kell kapniuk. A szerotonin-blokkoló gyógyszerek akkor hatnak a legjobban, ha a műtét végén adják őket.
A PONV-ben szenvedő személyek esetében, akik a műtét végén nem kaptak megelőző 5-HT3 RA adagot, a legjobb kezelés egy szerotonin-blokkoló gyógyszer kis adagja. Azokat a személyeket, akiknél a műtétet követő első 6 órán belül PONV alakul ki, a hányinger és hányás megelőzésére használt gyógyszertől eltérő osztályba tartozó gyógyszerrel kell kezelni. Azok a személyek, akiknél a műtét után több mint 6 órával PONV alakul ki, a dexametazon kivételével bármelyik hányás elleni gyógyszerrel kezelhetők.
A sebész vagy az aneszteziológus értékelni fogja az Ön egyedi kockázati tényezőit, mielőtt meghatározza, hogy mi a legjobb hányás elleni kezelés az Ön számára.
Milyen mellékhatásai lehetnek a szerotonin-blokkoló gyógyszerek alkalmazásának?
 A szerotonin-blokkoló gyógyszerek csoportját tekintve általában nagyon jól tolerálhatók, minimális, rövid távú mellékhatásokkal. A leggyakrabban tapasztalt mellékhatások a fejfájás, szédülés, gyomorfájás, székrekedés, fáradtság, a májműködés zavara és a szív elektromos vezetésének megváltozása. A granisetron tablettás formáját kapó egyénekkel végzett nagy vizsgálatban 15%-uknál jelentkezett fejfájás, 6%-uknál energiavesztés, 5%-uknál hasmenés, 5%-uknál túlzott álmosság és 7%-uknál székrekedés. A hányás elleni gyógyszerek más csoportjaitól eltérően a szerotonin-blokkoló gyógyszerekről nem mutatták ki, hogy neurológiai mellékhatásokat okoznának.
A szerotonin-blokkoló gyógyszerek csoportját tekintve általában nagyon jól tolerálhatók, minimális, rövid távú mellékhatásokkal. A leggyakrabban tapasztalt mellékhatások a fejfájás, szédülés, gyomorfájás, székrekedés, fáradtság, a májműködés zavara és a szív elektromos vezetésének megváltozása. A granisetron tablettás formáját kapó egyénekkel végzett nagy vizsgálatban 15%-uknál jelentkezett fejfájás, 6%-uknál energiavesztés, 5%-uknál hasmenés, 5%-uknál túlzott álmosság és 7%-uknál székrekedés. A hányás elleni gyógyszerek más csoportjaitól eltérően a szerotonin-blokkoló gyógyszerekről nem mutatták ki, hogy neurológiai mellékhatásokat okoznának.
A szív elektromos aktivitásának elektrokardiogramon (EKG) rögzített változásáról számoltak be ezzel a gyógyszercsoporttal kapcsolatban. A szívműködéssel kapcsolatos súlyos eseményeket azonban nem tulajdonítottak ennek a gyógyszercsoportnak. Amikor a szerotonin-blokkoló gyógyszerek alkalmazását megbeszéli orvosával, tájékoztassa őt minden korábbi vagy meglévő szívbetegségéről.
Ezeknek a gyógyszereknek a terhes vagy szoptató nőknél történő alkalmazásáról csak korlátozott információ áll rendelkezésre, ezért konzultáljon kezelőorvosával, ha teherbe kíván esni vagy szoptatni szeretne.
A szerotonin-blokkoló gyógyszerek kölcsönhatásba lépnek más gyógyszerekkel?
A csoportba tartozó gyógyszerek mindegyike ugyanazon a májban lévő útvonalon keresztül kerül feldolgozásra. Ez befolyásolhatja más, ugyanezt az útvonalat használó gyógyszerek felszívódását. Ez a kockázat nagyobb a kemoterápiában és sugárkezelésben részesülő egyéneknél, valamint a kórházi kezelésben részesülő egyéneknél. Bár ezek a kölcsönhatások potenciálisan befolyásolhatják más gyógyszerek felszívódását, ilyen esetekről nem számoltak be. Rendkívül fontos, hogy tájékoztassa kezelőorvosát minden szedett gyógyszeréről, hogy értékelni tudja az esetleges gyógyszerkölcsönhatások kockázatát.
Bővebb információ
 |
A hányingerről és hányásról, beleértve azt, hogy mi okozza, hogyan történik, a következményeket, valamint a kezelését és kezelését, lásd: Hányinger és hányás (emezis). |
 |
A gyógyszerekkel kapcsolatos további információkért, beleértve a farmakológiai bevezetést, a generikus és a márkás gyógyszerek összehasonlítását, valamint a gyógyszerlisták és a terhességi kategóriák jelentését, lásd: Gyógyszerek. |
- Gregory RE, Ettinger DS. 5-HT3 receptor antagonisták a kemoterápia okozta hányinger és hányás megelőzésére. Farmakológiájuk és klinikai hatékonyságuk összehasonlítása. Gyógyszerek. 1998;55(2):173-89.
- Hesketh PJ. Kemoterápia okozta hányinger és hányás. N Engl J Med. 2008;358(23):2482-94.
- de Boer-Dennert M, de Wit R, Schmitz PI, et al. Patient perceptions of the side-effects of chemotherapy: Az 5HT3 antagonisták hatása. Br J Cancer. 1997;76(8):1055-61.
- 5HT3 receptorok . Adelaide, SA: Australian Medicines Handbook; 2011. január . Elérhető: URL link
- Navari RM. A kemoterápia okozta hányinger és hányás farmakológiai kezelése: Fókuszban a legújabb fejlemények. Gyógyszerek. 2009;69(5):515-33.
- Rubenstein EB. Palonozetron: Az akut és késleltetett kemoterápia okozta hányinger és hányás megelőzésére javallt egyedülálló 5-HT3 receptor antagonista. Clin Adv Hematol Oncol. 2004;2(5):284-9.
- Dilly S. Granisetron (Kytril) klinikai biztonságossága és tolerálhatósága. Semin Oncol. 1994;21(3 Suppl 5):10-4.
- Baker PD, Morzorati SL, Ellett ML. A kemoterápia okozta hányinger és hányás patofiziológiája. Gastroenterol Nurs. 2005;28(6):469-80.
- Maricq AV, Peterson AS, Brake AJ, et al. Primary structure and functional expression of the 5HT3 receptor, a serotonin-gated ion channel. Science. 1991;254(5030):432-7.
- Kovac AL. A posztoperatív hányinger és hányás megelőzése és kezelése. Gyógyszerek. 2000;59(2):213-43.
-
Apfel CC, Kranke P, Katz MH, et al. Volatile anaesthetics may be the main cause of early but not delayed postoperative hányás: Egy randomizált, kontrollált, faktoriális felépítésű vizsgálat. Br J Anaesth. 2002;88(5):659-68.
- Billio A, Morello E, Clarke MJ. Szerotoninreceptor-antagonisták erősen emetogén kemoterápiában felnőtteknél. Cochrane Database Syst Rev. 2010;(1):CD006272.
- Jordan K, Sippel C, Schmoll HJ. Irányelvek a kemoterápia okozta hányinger és hányás antiemetikus kezelésére: Múlt, jelen és jövőbeli ajánlások. Onkológus. 2007;12(9):1143-50.
- Perwitasari DA, Gelderblom H, Atthobari J, et al. Anti-emetikus gyógyszerek az onkológiában: farmakológia és individualizáció farmakogenetikával. Int J Clin Pharm. 2011;33(1):33-43.
- Rittenberg CN. A kemoterápia okozta hányinger és hányás megelőzésének és kontrolljának következő generációja: Új 5-HT3 antagonista érkezik. Clin J Oncol Nurs. 2004;8(3):307-8, 310.
- Ettinger D, Armstrong K, Barbour S, et al. NCCN klinikai gyakorlati irányelvek az onkológiában: Antiemesis . Fort Washington, PA: National Comprehensive Cancer Care Network; 2011 . Elérhető: URL link
- Liau CT, Chu NM, Liu HE, et al. Incidence of chemotherapy-induced nausea and vomiting in Taiwan: Orvosok és ápolók becslése vs. a betegek által jelentett eredmények. Support Care Cancer. 2005;13(5):277-86.
- Lohr L. Kemoterápia okozta hányinger és hányás. Cancer J. 2008;14(2):85-93.
- Pollera CF, Giannarelli D. A ciszplatin által kiváltott hányást befolyásoló prognosztikai tényezők. Egy prediktív logisztikus modell meghatározása és validálása. Cancer. 1989;64(5):1117-22.
- Roila F, Herrstedt J, Aapro M, et al. Guideline update for MASCC and ESMO in the prevention of chemotherapy- and radiotherapy-induced nausea and vomiting: A perugiai konszenzuskonferencia eredményei. Ann Oncol. 2010;21(Suppl 5):v232-43.
- A heveny/késleltetett hányinger és hányás (emezis) megelőzése . Bethesda, MD: National Cancer Institute; 2011. március 16. . Elérhető: URL link
- Grunberg SM, Warr D, Gralla RJ, et al. Evaluation of new antiemetic agents and definition of antineoplastic agent emetogenicity – state of the art. Support Care Cancer. 2011;19(Suppl 1):S43-7.
- Vardy J, Chiew KS, Galica J, et al. A mérsékelten emetogén kemoterápiát követő késleltetett hányás megelőzésére alkalmazott dexametazon alkalmazásával kapcsolatos mellékhatások. Br J Cancer. 2006;94(7):1011-5.
- Salvo N, Doble B, Khan L, et al. A sugárzás okozta hányinger és hányás profilaxisa 5-hidroxi-triptamin-3 szerotonin receptor antagonistákkal: A randomizált vizsgálatok szisztematikus áttekintése. Int J Radiat Oncol Biol Phys. 2010 Nov 13.
- Cohen MM, Duncan PG, DeBoer DP, Tweed WA. A posztoperatív interjú: A hányinger és hányás kockázati tényezőinek felmérése. Anesth Analg. 1994;78(1):7-16.
-
Habib AS, Gan TJ. A posztoperatív hányinger és hányás bizonyítékokon alapuló kezelése: Egy áttekintés. Can J Anaesth. 2004;51(4):326-41.
- Gan TJ, Meyer T, Apfel CC, et al. Consensus guidelines for managing postoperative nausea and vomiting. Anesth Analg. 2003;97(1):62-71.
- Keefe DL. Az 5-HT(3) receptor antagonista antiemetikumok kardiotoxikus potenciálja: Van-e ok az aggodalomra? Onkológus. 2002(7):65-72.
- Aapro M, Blower P. 5-hidroxi-triptamin-3 típusú receptor antagonisták a kemoterápia és sugárterápia által kiváltott hányinger és hányás kezelésére: Lehet-e biztonságosan csökkenteni a beadott szerek dózisát? Cancer. 2005;104(1):1-18.
- Navari RM, Koeller JM. Az 5-hidroxi-triptamin3 receptor antagonisták elektrokardiográfiás és kardiovaszkuláris hatásai. Ann Pharmacother. 2003;37(9):1276-86.
-
Aapro M. Granisetron: A hányinger és hányás kezelésében való klinikai alkalmazásának aktualizálása. Onkológus. 2004;9(6):673-86.