- Aktivace satelitních buněk a zachování regeneračního potenciálu svalů po dlouhodobé denervaci
- Lithium moduluje hladiny miR-1906 extracelulárních vezikul odvozených z mezenchymálních kmenových buněk, které přispívají k neuroprotekci po cévní mozkové příhodě regulací toll-like receptoru 4
- Extracelulární vezikuly získané z fibroblastů podporují hojení ran optimalizací fibroblastových a endoteliálních buněčných funkcí
- Současné podávání endoteliálních a hladkých svalových buněk odvozených z lidských indukovaných pluripotentních kmenových buněk jako terapie kritické končetinové ischemie
Aktivace satelitních buněk a zachování regeneračního potenciálu svalů po dlouhodobé denervaci
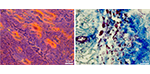
Alvin Wong, et al., STEM CELLS
Poškození pohybového nervu vede k atrofii koncových orgánů, která je trvalá, pokud je reinervace opožděná. Navzdory rozsáhlosti klinického problému je patofyziologie bránící obnově svalů málo známá. Autoři uvádějí, že i po delší době po poranění nervu si kmenové buňky v denervovaném svalu zachovávají regenerační schopnosti srovnatelné se schopnostmi nepoškozeného svalu. Tyto výsledky naznačují, že pozorování, že prodloužená denervace vede k trvalé svalové atrofii, není způsobeno vnitřní změnou regeneračního potenciálu svalových kmenových buněk, a naznačují, že úsilí o obnovení funkce by se mělo zaměřit na signály k vyvolání vnitřní regenerace a obnovení nervosvalové kontinuity.
Lithium moduluje hladiny miR-1906 extracelulárních vezikul odvozených z mezenchymálních kmenových buněk, které přispívají k neuroprotekci po cévní mozkové příhodě regulací toll-like receptoru 4

Matteo Haupt, et al., STEM CELLS Translational Medicine
Předkládaná práce poprvé poukazuje na zvýšený terapeutický potenciál extracelulárních vezikul (EV) odvozených z mezenchymálních kmenových buněk předem kondicionovaných lithiem proti mozkové ischemii. Tato práce objasňuje nový způsob působení takto obohacených EV a prokazuje zvýšené intravesikulární koncentrace vybraných miRNA, jako je miR-1906. Ta reguluje toll-like receptor 4 a známé prozánětlivé signální kaskády, což přispívá k lepšímu neurologickému zotavení po mrtvici. Hence, this work provides further and novel evidence for the therapeutic potential of EVs against stroke, paving the way for additional translational studies and clinical trials under stroke settings.
Extracelulární vezikuly získané z fibroblastů podporují hojení ran optimalizací fibroblastových a endoteliálních buněčných funkcí
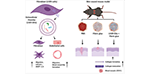
Eun Jung Oh, et al., STEM CELLS
Extracelulární vezikuly (EVs) byly zobrazeny jako schopní kandidáti pro doručování endogenních terapeutických cargo pro regenerativní terapie. Fibroblasty by mohly být kandidátskými zdrojovými buňkami pro EV, aby bylo možné zkoumat jejich terapeutické účinky při hojení ran. Podle nejlepšího vědomí autorů se jedná o první studii, která zkoumá in vitro účinky EVs vylučovaných myšími fibroblasty na hojení ran. Tato studie prokázala hojení ran o celé tloušťce pomocí myšího modelu a in vivo účinky hojení ran pomocí kombinace komerčně dostupného fibrinového lepidla a EVs vylučovaných fibroblasty.
Současné podávání endoteliálních a hladkých svalových buněk odvozených z lidských indukovaných pluripotentních kmenových buněk jako terapie kritické končetinové ischemie
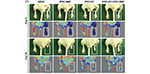
Jin Ju Park, et al., STEM CELLS Translational Medicine
Ischemická choroba je onemocnění periferních tepen, které se projevuje bolestí v klidu s nekrózami a vředy vedoucími k amputaci. Vzhledem ke schopnosti endoteliálních buněk a buněk hladkého svalstva cév regenerovat periferní tepny v ischemických tkáních představují buněčné terapie slibný prostředek k léčbě pacientů s ischemickou chorobou. Tato studie ukazuje, že kotransplantace endoteliálních buněk odvozených z indukovaných pluripotentních kmenových buněk a buněk hladkého svalstva zlepšuje krevní perfuzi a míru záchrany končetiny tím, že podporuje neovaskularizaci v ischemické končetině prostřednictvím parakrinního mechanismu zprostředkovaného exosomy odvozenými z buněk hladkého svalstva. Tato studie představuje novou techniku buněčné terapie pro léčbu periferních cévních onemocnění
.