-
 はじめに
はじめに - セロトニン遮断薬はどのように作用しますか
- セロトニン遮断薬にはどんな種類がありますか?
- 第一世代セロトニン遮断薬
- 第二世代セロトニン遮断薬
- セロトニン遮断薬はどんなことに使われるのですか?
- 化学療法に伴う悪心・嘔吐(CINV)
- 放射線に伴う悪心・嘔吐(RINV)
- 術後の悪心・嘔吐(PONV)
- セロトニン遮断薬の副作用はどの程度ありますか?
- セロトニン遮断薬は他の薬と相互作用しますか?
はじめに
5-hydroxytryptamine receptor antagonists(5-HT3 RAs)は、吐き気やおう吐を抑えるために使われる薬物群です。 5-HT3RAは、嘔吐反射を引き起こす神経を活性化する5-ヒドロキシトリプタミン(セロトニンとしても知られている)を阻害することから、その名前がつきました。 5-HT3 RA(セロトニンブロッカー)は、1990年代に発見された新しいタイプの嘔吐防止薬です。 これらの薬剤の有効性は、特に化学療法や放射線療法を受けている患者さんや、手術後の吐き気や嘔吐の治療において、吐き気や嘔吐の管理に革命をもたらしています。
現在オーストラリアでは、化学療法誘発性の悪心・嘔吐(CINV)の治療または予防を目的として、ドラセトロン(Anzemet)、グラニセトロン(Kytril)、オンダンセトロン(Zofran)、トロピセトロン(Navoban)、パロノセトロン(Aloxi)の5種類のセロトニンブロッカーが販売されています。 これらの薬は、腸から脳へ嘔吐のインパルスを伝える神経に作用するセロトニンの働きを阻害することによって作用する。
異なる化学組成と異なる吸収プロファイルを持つにもかかわらず、このクラスのほとんどの薬は同様に有効である。 上記のセロトニンブロッカーは、副作用が少なく、非常に忍容性が高い。 これらの薬は一般的に他の処方薬と一緒に服用しても安全ですが、2つの薬を同時に服用する前に、相互作用の可能性について医師または薬剤師に相談することが常に賢明です。
セロトニン遮断薬の作用は?
嘔吐と吐き気は、いくつかの段階を含む複雑な経路によってもたらされます。 最終的にこの経路は、脳内の「嘔吐中枢」と呼ばれる領域の活性化を伴います。 この領域は、体からの信号を調整し、処理し、嘔吐反射を活性化する役割を担っています。
セロトニン(5-HT3)は、嘔吐のシグナルを伝達する化学伝達物質であり、胃や喉に加え、平衡感覚中枢など脳のさまざまな部位からシグナルを受け取ります。 化学療法や放射線療法は、腸を覆う細胞を損傷させることで嘔吐を引き起こすと考えられています。 このセロトニンが神経に結合し、嘔吐を誘発するインパルスを胃から嘔吐中枢に伝達するのです。 この信号が嘔吐中枢に到達すると、セロトニンは嘔吐反射の活性化に関与する他の神経を活性化する。
手術後の吐き気および嘔吐についてはあまりよく分かっていないが、使用した麻酔薬、手術の種類および時間、個人関連因子など多くの異なる要因に起因すると思われる。 このうち、ある種の麻酔薬が最も強い危険因子と考えられています。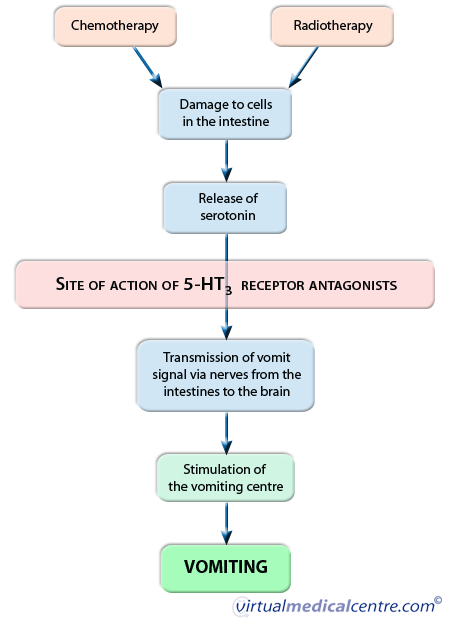
 |
胃、喉、腸の詳細については、消化器系の解剖をご覧下さい。 |
セロトニン遮断薬の種類は?
 現在オーストラリアでは、ドラセトロン(アンゼメット)、グラニセトロン(カイトリル)、オンダンセトロン(ゾフラン)、トロピセトロン(ナボバン)とパロノセトロン(アロキシ)、5つのセロトニン遮断薬が販売されています。 2003年に米国食品医薬品局(FDA)から承認されたパロノセトロンは、最も新しいセロトニン遮断薬で、化学構造が異なり、他の薬剤とはわずかに異なる方法で作用するため、第2世代の薬剤と考えられている。
現在オーストラリアでは、ドラセトロン(アンゼメット)、グラニセトロン(カイトリル)、オンダンセトロン(ゾフラン)、トロピセトロン(ナボバン)とパロノセトロン(アロキシ)、5つのセロトニン遮断薬が販売されています。 2003年に米国食品医薬品局(FDA)から承認されたパロノセトロンは、最も新しいセロトニン遮断薬で、化学構造が異なり、他の薬剤とはわずかに異なる方法で作用するため、第2世代の薬剤と考えられている。
第1世代のセロトニン遮断薬
ドラセトロン、グラニセトロン、オンダンセトロン、トロピセトロンは第1世代のセロトニン遮断薬と呼ばれ、その中でも、グラニセトロンは最も優れたセロトニン 遮断薬である。 化学構造や体内への吸収のされ方が異なるものの、第一世代の薬剤はすべて同じように作用し、副作用も似ています。
第一世代セロトニン遮断薬については、膨大な研究が行われた結果、以下のような重要なポイントが明らかになっています。
- 異なるセロトニン遮断薬は同等の効果があり、したがって互換的に使用できる;
- これらの薬は忍容性が高く、副作用はほとんどない;
- 吐き気やおう吐を完全に予防できる1日1回の最低量を使用すべきである;
- 薬の錠剤(経口剤)は静脈剤と同様におう吐予防に効果がある;などです。
第二世代セロトニンブロッカー
パロノセトロンは第二世代セロトニンブロッカーとして2003年にFDAに承認された。 第一世代の薬剤よりも受容体への結合力が強いため、より長い期間にわたって作用する。 第一世代の薬剤が腸の神経にのみ結合すると考えられているのに対し、パロノセトロンは脳の受容体にも直接結合して働くと考えられています。
パロノセトロンは、急性および遅発性CINVの予防薬としてFDAから承認された最初の薬剤です。
セロトニン遮断薬は何に使われるのか
化学療法誘発性悪心・嘔吐(CINV) セロトニン遮断薬はCINVの管理に革命を起こし、これらの薬剤が現在この症状における抗嘔吐療法の基礎となっている。 これらの薬剤が発見されるまでは、嘔吐は化学療法で最も恐れられていた副作用であった。 セロトニン遮断薬が導入されて以来、嘔吐は吐き気と脱毛に次いで3番目に恐れられている副作用になった。
セロトニン遮断薬はCINVの管理に革命を起こし、これらの薬剤が現在この症状における抗嘔吐療法の基礎となっている。 これらの薬剤が発見されるまでは、嘔吐は化学療法で最も恐れられていた副作用であった。 セロトニン遮断薬が導入されて以来、嘔吐は吐き気と脱毛に次いで3番目に恐れられている副作用になった。
CINVは、化学療法の投与との関連でいつ発生するかによって、急性、遅延、予期、破瓜、難治性に分類される。
CINVはがん患者の70~80%に影響を与え、個人および医療資源に大きな影響を及ぼす。
CINVを経験しやすくする要因は、薬剤関連因子と個人関連因子に大別される。 薬物関連のリスク因子には、化学療法剤が嘔吐を誘発する可能性(その「催吐性」)、薬剤の投与量、薬剤の服用方法(例、経口投与または静脈への直接注射)などがあります。 個人関連の危険因子には、年齢、性別、化学療法の経験、乗り物酔いまたは妊娠に伴う吐き気の既往、およびアルコールの大量使用歴が含まれる。
幅広い研究の結果として作成された現在のガイドラインでは、急性および遅発性CINVの治療においてセロトニン遮断薬の使用が提唱されている。 高度に嘔吐を誘発する化学療法による急性の吐き気および嘔吐の予防には、セロトニン遮断薬、コルチコステロイド(デキサメタゾンなど)、サブスタンスP(NK-1)遮断薬(アプレピタント)の併用が推奨される。 これらの薬物は化学療法の開始前に投与されるべきである。
中程度の嘔吐誘発性の化学療法による急性CINVの予防には、セロトニン遮断薬とデキサメタゾンの併用、サブスタンスP遮断薬の併用または非併用が推奨される。 デキサメタゾンなどのコルチコステロイドは、嘔吐の予防に有用な追加的役割を果たす一方で、重大な副作用を有することは注目に値します。 ある研究では、中等度の嘔吐を誘発する化学療法に対してデキサメタゾンを投与された一部の患者は、化学療法後の1週間に中等度から重度の不眠、胃の不快感または消化不良、激越、食欲増進、体重増加またはニキビを経験したとされた。
パロノセトロンは、中等度の嘔吐誘発性の化学療法後の急性吐き気および嘔吐を予防するために望ましいセロトニンブロッカーである。 最新のガイドラインでは、化学療法1日目の遅発性CINVの治療においてのみ、パロノセトロンの静脈内注射の使用が提唱されている。 これは、遅発性嘔吐の治療に利用可能な唯一のセロトニン遮断薬である。 パロノセトロンの追加投与による効果はまだ完全に分かっていない。
腫瘍医は化学療法レジメンと患者固有の危険因子を評価した上で、患者にとって最善の嘔吐防止治療が何かを決定することになる。
 |
放射線誘発性の吐き気および嘔吐(RINV) 放射線によって吐き気および嘔吐を引き起こす仕組みはCINVと同じで、放射線照射によって引き起こされた場合は、吐き気および嘔吐を誘発する可能性がある。 統計によると、放射線療法を受けた人の50-80%が吐き気および/または嘔吐を経験することになっています。 全身または胃の上部への放射線療法を受けた人は、RINVを発症するリスクが最も高くなります。 RINVのリスクは、放射線治療の1日当たりの線量、総線量、および放射線にさらされる身体組織の量が増えるにつれて高くなります。
放射線によって吐き気および嘔吐を引き起こす仕組みはCINVと同じで、放射線照射によって引き起こされた場合は、吐き気および嘔吐を誘発する可能性がある。 統計によると、放射線療法を受けた人の50-80%が吐き気および/または嘔吐を経験することになっています。 全身または胃の上部への放射線療法を受けた人は、RINVを発症するリスクが最も高くなります。 RINVのリスクは、放射線治療の1日当たりの線量、総線量、および放射線にさらされる身体組織の量が増えるにつれて高くなります。
RINVの予防は、身体のどの部分に放射線を当てるか、および放射線を化学療法と併用するかどうかによって異なります。 放射線療法が化学療法と併用される場合、化学療法薬の強さによって、どの嘔吐防止薬を使用するかを決定する必要がある。 RINVを予防するための抗嘔吐薬としては、セロトニン遮断薬が望ましいです。 胃の上部および上半身全体への放射線療法を受ける人は、セロトニン遮断薬(オンダンセトロンまたはグラニセトロン)と副腎皮質ホルモン(デキサメタゾン)の併用または併用なしの投与を受ける必要があります。
腫瘍医は放射線療法のレジメンと患者固有の危険因子を評価した上で、患者にとって最善の嘔吐防止治療法を決定します。
術後悪心・嘔吐(PONV)
抗嘔吐薬の開発にもかかわらず、術後の嘔吐と悪心は依然として患者の20~30%に認められます。 PONV発症の危険因子は、麻酔薬に関するもの、個人に関するもの、手術の種類と時間に関するものに大別される。
PONVの予防と治療には、セロトニン遮断薬が強く推奨される。 これらの患者における吐き気と嘔吐の予防は、個人をPONV発症の高リスク、中リスク、低リスクに分類する危険因子によって導かれる。 危険因子に基づいてPONVを発症するリスクが中程度または高い個人は、他の抗嘔吐薬に加えて、セロトニン遮断薬を投与する必要があります。 セロトニン遮断薬は手術終了時に投与するのが最も効果的です。
手術終了時に5-HT3 RAによる予防投与を受けなかったPONV患者にとって、最良の治療は少量のセロトニン遮断薬の投与となります。 手術後6時間以内にPONVを発症した人は、吐き気と嘔吐を予防するために使用した薬とは別のクラスの薬で治療する必要があります。 手術後6時間以上経過してPONVを発症した人は、デキサメタゾンを除いて、どの抗嘔吐薬でも治療できます。
外科医または麻酔科医は、患者固有の危険因子を評価して、患者にとって最善の抗嘔吐治療が何であるかを判断します。
セロトニン遮断薬の副作用は?
 グループとして、セロトニン遮断薬は一般的に非常に忍容性が高く、短期間の副作用はごくわずかです。 主な副作用は、頭痛、めまい、胃痛、便秘、疲労、肝機能障害、心臓の電気伝導の変化などです。 グラニセトロンの錠剤を投与された人を対象とした大規模な研究では、15%が頭痛を、6%が活力喪失を、5%が下痢を、5%が過度の眠気を、7%が便秘を経験したとされています。 他のクラスの嘔吐防止薬とは異なり、セロトニン遮断薬は神経系の副作用を引き起こすことは示されていません。
グループとして、セロトニン遮断薬は一般的に非常に忍容性が高く、短期間の副作用はごくわずかです。 主な副作用は、頭痛、めまい、胃痛、便秘、疲労、肝機能障害、心臓の電気伝導の変化などです。 グラニセトロンの錠剤を投与された人を対象とした大規模な研究では、15%が頭痛を、6%が活力喪失を、5%が下痢を、5%が過度の眠気を、7%が便秘を経験したとされています。 他のクラスの嘔吐防止薬とは異なり、セロトニン遮断薬は神経系の副作用を引き起こすことは示されていません。
このクラスの薬剤では、心電図(ECG)に記録される心臓の電気的活動に変化が生じることが報告されています。 しかし、心臓の活動に関連する重篤な事象は、この薬物群に起因するものではありません。
妊娠中または授乳中の女性におけるこれらの薬の使用に関する情報は限られており、妊娠または授乳の予定がある場合は医師に相談してください。
セロトニン遮断薬は他の薬と相互作用しますか?
このグループのすべての薬は肝臓で同じ経路を使って処理されます。 そのため、同じ経路を使う他の薬剤の吸収に影響を与える可能性があります。 このリスクは、化学療法や放射線療法を受けている人、入院している人でより大きくなります。 これらの相互作用は、他の薬剤の吸収に影響を与える可能性がありますが、そのような症例は報告されていません。
その他の情報
 |
吐き気と嘔吐について、原因、起こり方、結果、管理および治療などの詳しい情報は、吐き気と嘔吐(催吐)の項をご覧ください。 |
 |
薬理の紹介、後発医薬品と先発医薬品、薬剤スケジュールや妊娠分類の意味など、医薬品に関する詳細は、医薬品を参照してください。 |
- Gregory RE, Ettinger DS. 化学療法誘発性の吐き気と嘔吐の予防のための5-HT3受容体拮抗薬。 その薬理学と臨床効果の比較。 Drugs. 1998;55(2):173-89.
- Hesketh PJ. 化学療法による吐き気と嘔吐。 N Engl J Med. 2008;358(23):2482-94.
- de Boer-Dennert M, de Wit R, Schmitz PI, et al.化学療法の副作用に関する患者の認識。 5HT3 拮抗薬の影響。 Br J Cancer. 1997;76(8):1055-61.
- 5HT3 レセプター. Adelaide, SA: Australian Medicines Handbook; January 2011 . 利用可能な場所:URLリンク
- Navari RM. 化学療法誘発性の吐き気と嘔吐の薬理学的管理。 最近の動向を中心に。 Drugs. 2009;69(5):515-33.
- Rubenstein EB. パロノセトロン。 化学療法による急性および遅発性の悪心・嘔吐の予防を適応とするユニークな5-HT3受容体拮抗薬です。 Clin Adv Hematol Oncol. 2004;2(5):284-9.
- Dilly S. Granisetron (Kytril) clinical safety and tolerance. Semin Oncol. 1994;21(3 Suppl 5):10-4.
- Baker PD, Morzorati SL, Ellett ML. 化学療法誘発性悪心・嘔吐の病態生理。 Gastroenterol Nurs. 2005;28(6):469-80.
- Maricq AV, Peterson AS, Brake AJ, et al. セロトニン作動性イオンチャネル、5HT3受容体の一次構造と機能発現. Science. 1991;254(5030):432-7.
- Kovac AL. 術後の悪心・嘔吐の予防と治療. Drugs. 2000;59(2):213-43.
-
Apfel CC, Kranke P, Katz MH, et al. Volatile anaesthetics may be the main cause of early but not delayed postoperative vomiting.術後嘔吐の主な原因は揮発性麻酔薬かもしれない。 要因設計の無作為化比較試験。 Br J Anaesth 2002;88(5):659-68.
- Billio A, Morello E, Clarke MJ. 成人における催吐性の高い化学療法に対するセロトニン受容体拮抗薬。 Cochrane Database Syst Rev. 2010;(1):CD006272.
- Jordan K, Sippel C, Schmoll HJ. 化学療法誘発性の悪心・嘔吐の制吐療法に関するガイドライン。 過去、現在、そして将来の推奨事項。 Oncologist. 2007;12(9):1143-50.
- Perwitasari DA, Gelderblom H, Atthobari J, et al. 腫瘍科における制吐薬:薬理学と薬理遺伝学による個別化。 Int J Clin Pharm. 2011;33(1):33-43.
- リッテンバーグCN. 化学療法による悪心・嘔吐の予防と制御の次世代型。 新しい5-HT3アンタゴニストの登場です。 Clin J Oncol Nurs. 2004;8(3):307-8, 310.
- Ettinger D, Armstrong K, Barbour S, et al. NCCN clinical practice guidelines in oncology(腫瘍学における臨床実践ガイドライン)。 制吐剤. フォートワシントン、ペンシルベニア州。 全米包括的がん医療ネットワーク; 2011 . URLリンク
- Liau CT, Chu NM, Liu HE, et al. 台湾における化学療法による悪心・嘔吐の発生率。 医師および看護師の推定値と患者の報告値との比較。 サポートケアキャンサー。 2005;13(5):277-86.
- Lohr L. Chemotherapy-induced nausea and vomiting(化学療法による悪心・嘔吐)。 Cancer J. 2008;14(2):85-93.
- Pollera CF, Giannarelli D. シスプラチン誘発性嘔吐に影響する予後因子。 予測ロジスティックモデルの定義と検証。 Cancer. 1989;64(5):1117-22.
- Roila F, Herrstedt J, Aapro M, et al. 化学療法および放射線療法による吐き気と嘔吐の予防に関するMASCCおよびESMOのガイドラインの更新。 Perugia consensus conference の結果。 Ann Oncol. 2010;21(Suppl 5):v232-43.
- 急性/遅発性悪心・嘔吐(嘔吐)の予防. Bethesda, MD: National Cancer Institute; 16 March 2011 .
- Grunberg SM, Warr D, Gralla RJ, et al. 新しい制吐剤の評価と抗悪性腫瘍剤の催吐性の定義 – state of the art.より入手可能です。 Support Care Cancer. 2011;19(Suppl 1):S43-7.
- Vardy J, Chiew KS, Galica J, et al. 催吐性が中程度の化学療法後の遅発性嘔吐の予防のためのデキサメタゾンの使用に関連する副作用. Br J Cancer. 2006;94(7):1011-5.
- Salvo N, Doble B, Khan L, et al. 5-hydroxytryptamine-3セロトニン受容体拮抗薬を用いた放射線誘発性吐き気・嘔吐の予防法: 無作為化試験の系統的レビュー。 2010年11月13日。
- Cohen MM, Duncan PG, DeBoer DP, Tweed WA. 術後インタビュー。 吐き気・嘔吐の危険因子を評価する。 Anesth Analg. 1994;78(1):7-16.
-
Habib AS, Gan TJ. 術後の悪心・嘔吐のエビデンスに基づく管理。 レビュー。 2004;51(4):326-41.
- Gan TJ, Meyer T, Apfel CC, et al. 術後の吐き気と嘔吐を管理するためのコンセンサスガイドライン。 Anesth Analg. 2003;97(1):62-71.
- Keefe DL. 5-HT(3)受容体拮抗型制吐剤の心毒性の可能性。 懸念すべき点はあるか? Oncologist. 2002(7):65-72.
- Aapro M, Blower P. 化学療法および放射線療法による悪心・嘔吐に対する5-hydroxytryptamine type-3 receptor antagonists for chemotherapy-induced and radiotherapy-induced nausea and emesis(化学療法および放射線療法による悪心・嘔吐に対する3型受容体拮抗薬。 投与薬剤の量を安全に減らせるか? Cancer. 2005;104(1):1-18.
- Navari RM, Koeller JM. 5-hydroxytryptamine3受容体拮抗薬の心電図および心血管効果. Ann Pharmacother. 2003;37(9):1276-86.
-
Aapro M. Granisetron: 吐き気と嘔吐の管理におけるその臨床使用に関する最新情報。 Oncologist. 2004;9(6):673-86.