補酵素は酵素につながる小さな有機分子で、その存在は酵素の活性に不可欠である。 補酵素は、金属イオンも含む補因子と呼ばれる大きなグループに属し、補因子は、関連する酵素の活性に必要な小さな分子のより一般的な用語である。 この2つの用語の関係は次の通りである
I. 補酵素
- 必須イオン
- 疎結合(金属活性化酵素を形成)
- 密結合(金属酵素を形成) 補酵素
- 疎結合補基
多くの補酵素はビタミン類に由来している . 表1にビタミンとそれに由来する補酵素、それらが関与する反応の種類、および補酵素の種類を示す。
補酵素は酵素と強固に結合し、酵素の触媒サイクルに関与している。 他の触媒と同様に、酵素-置換基複合体は反応中に変化を受けるが、次の反応を触媒する前に、元の状態に戻らなければならない。
フラビンアデニンジヌクレオチド(FAD)は、細胞内のいくつかの酸化還元反応に関与する補欠基です。 コハク酸脱水素酵素の触媒サイクルにおいて、FADはコハク酸から2個の電子を受け取り、生成物としてフマル酸を得る。 FADは酵素に強く結合しているので、この反応は次のように示されることがある。
コハク酸 + E-FAD → フマル酸 + E-FADH 2
ここでE-FADはFAD補欠基と強く結合した酵素のことである。 この反応では補酵素FADはFADH 2に還元され、終始酵素に強固に結合したままである。 酵素が別のコハク酸分子の酸化を触媒する前に、E-FADH 2に属している2個の電子は、別の電子受容体であるユビキノンに移動させられなければならない。 再生されたE-FAD複合体は、次に別のコハク酸分子を酸化することができる。
共基質とは、酵素が化学量論的な量で必要とする、ゆるく結合した補酵素のことである。 ニコチンアミドアデニンジヌクレオチド(NAD)は、クエン酸サイクルの酵素の1つであるリンゴ酸脱水素酵素が触媒する酸化還元反応において副基質として作用している。
リンゴ酸+NAD+→オキサロ酢酸+NADH
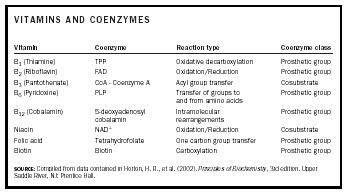
| ビタミンと補酵素 | |||
| ビタミン | 補酵素 | 反応型 | 補酵素クラス |
| SOURCE: Horton, H. R., et al.(2002)に含まれるデータから作成。 Principles of Biochemistry , 3rd edition. Upper Saddle River, NJ: Prentice Hall. | |||
| B 1(チアミン) | TPP | 酸化的脱炭酸 | 合成基 |
| B 1(チアミン B 2 (リボフラビン) | FAD | 酸化還元 | 合成基 |
| B 3 (パントテン酸) | CoA – CoA – CoA コエンザイムA | アシル基転移 | 共基質 |
| B 6(ピリドキシン) | PLP | 補欠基 | |
| B 12(コバラミン) | 5-.デオキシアデノシルコバラミン | 分子内転位 | 合成基 |
| ナイアシン | NAD + | 酸化・還元 | 共基質 |
| 葉酸 | テトラヒドロ葉酸 | 1つの炭素基の移動 | 合成基 |
| ビオチン | カルボキシル化 | 合成基 | |
本反応では。 リンゴ酸とNAD +は、リンゴ酸デヒドロゲナーゼの活性部位に拡散する。 ここでNAD +はリンゴ酸から2個の電子を受け取り、オキサロ酢酸とNADHは活性部位から拡散していく。 還元されたNADHは、NAD +の形に戻されなければならない。 各触媒サイクルにおいて、反応が起こるためには「新しい」NAD + 分子が必要であり、したがって、化学量論的量の副基質が必要である。 この補酵素の還元型(NADH)は、細胞内で同時に起こる多くのプロセスを経て、酸化型(NAD +)に戻され、再生されたNAD +は、次に別の触媒反応に参加することができます。
補酵素は補酵素の一種である。 酵素が触媒作用に参加する際に、酵素と強く(補欠基)またはゆるく(共基質)結合する小さな有機分子である。