Guanosine triphosphate (Guanosine-5′-triphosphate to be precise or also commonly abbremitted GTP for simplicity) is the high energy nucleotide ( nucleoside not to confuse with nucleoside) found in cytoplasm or polymerised into form guanine base.The グアニン塩基を形成するために細胞質で見いだし、グアノシン三リン酸と呼ばれる。
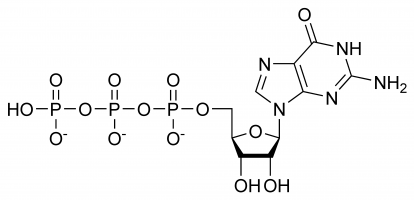
GTPは、RNA鎖の形成、タンパク質合成のエネルギー運搬分子としての機能、補酵素、cGMPの前身である二次伝道分子、エフェクター分子として選択的な役割を担っています。 最後の2つは、Gタンパク質の調節によって一般的に示される。 これらはすべて、複雑な三次元構造と、さまざまな化学基から構成されていることの結果である。 例えば、三リン酸だけが重合のためのエネルギー放出に関与し、グアニン塩基だけが脱アミノ化に関与しているように。 冒頭のリストは、その化学的相互作用を誇示しているのではなく、単にその様々な能力を示しているに過ぎないことに留意することが重要である。
GTPのリボース糖は、共有結合したグアニン分子と三リン酸分子の三次元的な配置の中心をなしています。 この単糖は縮合反応や求核攻撃のための水酸基を提供し、後者はRNA分子の破壊、ひいては遺伝子発現の調節に重要である。 グアニン分子はC’1、三リン酸はC’5で共有結合を形成するが、衝突を起こさない限り、他の水酸基を利用することも可能である。 プリン体から見ると、それまで水素原子と共有結合していた9’Nで縮合反応により結合している。 グアニンはプリン塩基であるため、アデニン三リン酸(ATP)と共にプリン三リン酸に分類され、イノシン一リン酸が修飾されて生成される。
Contents
- 1 誤信です。 GTP, A Baseline Building Block
- 2 多くのRNA塩基の前駆体の一つ
- 3 GTP; ATPの従兄弟
- 4 シグナルのリソース
- 5 References
Misconcept: GTPは、RNAの前駆体である。 GTP, A Baseline Building Block
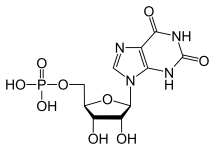
プリンおよびピラミジンヌクレオチドを合成する主要な臓器は肝臓である。 プリンヌクレオチド(GTPとATP)は、まずATP、グルタミン、グリシン、CO2、アスパラギン酸、ギ酸からイノシン一リン酸を作り合成される。 IMP
は、その後、いずれかの分子を得るために修飾されることができる。
GTPの生成の場合、IMPはまずIMPデヒドロゲナーゼによってXMPに変換される。 その結果、化学的および構造的変化が起こり、XMPをGMPに急速に変換するGTP合成酵素の作用が可能になります。 しかし、GMPは三リン酸を持たないため高エネルギー分子ではなく、ヌクレオシドリン酸キナーゼによってリン酸化され、まず二リン酸、最終的に三リン酸が生成される。
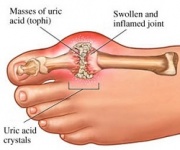
GTPは通常、不溶性の尿酸に分解され、尿酸ナトリウムの結晶として尿中に生成されます。 この過程が滑膜関節で起こると異常とみなされ、尿酸は有害な尿酸ナトリウムやピロリン酸カルシウム二水和物に変換されます。 このような化学物質が存在すると、炎症や関節炎が起こりやすくなり、その症状が複合して痛風という病気に分類されるのです。 プリンヌクレオチドの適切な異化の重要性を示すもう一つの例は、必須のBおよびTリンパ球の破壊をもたらす重症複合免疫不全症である
One Of Many RNA Base Predecesors
RNAとDNAにはいくつかの違いがあるが、第一の違いは各ポリマーを作る塩基の構造の違いである。 RNA の核酸塩基はリボース糖上に 2’OH 基を持ち、化学的反応性、触媒作用、不安定性が著しく高くなっています。 ここで重要なのは、グアノシン三リン酸はRNAのグアニン塩基の生成にのみ関与しているということである。 DNAのグアニン塩基を形成するためのGTPの類似体は、デオキシグアノシン三リン酸です。 この三リン酸は、
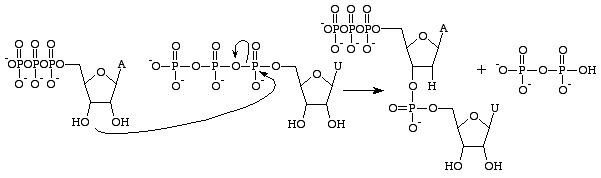
2’OH グループを持たないデオキシリボース糖で、核酸塩基間のリン酸ジエステル結合を切断する求核攻撃を防ぐため、非常に安定したものとなっています。 これは、RNA がタンパク質に翻訳された後に分解されるのに対して、DNA は娘細胞に遺伝情報を伝達するために無傷でなければならないので、理想的な状態です。
グアノシン三リン酸は、無水物結合が切断され、遊離リン酸としてαおよびγリン酸が放出される結果、グアニン塩基が形成されます。 その後、GMPは近くの3’OH基を持つ塩基とホスホジエステル結合を形成し、次のRNA塩基のための3’OH基を供給することになる。 この反応は、GMPの反対側の塩基がシトシンで、水素結合を形成できる場合にのみ起こり、RNAポリメラーゼによってその割合が増加する。 RNAポリメラーゼは三リン酸を整列させることはない。 RNAポリメラーゼは三リン酸を揃えるのではなく、それが単独で行われた後に起こる反応を触媒しているに過ぎない。 触媒作用の後、分子はポリヌクレオチド鎖の一部となり、もはやGTPとしてではなく、塩基グアニンとして知られるようになる。
GTP;ユニバーサルATPのいとこ
無水物結合の開裂からエネルギーを得るという基本的なメカニズムは、すべての三リン酸で同じである。 三リン酸の高エネルギー状態は、3つの異なるメカニズムによって達成される。 1つ目は、各リン酸基の反発力
に起因するものである。 これは結合した三リン酸の高い不安定性と、より低いエネルギー状態を実現するための高い「欲求」に寄与している。 第二は共鳴安定化によるものである。 GTPが
に変換されると、存在する電子対の可能な位置が増え、より安定性に寄与することになります。 この議論は、GDPをGMPに変換した場合にも当てはまります。 3 つ目は、リン酸塩の増加により、分子を取り囲む水分子のコンフォメーションに好ましくないエントロピー的な影響が生じるためです。
細胞質内のGTP濃度はATPよりも著しく低いため、細胞の代謝過程における特定の機能に利用される。
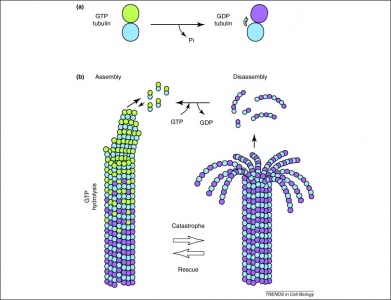
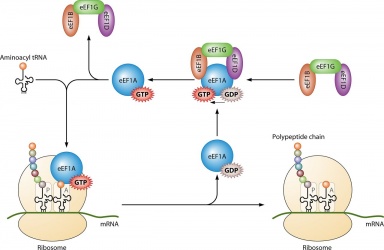
主な用途は、リボソーム開始時のIF2、伸長時のEf-TuとEf-G、終結時のRF3と結合して、タンパク質合成に利用されることです。 また、GTPはチューブリン二量体が微小管を形成する際にも利用される。 チューブリン二量体はアルファチューブリンとベータチューブリンからなり、それぞれがGTP結合部位を持つ。 ベータチューブリンはフィラメントのプラス端に存在するため、別の二量体が伸長ポリマーに加えられると、GTPは常にここで加水分解される。 重要なことは、GTPの加水分解によってチューブリン二量体間の非共有結合が弱まり、必要なときに微小管を分解しやすくなることである。 なお、αチューブリンタンパク質のGTPは脱リン酸化されないので、微小管構造全体を通じて一貫していると考えることができる。
A Resource for Signalling
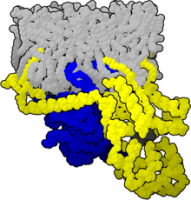
GTPの特異的化学構造と空間構造の利用は、シグナル伝達における利用によって効果的に証明されます。 主に、GTPは2つの異なるグループに分類される異なるシグナル伝達経路のタンパク質に結合し、その活性を制御することができます。 一つはヘテロ三量体GTP結合タンパク質(ヘテロ三量体Gタンパク質とも呼ばれる)で、Gタンパク質結合受容体の活性化時にGTPを利用し、経路上の他のタンパク質の活性を変化させるために利用される。 もう一つは、単量体GTP結合タンパク質(単量体Gタンパク質とも呼ばれる)である。 これらはGタンパク質共役型受容体以外の受容体に反応する。 典型的な例としては、Rasタンパク質が挙げられる。 なお、GTPはその特異的な化学的性質だけでなく、誘導適合現象により選択的に結合することができる。 結合したGTPは一定時間後に加水分解され、その結果、タンパク質は自動的に不活性化され、シグナル伝達経路が過剰に刺激されるのを防ぐことができます。 GTPが加水分解された後も、構造変化によってGTP分子とGDP分子との親和性が変化するため、GDPは結合したままとなる。 しかし、これは一時的な変化であり、その後Gタンパク質共役型受容体によって活性化されれば元に戻る。
GTPはまた、比較的一般的な二次シグナル分子であるcGMPを生成するための反応物質として使用されることがある。 cGMPは、特定のタンパク質をリン酸化し、その作用を変化させるプロテインキナーゼのエフェクターとして作用することができる。
- J Koolman and KH Roehm, Color Atlas of Biochemistry, 3rd Edition, Stuttgart, Germany. Thieme 2013.
- R K Murray, D A Bender, K M Botham, P J Kennelly, V W Rodwell and P A Weil. ハーパース イラストレイテッド バイオケミストリー. 第28版. 北京、中国。 2009.
- J Dow, G Lindsay and J Morrison, Biochemistry: 分子・細胞・身体. 第1版. イギリス、ウォーキンガム。 アディソン-ウェスリー。 1996.
- J Dow, G Lindsay and J Morrison, Biochemistry: 分子、細胞、そして身体。 第1版. イングランド、ウォーキンガム。 アディソン-ウェスリー。 1996.
- J Dow, G Lindsay and J Morrison, Biochemistry: 分子、細胞、そして身体。 第1版. イングランド、ウォーキンガム。 アディソン-ウェスリー。 1996.
- J Koolman and KH Roehm, Color Atlas of Biochemistry, 3rd Edition, Stuttgart, Germany.「生化学のカラーアトラス」.日本経済新聞社. Thieme 2013.
- J Koolman and KH Roehm, Color Atlas of Biochemistry, 3rd Edition, Stuttgart, Germany.ドイツ.ドイツ.日本経済新聞出版社.1996.
- M W King. 医学生物化学のページ。 2016年9月号 引用されました。 11:31. 03.12.2016. Available from: http://themedicalbiochemistrypage.org/nucleotide-metabolism.php#purine
- R K Murray, D A Bender, K M Botham, P J Kennelly, V W Rodwell and P A Weil. ハーパース イラストレイテッド バイオケミストリー. 第28版. 北京、中国。 2009.
- M・W・キング. メディカルバイオケミストリーのページ. 2016年9月号 引用されました。 11:31. 03.12.2016. 配信元: http://themedicalbiochemistrypage.org/nucleotide-metabolism.php#purine
- M W King. メディカルバイオケミストリーのページです。 2016年9月号 引用されました。 11:31. 03.12.2016. 配信元: http://themedicalbiochemistrypage.org/nucleotide-metabolism.php#purine
- M W King. メディカルバイオケミストリーのページです。 2016年9月号 引用されました。 11:31. 03.12.2016. 配信元: http://themedicalbiochemistrypage.org/nucleotide-metabolism.php#purine
- M W King. メディカルバイオケミストリーのページです。 2016年9月号 引用されました。 11:31. 03.12.2016. 引用元: http://themedicalbiochemistrypage.org/nucleotide-metabolism.php#purine
- J Dow, G Lindsay and J Morrison, Biochemistry: 分子・細胞・身体. 第1版. イギリス、ウォーキンガム。 アディソン-ウェスリー。 1996.
- J Dow, G Lindsay and J Morrison, Biochemistry: 分子、細胞、そして身体。 第1版. イングランド、ウォーキンガム。 アディソン-ウェスリー。 1996.
- J Dow, G Lindsay and J Morrison, Biochemistry: 分子、細胞、そして身体。 第1版. イングランド、ウォーキンガム。 アディソン-ウェスリー。 1996.
- J Koolman and KH Roehm, Color Atlas of Biochemistry, 3rd Edition, Stuttgart, Germany. Thieme 2013.
- J M Berg, J L Tymoczko, G J Gatto and R Stryer. 生化学. 第8版. 都市・国名未定。 フリーマン・アンド・カンパニー 2015.
- J M Berg, J L Tymoczko, G J Gatto and R Stryer. バイオケミストリー. 第8版. 市町村不詳。 フリーマン・アンド・カンパニー 2015.
- J M Berg, J L Tymoczko, G J Gatto and R Stryer. バイオケミストリー. 第8版. 市町村不詳。 Freeman and Co. 2015.
- T E Dever and R Green. 真核生物の伸長期・終結期・リサイクル期. CSHPB. 2012年7月号 4:7:1-16
- B Alberts et al. モレキュラー・バイオロジー・オブ・ザ・セル. 第6版. アメリカ、ニューヨーク。 ガーランド・サイエンス. 2015.
- B アルバーツ. Molecular Biology of The Cell. 第6版. アメリカ、ニューヨーク。 ガーランド・サイエンス. 2015.
- J Koolman and KH Roehm, Color Atlas of Biochemistry, 3rd Edition, Stuttgart, Germany.日本経済新聞社. Thieme 2013.
- J Koolman and KH Roehm, Color Atlas of Biochemistry, 3rd Edition, Stuttgart, Germany. Thieme 2013.
- J Koolman and KH Roehm, Color Atlas of Biochemistry, 3rd Edition, Stuttgart, Germany. Thieme 2013.
- J Koolman and KH Roehm, Color Atlas of Biochemistry, 3rd Edition, Stuttgart, Germany. Thieme 2013.
、KH Roehm, Color Atlas of Biochemistry, 3rd Edition, Stuttgart, Germany. Thieme 2013.
から検索した。