Koentsyymit ovat pieniä orgaanisia molekyylejä, jotka liittyvät entsyymeihin ja joiden läsnäolo on olennaista näiden entsyymien toiminnalle. Koentsyymit kuuluvat suurempaan ryhmään nimeltä kofaktorit, johon kuuluvat myös metalli-ionit; kofaktori on yleisempi termi pienille molekyyleille, joita tarvitaan niihin liittyvien entsyymien toimintaan. Näiden kahden termin välinen suhde on seuraava
I. Kofaktorit
- Välttämättömät ionit
- Löyhästi sidotut (muodostavat metalliaktivoituja entsyymejä)
- Tiiviisti sidotut (muodostavat metallientsyymejä
- Koentsyymit
- Tiiviisti sidotut proteettiset ryhmät
- 2 Löyhästi sidotut koentsyymiyhdisteytykset
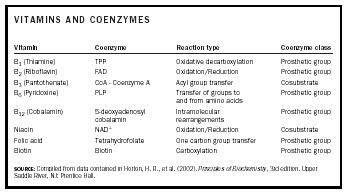
Useat koentsyymit ovat peräisin vitamiineista . Taulukossa 1 luetellaan vitamiinit, niistä johdetut koentsyymit, reaktiotyyppi, johon ne osallistuvat, ja koentsyymiluokka.
Proteiiniryhmät ovat tiukasti sidoksissa entsyymeihin ja osallistuvat entsyymien katalyyttisiin sykleihin. Kuten mikä tahansa katalyytti , entsyymi-proteettisen ryhmän kompleksi muuttuu reaktion aikana, mutta ennen kuin se voi katalysoida toista reaktiota, sen on palattava alkuperäiseen tilaansa.
Flaviiniadeniinidinukleotidi (FAD) on proteettinen ryhmä, joka osallistuu useisiin solunsisäisiin hapetus-pelkistysreaktioihin. Sukkinaattidehydrogenaasientsyymin katalyyttisen syklin aikana FAD ottaa kaksi elektronia sukkinaatista, jolloin tuotteena on fumaraatti. Koska FAD on tiukasti sidottu entsyymiin, reaktio esitetään joskus näin
sukkinaatti + E-FAD → fumaraatti + E-FADH 2
missä E-FAD tarkoittaa entsyymiä, joka on tiukasti sidottu FAD-proteettiseen ryhmään. Tässä reaktiossa koentsyymi FAD pelkistyy FADH 2:ksi ja pysyy koko ajan tiukasti sidottuna entsyymiin. Ennen kuin entsyymi voi katalysoida toisen sukkinaattimolekyylin hapettumista, E-FADH 2:een nyt kuuluvat kaksi elektronia on siirrettävä toiselle elektroniakseptorille, ubikinonille. Uudelleen muodostunut E-FAD-kompleksi voi sitten hapettaa toisen sukkinaattimolekyylin.
Kosubstraatit ovat löyhästi sitoutuneita koentsyymejä, joita entsyymit tarvitsevat stoikiometrisiä määriä. Nikotiiniamidi-adeniinidinukleotidimolekyyli (NAD) toimii kosubstraattina hapetus-pelkistysreaktiossa, jota katalysoi malaattidehydrogenaasi, yksi sitruunahappokierron entsyymeistä.
malaatti + NAD + → oksaloasetaatti + NADH
| VITAMIINIT JA KOENSIYMIT | |||||||
| Vitamiini | Koentsyymi | Reaktiotyyppi | Koentsyymiluokka | ||||
| LÄHTEET: Horton, H. R., et al. (2002). Principles of Biochemistry , 3. painos. Upper Saddle River, NJ: Prentice Hall. | |||||||
| B 1 (Tiamiini) | TPP | Oksidatiivinen dekarboksylaatio | Proteettinen ryhmä | ||||
| B 2 (Riboflaviini) | FAD | Hapetus/reduktio | Proteettinen ryhmä | ||||
| B 3 (Pantotenaatti) | CoA – – Koentsyymi A | Asyyliryhmän siirto | Kosubstraatti | ||||
| B 6 (Pyridoksiini) | PLP | Ryhmien siirto aminohapoille ja aminohapoista | Proteettinen ryhmä | ||||
| B 12 (kobalamiini) | 5-deoksiadenosyylikobalamiini | Intramolekulaariset uudelleenjärjestelyt | Proteettinen ryhmä | ||||
| Niasiini | NAD + | Hapetus/reduktio | Kosubstraatti | ||||
| Foolihappo | Tetrahydrofolaatti | Yhden hiiliryhmän siirto | Karboksylaatio | Karboksylaatio | Karboksylaatio | Karboksylaatio | Karboksylaatioryhmän siirto |
Tässä reaktiossa, malaatti ja NAD + diffundoituvat malaattidehydrogenaasin aktiiviseen kohtaan. Tässä NAD + ottaa kaksi elektronia malaatista; oksaloasetaatti ja NADH diffundoituvat sitten ulos aktiivisesta kohdasta. Pelkistynyt NADH on sitten palautettava NAD + -muotoonsa. Jokaista katalyyttistä sykliä varten tarvitaan ”uusi” NAD + -molekyyli, jotta reaktio tapahtuisi; näin ollen tarvitaan stoikiometrinen määrä yhteissubstraattia. Tämän koentsyymin pelkistynyt muoto (NADH) muunnetaan takaisin hapettuneeseen muotoon (NAD + ) useiden samanaikaisesti solussa tapahtuvien prosessien kautta, ja uusiutunut NAD + voi sitten osallistua uuteen katalyysikierrokseen.
Koentsyymit ovat siis eräänlainen kofaktori. Ne ovat pieniä orgaanisia molekyylejä, jotka sitoutuvat tiukasti (proteettiset ryhmät) tai löyhästi (kosubstraatit) entsyymeihin niiden osallistuessa katalyysiin.