
Kirjoita esimerkkisi tähän.
- 9.1 Signaalimolekyylit ja solureseptorit
- 9.2 Signaalin leviäminen
- 9.3 Vastaus signaaliin
Kuvittele, millaista elämä olisi, jos sinä ja ympärilläsi olevat ihmiset eivät voisi kommunikoida. Et pystyisi ilmaisemaan toiveitasi muille, etkä voisi esittää kysymyksiä saadaksesi lisätietoja ympäristöstäsi. Yhteiskunnallinen järjestäytyminen on riippuvainen yhteiskunnan muodostavien yksilöiden välisestä kommunikaatiosta.
Aivan kuten ihmisten kohdalla, myös yksittäisten solujen on elintärkeää pystyä olemaan vuorovaikutuksessa ympäristönsä ja toistensa kanssa. Tämä pätee riippumatta siitä, kasvaako solu yksinään lammessa vai onko se yksi monista soluista, jotka muodostavat suuremman organismin. Jotta solut voisivat reagoida asianmukaisesti ulkoisiin ärsykkeisiin, ne ovat kehittäneet monimutkaisia viestintämekanismeja, jotta ne voivat vastaanottaa viestin, siirtää tiedon plasmakalvon läpi ja sitten tuottaa muutoksia solun sisällä vastauksena viestiin.
Monisoluisissa eliöissä solut lähettävät ja vastaanottavat jatkuvasti kemiallisia viestejä koordinoidakseen muiden elinten, kudosten ja solujen toimintaa. Kyky lähettää viestejä nopeasti ja tehokkaasti antaa soluille mahdollisuuden koordinoida ja hienosäätää toimintojaan. Vaikka soluviestinnän tarpeellisuus suuremmissa eliöissä vaikuttaa ilmeiseltä, myös yksisoluiset eliöt kommunikoivat keskenään. Hiivasolut viestittävät toisilleen parittelun helpottamiseksi. Jotkin bakteerimuodot koordinoivat toimintaansa muodostaakseen suuria komplekseja, joita kutsutaan biokalvoiksi, tai organisoidakseen myrkkyjen tuotantoa kilpailevien organismien poistamiseksi. Solujen kyky kommunikoida kemiallisten signaalien välityksellä sai alkunsa yksittäisistä soluista, ja se oli välttämätöntä monisoluisten organismien kehittymiselle. Tehokas ja virheetön viestintä on elintärkeää kaikelle elämälle.
- 9.1 | Signaalimolekyylit ja solureseptorit
- 9.1.1 Signaloinnin muodot
- Parakriininen signalointi
- Autokriininen signalointi
- Endokriininen signalointi
- Suora signalointi
- 9.1.2 Reseptorityypit
- Sisäiset reseptorit
- Solupinnan reseptorit
- 9.1.3 Signaalimolekyylit
- Pienet hydrofobiset ligandit
- Vesiliukoiset ligandit
- 9.2 | Signaalin leviäminen
- 9.2.1 Signaalireitit ja signaalin vahvistaminen
- 9.2.2 Solunsisäisen signaloinnin menetelmät
- Fosforylaatio
- Sekundaariset sanansaattajat
- 9.3 | Vastaus signaaliin
- 9.3.1 Signaalireitin vasteet
- Geeniekspressio
- Solun aineenvaihdunnan lisääntyminen
- Solujen kasvu
- Solukuolema
- 9.3.2 Signaalireittien lopettaminen
9.1 | Signaalimolekyylit ja solureseptorit
Tämän jakson lopussa osaat:
- Kuvailla neljää monisoluisissa eliöissä esiintyvää signalointia.
- Vertailla sisäisiä reseptoreita solupinnan reseptoreihin.
- Tunnistaa ligandin kemian ja sen vaikutusmekanismin välisen suhteen.
Elävien solujen maailmassa on kahdenlaista viestintää. Solujen välistä viestintää kutsutaan solujenväliseksi signaloinniksi ja solun sisäistä viestintää solunsisäiseksi signaloinniksi. Helppo tapa muistaa ero on ymmärtää, että etuliite inter- tarkoittaa ”välillä” (osavaltioiden välinen moottoritie kulkee osavaltioiden välillä) ja intra- tarkoittaa ”sisällä” (infuusio tarkoittaa laskimonsisäistä tai ”suonen sisällä”).
Kemiallisia signaaleja vapautuu signaloivasta solusta ja kohdesolu vastaanottaa ne. Kohdesoluilla on reseptoreiksi kutsuttuja proteiineja, jotka sitoutuvat signaalimolekyyleihin ja aiheuttavat vasteen. Reseptoreihin sitoutuvia signaalimolekyylejä kutsutaan ligandeiksi. Ligandit ja reseptorit ovat spesifisiä toisilleen; reseptori sitoutuu yleensä vain tiettyyn ligandiinsa. On kuitenkin olemassa erityyppistä signalointia.
9.1.1 Signaloinnin muodot
Monisoluisissa eliöissä esiintyy neljää kemiallisen signaloinnin kategoriaa: autokriininen signalointi, parakriininen signalointi, endokriininen signalointi ja suora signalointi aukkoliitosten kautta (kuva 9.2). Merkittävin ero eri signalointikategorioiden välillä on matka, jonka signaali kulkee saavuttaakseen kohdesolun.
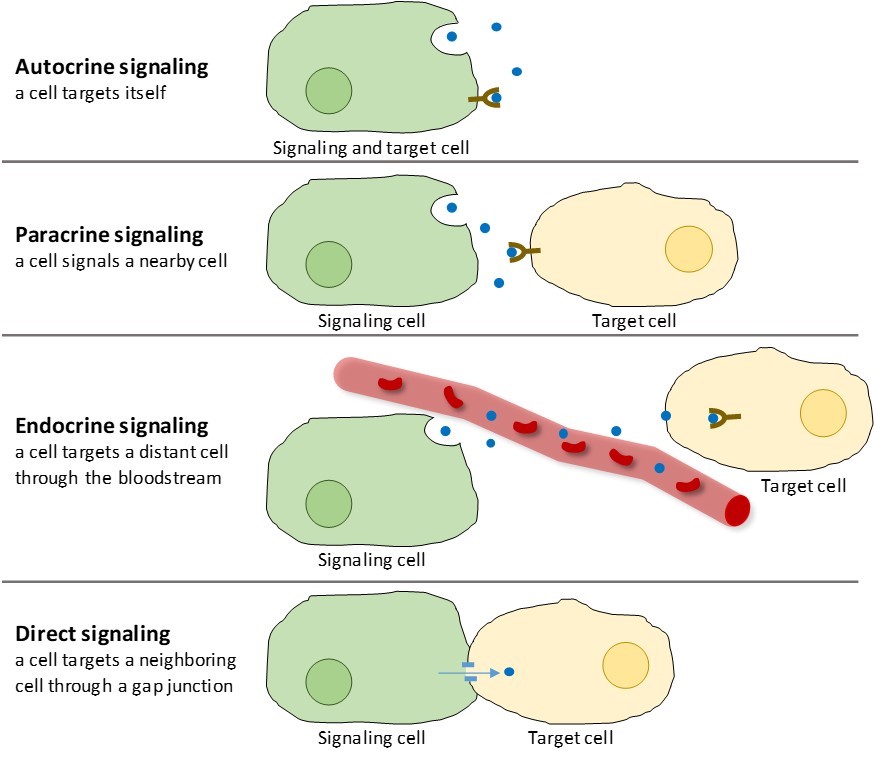
Parakriininen signalointi
Signaaleja, jotka vaikuttavat paikallisesti lähellä toisiaan olevien solujen välillä, sanotaan parakriinisiksi signaaleiksi. Parakriiniset signaalit liikkuvat diffuusiolla solunulkoisen matriksin läpi (kuva 9.2). Tämäntyyppiset signaalit saavat yleensä aikaan nopeita vasteita, jotka kestävät vain lyhyen aikaa. Jotta vaste pysyisi paikallisena, parakriiniset ligandit yleensä hajoavat nopeasti entsyymien avulla tai naapurisolut poistavat ne. Signaalien poistaminen palauttaa signaalimolekyylin konsentraatiogradientin, jolloin ne diffundoituvat nopeasti solunsisäisen tilan läpi, jos niitä vapautuu uudelleen.
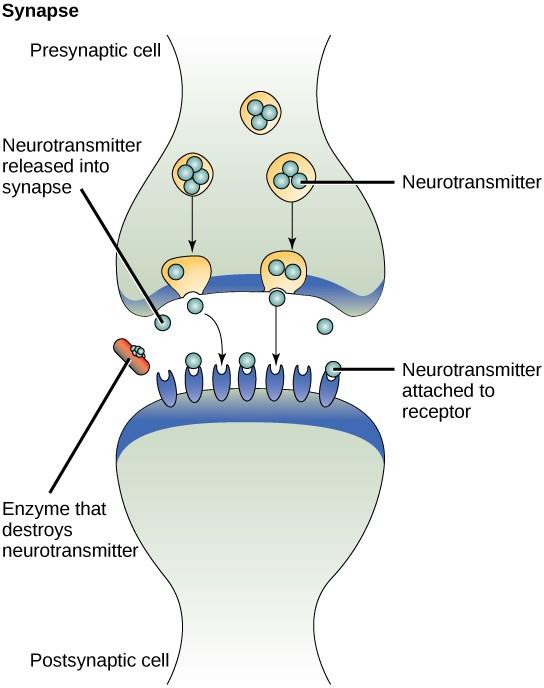
Yksi esimerkki parakriinisestä signaloinnista on signaalien siirtyminen hermosolujen välillä. Hermosolujen välistä pientä tilaa, jossa signaalinsiirto tapahtuu, kutsutaan synapsiksi. Signaalit etenevät hermosoluja pitkin nopealiikkeisinä sähköimpulsseina. Kun nämä impulssit saavuttavat yhden hermosolun pään, presynaptinen solu (signaalin lähettänyt solu) vapauttaa synapsiin kemiallisia ligandeja, joita kutsutaan neurotransmittereiksi. Neurotransmitterit diffundoituvat synapsiin (kuva 9.3). Hermosolujen välinen pieni etäisyys mahdollistaa signaalin nopean kulkeutumisen, mikä mahdollistaa välittömän reaktion, kuten ”ota käsi pois liedeltä!”. Kun välittäjäaine sitoutuu postsynaptisen solun pinnalla olevaan reseptoriin, seuraava sähköinen impulssi käynnistyy. Neurotransmitterit hajoavat nopeasti tai imeytyvät takaisin presynaptiseen soluun, jotta vastaanottajahermosolu voi toipua nopeasti ja valmistautua reagoimaan nopeasti seuraavaan synaptiseen signaaliin.
Autokriininen signalointi
Kun solu reagoi omaan signaalimolekyyliinsä, sitä kutsutaan autokriiniseksi signaloinniksi (auto = ”itse”). Autokriininen signalointi esiintyy usein yhdessä muun tyyppisen signaloinnin kanssa. Esimerkiksi kun parakriininen signaali vapautuu, signaloiva solu voi reagoida signaaliin yhdessä naapureidensa kanssa (kuva 9.2).
Autokriininen signalointi tapahtuu usein organismin varhaiskehityksen aikana sen varmistamiseksi, että solut kehittyvät oikeiksi kudoksiksi. Autokriininen signalointi säätelee myös kipuaistimusta ja tulehdusreaktioita. Lisäksi jos solu saa virusinfektion, solu voi signaloida itselleen ohjelmoidun solukuoleman ja tappaa samalla viruksen.
Endokriininen signalointi
Kauempana sijaitsevista soluista tulevia signaaleja kutsutaan endokriinisiksi signaaleiksi, ja ne ovat peräisin endokriinisistä soluista. (Kehossa monet hormonaaliset solut sijaitsevat hormonaalisissa rauhasissa, kuten kilpirauhasessa, hypotalamuksessa ja aivolisäkkeessä). Tämäntyyppiset signaalit tuottavat yleensä hitaamman vasteen, mutta niiden vaikutus kestää kauemmin. Endokriinisessä signaloinnissa vapautuvia ligandeja kutsutaan hormoneiksi, signaalimolekyyleiksi, joita tuotetaan yhdessä kehon osassa mutta jotka vaikuttavat muihin kehon alueisiin jonkin matkan päässä (kuva 9.2).
Hormonit kulkevat hormonisolujen ja niiden kohdesolujen väliset suuret etäisyydet verenkierron välityksellä, joka on suhteellisen hidas tapa liikkua elimistössä. Kuljetusmuotonsa vuoksi hormonit laimenevat ja ovat pieninä pitoisuuksina läsnä, kun ne vaikuttavat kohdesoluihinsa. Tämä eroaa parakriinisestä signaloinnista, jossa signaalimolekyylien paikalliset pitoisuudet voivat olla hyvinkin korkeita.
Suora signalointi
Eläimillä rakokytkennät ja kasveilla plasmodesmat ovat naapurisolujen plasmakalvojen välisiä yhteyksiä. Nämä vedellä täytetyt kanavat mahdollistavat pienten signaalimolekyylien diffuusion kahden solun välillä. Pienet molekyylit, kuten kalsiumionit (Ca2+), pystyvät liikkumaan solujen välillä, mutta suuret molekyylit, kuten proteiinit ja DNA, eivät mahdu kanavien läpi. Kanavien spesifisyys varmistaa, että solut pysyvät itsenäisinä, mutta pystyvät välittämään signaaleja nopeasti ja helposti. Suora signalointi mahdollistaa sen, että ryhmä soluja voi koordinoida vastauksensa signaaliin, jonka vain yksi niistä on saattanut vastaanottaa. Kasveissa plasmodesmat ovat kaikkialla läsnä, mikä tekee koko kasvista jättimäisen viestintäverkon.
9.1.2 Reseptorityypit
Reseptorit ovat kohdesolussa tai sen pinnalla olevia proteiinimolekyylejä, jotka sitoutuvat ligandeihin. Reseptoreita on kahdenlaisia, sisäisiä reseptoreita ja solupinnan reseptoreita.
Sisäiset reseptorit
Sisäiset reseptorit, joita kutsutaan myös solunsisäisiksi tai sytoplasmisiksi reseptoreiksi, sijaitsevat kohdesolujen sytoplasmassa ja reagoivat hydrofobisiin ligandimolekyyleihin, jotka pystyvät kulkemaan plasmakalvon läpi. Solun sisälle päästyään monet näistä molekyyleistä sitoutuvat proteiineihin, jotka toimivat mRNA-synteesin (transkription) säätelijöinä välittäen geeniekspressiota.
Geeniekspressio on solussa tapahtuva prosessi, jossa solun DNA:ssa oleva informaatio muutetaan aminohappojen sekvenssiksi, joka lopulta muodostaa proteiinin. Kun ligandi sitoutuu sisäiseen reseptoriin, käynnistyy konformaatiomuutos, joka paljastaa DNA:n sitoutumiskohdan reseptoriproteiinissa. Ligandi-reseptorikompleksi siirtyy tumaan, sitoutuu sitten kromosomaalisen DNA:n tiettyihin säätelyalueisiin ja edistää transkription käynnistymistä (kuva 9.4). Transkriptio on prosessi, jossa solun DNA:ssa oleva informaatio kopioidaan erityiseen RNA:n muotoon, jota kutsutaan sanansaattaja-RNA:ksi (messenger RNA, mRNA); solu käyttää mRNA:n sisältämää informaatiota tiettyjen aminohappojen yhdistämiseen oikeassa järjestyksessä, jolloin syntyy proteiini. Kun ligandi siis sitoutuu sisäiseen reseptoriin, se voi suoraan vaikuttaa geeniekspressioon kohdesolussa.
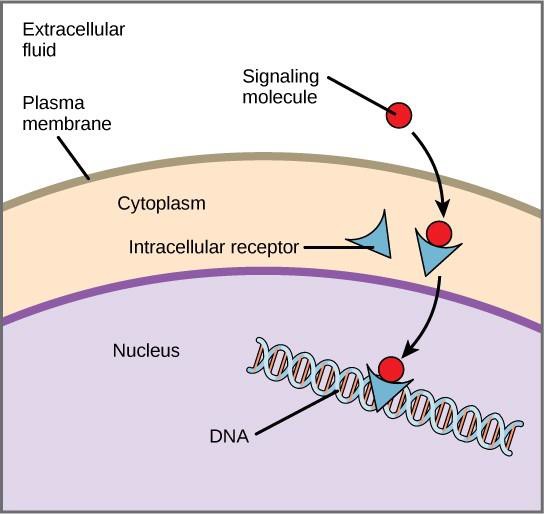
Solupinnan reseptorit
Solupinnan reseptorit, jotka tunnetaan myös nimellä transmembraanireseptorit, ovat integraalisia proteiineja, jotka sitoutuvat ulkoisiin signaalimolekyyleihin. Nämä reseptorit kattavat plasmakalvon ja suorittavat signaalin transduktiota, jossa solunulkoinen signaali muunnetaan solujen väliseksi signaaliksi. (Kuva 9.5). Koska solupinnan reseptoriproteiinit ovat perustavanlaatuisia solun normaalin toiminnan kannalta, ei liene yllättävää, että minkä tahansa näistä proteiineista toimintahäiriöllä voi olla vakavia seurauksia. Tiettyjen reseptorimolekyylien proteiinirakenteiden virheillä on osoitettu olevan merkitystä hypertensiossa (korkea verenpaine), astmassa, sydänsairauksissa ja syövässä.
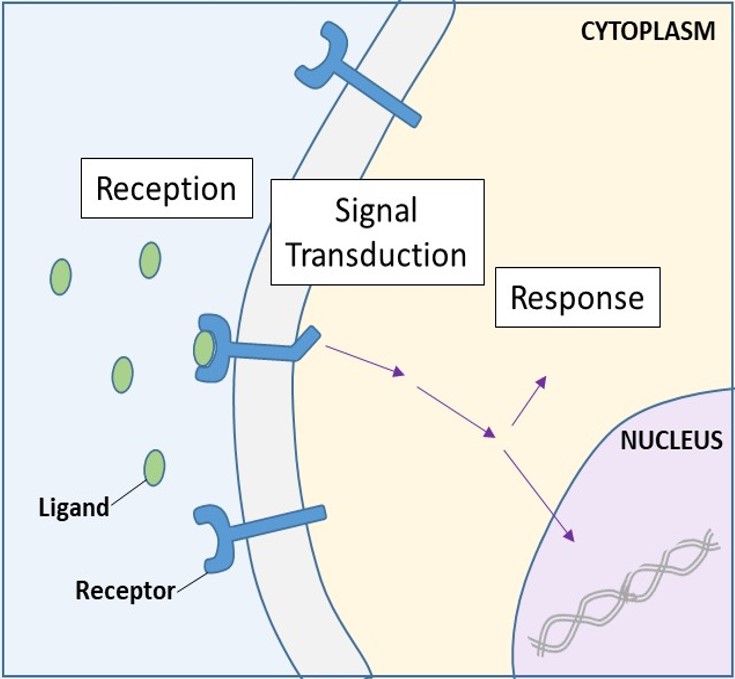
Kullakin solupinnan reseptorilla on kolme pääkomponenttia: ulkoinen ligandia sitova domeeni eli solunulkoinen domeeni, hydrofobinen kalvon ylittävä alue ja solunsisäinen domeeni. Solupintareseptorit osallistuvat suurimpaan osaan monisoluisten organismien signaloinnista. Solupintareseptoreita on kolme yleistä luokkaa: entsyymiin sidotut reseptorit, ionikanaviin sidotut reseptorit ja G-proteiiniin sidotut reseptorit.
Ensyymiin sidotut reseptorit ovat solupinnan reseptoreita, joilla on solunsisäisiä domeeneja, jotka liittyvät entsyymiin. Joissakin tapauksissa reseptorin solunsisäinen domeeni on itse entsyymi. Toisissa entsyymisidonnaisissa reseptoreissa on pieni solunsisäinen domeeni, joka on suoraan vuorovaikutuksessa entsyymin kanssa. Entsyymisidonnaisilla reseptoreilla on tavallisesti suuret solunulkoiset ja solunsisäiset domeenit, mutta membraanin läpäisevä alue koostuu yhdestä alfahelixistä peptidiketjussa.
Kun ligandi sitoutuu entsyymisidonnaisen reseptorin solunulkoiseen domeeniin, signaali siirtyy membraanin läpi ja aktivoi entsyymin. Entsyymin aktivoituminen käynnistää solun sisällä tapahtumaketjun, joka lopulta johtaa vasteeseen.
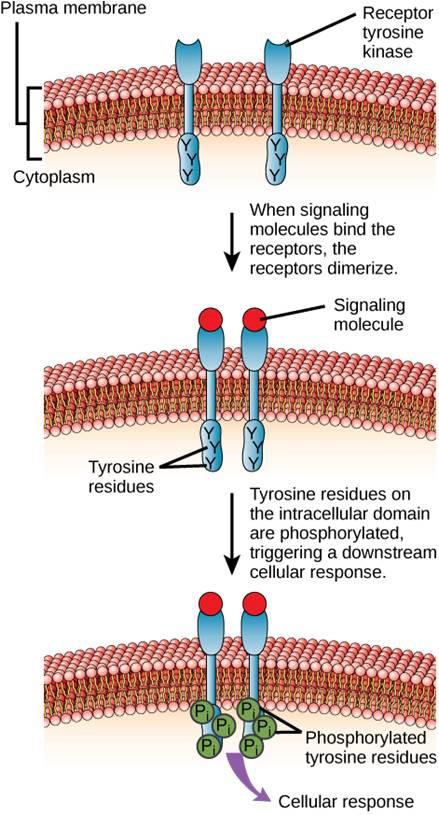
Yksi esimerkki entsyymisidonnaisesta reseptorista on tyrosiinikinaasireseptori (kuva 9.6). Kinaasi on entsyymi, joka siirtää fosfaattiryhmiä ATP:stä toiseen proteiiniin. Tyrosiinikinaasireseptori siirtää fosfaattiryhmiä tyrosiinimolekyyleihin. Ensin signaalimolekyylit sitoutuvat kahden läheisen tyrosiinikinaasireseptorin solunulkoiseen domeeniin. Tämän jälkeen kaksi naapurireseptoria sitoutuvat toisiinsa eli dimeroituvat. Tämän jälkeen reseptorien solunsisäisen domeenin tyrosiinijäämiin lisätään fosfaatteja (fosforylaatio). Fosforyloituneet jäännökset voivat sitten välittää signaalin seuraavalle viestinviejälle sytoplasmassa.
Epidermisen kasvutekijän reseptorit ovat esimerkki reseptorityrosiinikinaaseista, jotka noudattavat tätä signalointitapaa. Viat tämän perheen ErbB-signaloinnissa voivat johtaa neuromuskulaarisiin sairauksiin, kuten multippeliskleroosiin ja Alzheimerin tautiin.
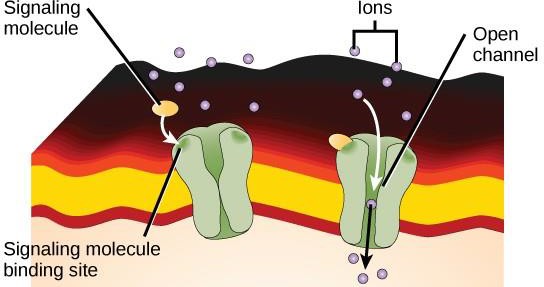
Ionikanaviin sidoksissa olevat reseptorit sitoutuvat ligandiin ja avaavat kalvon läpi kanavan, joka päästää tietyt ionit läpi. Tämäntyyppisillä solupintareseptoreilla on laaja kalvot ylittävä alue, jossa on hydrofobisia aminohappoja. Kanavan sisäpuolella olevat aminohapot ovat sitä vastoin hydrofiilisiä, jotta ionit pääsevät läpi. Kun ligandi sitoutuu kanavan solunulkoiseen alueeseen, proteiinin rakenteessa tapahtuu konformaatiomuutos, joka sallii ionien, kuten natriumin, kalsiumin, magnesiumin tai vedyn kulkeutumisen (kuva 9.7).
G-proteiiniin sidoksissa olevat reseptorit sitoutuvat ligandiin ja aktivoivat siihen liittyvän G-proteiinin. Aktivoitunut G-proteiini on sitten vuorovaikutuksessa läheisen kalvoproteiinin kanssa, joka voi olla ionikanava tai entsyymi (kuva 9.8). Kaikilla G-proteiiniin sidoksissa olevilla reseptoreilla on seitsemän transmembraanidomeenia, mutta kullakin reseptorilla on erityinen solunulkoinen domeeni ja G-proteiinin sitoutumiskohta.
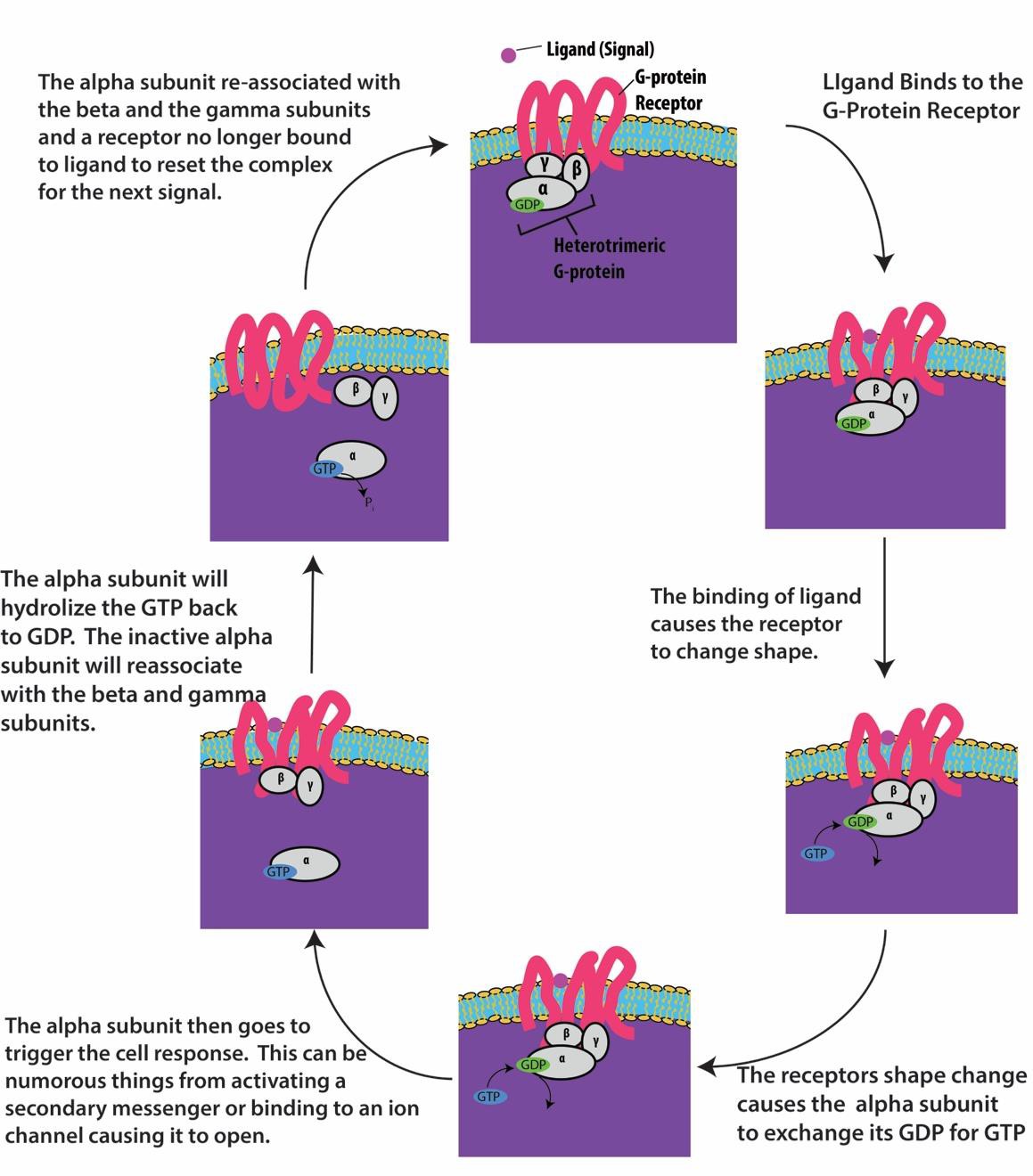
Solun signalointi G-proteiiniin sidottujen reseptorien avulla tapahtuu syklinä. Kun ligandi sitoutuu reseptoriin, syntyvä muodonmuutos aktivoi G-proteiinin, joka vapauttaa GDP:tä ja ottaa GTP:tä. Tämän jälkeen G-proteiinin alayksiköt jakautuvat α- ja βγ-alayksiköiksi. Toinen tai molemmat näistä G-proteiinifragmenteista voivat aktivoida muita solun proteiineja. Jonkin ajan kuluttua G-proteiinin aktiivisen α-alayksikön GTP hydrolysoituu GDP:ksi ja βγ-alayksikkö deaktivoituu. Alayksiköt assosioituvat uudelleen muodostaen inaktiivisen G-proteiinin, ja sykli alkaa uudelleen (kuva 9.8).
G-proteiiniin kytkeytyviä reseptoreita käytetään monissa fysiologisissa prosesseissa, kuten näönsiirtoon, makuun sekä immuunijärjestelmän ja tulehduksen säätelyyn.

HER2 on reseptorityrosiinikinaasi. Ihmisen rintasyövistä 30 prosentissa HER2 aktivoituu pysyvästi, mikä johtaa sääntelemättömään solunjakautumiseen. Lapatinibi, rintasyövän hoitoon käytettävä lääke, estää prosessia, jossa reseptori fosforyloi itseään, ja vähentää siten kasvaimen kasvua 50 prosenttia. Mitä seuraavista vaiheista Lapatinibi estäisi?
- Signaalimolekyylin sitoutuminen, dimerisaatio ja solun myöhempi vaste
- Dimerisaatio ja solun myöhempi vaste
- Solun myöhempi vaste
- Solun myöhempi vaste
- Fosfataasiaktiviteetti, dimerisaatio ja solun myöhempi vaste
>
9.1.3 Signaalimolekyylit
Signaalisolujen tuottamat ligandit ovat kemiallisia signaaleja, jotka kulkeutuvat kohdesoluihin ja aiheuttavat vasteen. Ligandeina toimivia molekyylejä on uskomattoman monenlaisia, ja ne vaihtelevat pienistä proteiineista pieniin ioneihin. Ligandit luokitellaan joko pieniin hydrofobisiin ligandeihin, jotka voivat läpäistä plasmakalvot, tai vesiliukoisiin ligandeihin, jotka eivät voi läpäistä plasmakalvoja.
Pienet hydrofobiset ligandit
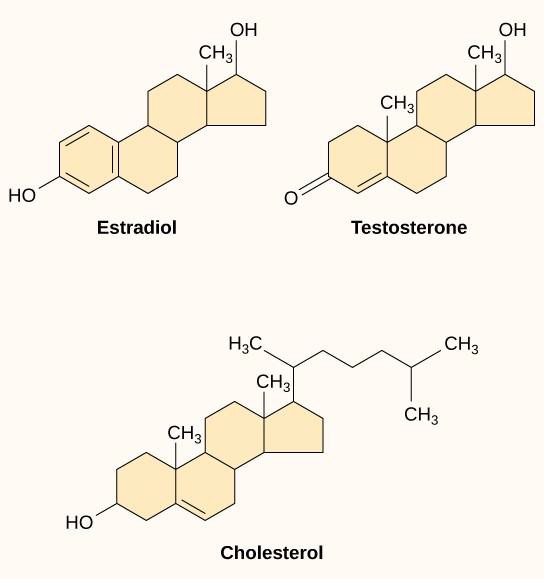
Pienet hydrofobiset ligandit, joita kutsutaan myös lipidiliukoisiksi ligandeiksi, pystyvät diffuusiutumaan suoraan plasmakalvon läpi ja olemaan vuorovaikutuksessa plasmakalvon sisäisten reseptorien kanssa. Tämän ligandiluokan tärkeitä jäseniä ovat steroidihormonit. Steroidit ovat lipidejä, joilla on hiilivetyrunko, jossa on neljä sulautunutta rengasta; eri steroideilla on erilaisia funktionaalisia ryhmiä kiinnittyneenä hiilirunkoon. Steroidihormoneihin kuuluvat naispuolinen sukupuolihormoni estradioli, joka on eräs estrogeenityyppi, miespuolinen sukupuolihormoni testosteroni ja kolesteroli, joka on biologisten kalvojen tärkeä rakenneosa ja steroidihormonien esiaste (kuva 9.10). Muita hydrofobisia hormoneja ovat kilpirauhashormonit ja D-vitamiini. Jotta hydrofobiset ligandit liukenisivat vereen, niiden on sitouduttava kantajaproteiineihin, kun ne kulkeutuvat verenkierrossa.
Vesiliukoiset ligandit
Sen vuoksi, että vesiliukoiset ligandit ovat polaarisia, ne eivät pääse kulkemaan plasmakalvon läpi ilman apua. Joskus ne ovat liian suuria kulkeutuakseen kalvon läpi lainkaan. Sen sijaan useimmat vesiliukoiset ligandit sitoutuvat solupinnan reseptorien solunulkoiseen domeeniin (ks. kuva 9.5). Tämä ligandien ryhmä on varsin monimuotoinen, ja siihen kuuluu pieniä molekyylejä, peptidejä ja proteiineja.
9.2 | Signaalin leviäminen
Tämän jakson lopussa osaat:
- selittää, miten ligandin sitoutuminen käynnistää signaalinsiirron koko solussa.
- Tunnistaa, että solunsisäiset signaalit välittyvät fosforylaation tai kakkoslähettiläiden roolissa.
Kun vesiliukoinen ligandi sitoutuu reseptoriinsa, signaali välittyy kalvon läpi sytoplasmaan. Signaalin jatkumista tällä tavoin kutsutaan signaalin transduktioksi (kuva 9.5). Signaalin transduktiota tapahtuu vain solupinnan reseptoreilla, sillä solun sisäiset reseptorit voivat päästä soluun.
Kun ligandi sitoutuu reseptoriinsa, tapahtuu konformaatiomuutoksia, jotka vaikuttavat reseptorin solunsisäiseen domeeniin. Nämä konformaatiomuutokset johtavat solunsisäisen domeenin tai siihen liittyvien proteiinien aktivoitumiseen. Joissakin tapauksissa ligandin sitoutuminen aiheuttaa reseptorin dimeroitumisen, mikä tarkoittaa, että kaksi reseptoria sitoutuu toisiinsa muodostaen vakaan kompleksin, jota kutsutaan dimeriksi. Dimeeri on kemiallinen yhdiste, joka muodostuu, kun kaksi (usein identtistä) molekyyliä liittyy yhteen. Reseptorien sitoutuminen tällä tavoin mahdollistaa sen, että niiden solunsisäiset domeenit joutuvat läheiseen kosketukseen ja aktivoivat toisiaan.
9.2.1 Signaalireitit ja signaalin vahvistaminen
Vaikka signaalimolekyylejä esiintyy usein hyvin pieninä pitoisuuksina, ne voivat saada aikaan syvällisiä vaikutuksia. Kun ligandi sitoutuu solupinnan reseptoriin, reseptorin solunsisäisten komponenttien aktivoituminen käynnistää tapahtumaketjun, jota kutsutaan signaalireitiksi tai signaalikaskadiksi. Signaalireitissä toiset sanansaattajat, entsyymit ja/tai aktivoituneet proteiinit aktivoivat muita proteiineja tai sanansaattajia (kuva 9.11). Jokainen reitin jäsen voi aktivoida tuhansia reitin seuraavia jäseniä prosessissa, jota kutsutaan signaalin vahvistamiseksi. Koska signaali vahvistuu jokaisessa vaiheessa, yhdestä reseptorista, joka sitoo ligandin, voi syntyä hyvin suuri vaste.
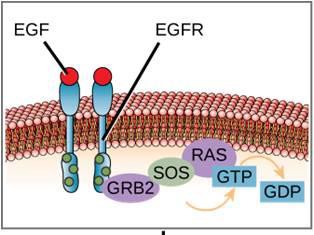
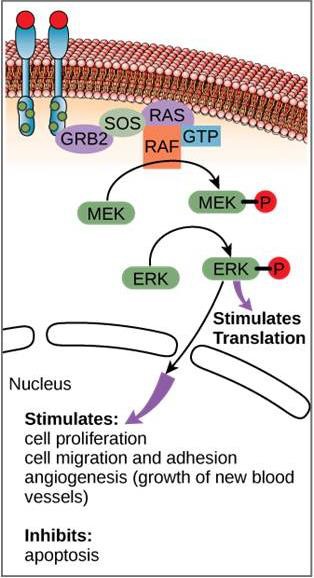
Kuvassa 9.11 on esimerkki signaalireitistä. Epidermaalinen kasvutekijä (EGF) on signaalimolekyyli, joka osallistuu solujen kasvun, haavan paranemisen ja kudosten korjautumisen säätelyyn. EGF:n reseptori (EGFR) on tyrosiinikinaasi. Aktivoitunut kinaasi fosforyloi ja aktivoi monia jatkoketjun molekyylejä. Kun EGF sitoutuu EGFR:ään, jatkoketjun fosforylaatiotapahtumien kaskadi antaa solulle signaalin kasvaa ja jakautua. Jos EGFR aktivoituu sopimattomina aikoina, voi syntyä hallitsematonta solukasvua (syöpää).
Tietyissä syövissä RAS G-proteiinin GTPaasiaktiivisuus on estynyt. Tämä tarkoittaa, että RAS-proteiini ei enää pysty hydrolysoimaan GTP:tä GDP:ksi. Miten tämä vaikuttaisi solun myöhempiin tapahtumiin?
9.2.2 Solunsisäisen signaloinnin menetelmät
Signalointireitin indusoituminen riippuu siitä, miten jokin entsyymi muuttaa solun komponenttia. On olemassa lukuisia entsymaattisia modifikaatioita, jotka voivat tapahtua polun seuraavan komponentin aktivoimiseksi. Seuraavassa on lueteltu joitakin solunsisäisen signaloinnin yleisimpiä tapahtumia.
Fosforylaatio
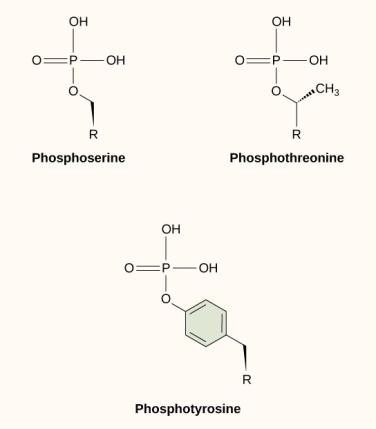
Yksi yleisimmistä kemiallisista modifikaatioista, joita tapahtuu signaalireiteissä, on fosfaattiryhmän lisääminen molekyyliin prosessissa, jota kutsutaan fosforylaatioksi. Fosfaatti voidaan lisätä nukleotidiin, kuten GMP:hen, jolloin muodostuu GDP tai GTP. Fosfaatteja lisätään usein myös proteiinien seriini-, treoniini- ja tyrosiinijäämiin, jolloin ne korvaavat aminohapon hydroksyyliryhmän (kuva 9.12). Fosfaatin siirtoa katalysoi entsyymi, jota kutsutaan kinaasiksi. Fosforylaatio voi aktivoida tai inaktivoida entsyymejä, ja fosforylaation kumoaminen, defosforylaatio, kääntää vaikutuksen päinvastaiseksi.
Sekundaariset sanansaattajat
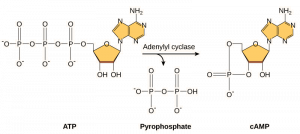
Sekundaariset sanansaattajat (second messengers) ovat pieniä molekyylejä, jotka levittävät signaalia sen jälkeen, kun se on käynnistynyt signaalimolekyylin sitoutuessa reseptoriin. Nämä molekyylit auttavat levittämään signaalia sytoplasmassa muuttamalla tiettyjen soluproteiinien käyttäytymistä. Monien eri solutyyppien käyttämä toinen lähettiläs on syklinen AMP (cAMP). Syklistä AMP:tä syntetisoi entsyymi adenyylisyklaasi ATP:stä (kuva 9.13). CAMP:n tärkein tehtävä soluissa on sitoutua cAMP-riippuvaiseksi kinaasiksi (A-kinaasiksi) kutsuttuun entsyymiin ja aktivoida se. A-kinaasi säätelee monia elintärkeitä aineenvaihduntareittejä: Se fosforyloi kohdeproteiiniensa seriini- ja treoniinijäämiä ja aktivoi niitä samalla. A-kinaasia esiintyy monissa eri solutyypeissä, ja kunkin solutyypin kohdeproteiinit ovat erilaisia. Toinen sekundaarilähettiläs on Ca2+,joka voi vapautua tulvimaan soluun.
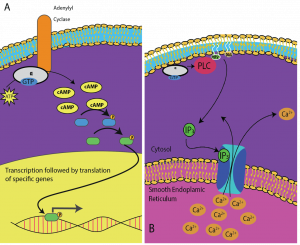
Eri solut reagoivat cAMP:iin eri tavoin. Kuvassa 9.14 on esitetty G-proteiinireseptorin alfa-alayksikkö aktivoimassa kahta erityyppistä signalointia. Ensimmäisessä kuvassa adenylaattisyklaasientsyymi tuottaa cAMP:a, kun alfa-alayksikkö aktivoi sen. cAMP aktivoi sitten muita proteiineja, jotka vaikuttavat geenien transkriptioon. Toisessa kuvassa G-proteiinin alfa-alayksikkö käynnistää kaskadin, joka vapauttaa Ca2+:a sileästä endoplasmisesta retikulumista. Tässä tapauksessa Ca2+ on sekundaarinen sanansaattaja, joka aiheuttaa soluvasteen.
9.3 | Vastaus signaaliin
Tämän jakson lopussa osaat:
- Tunnistaa, että signaalireitit ohjaavat proteiinien ilmentymistä, solujen aineenvaihduntaa ja solujen kasvua.
- Tunnistaa apoptoosin roolin terveen elimistön kehityksessä ja ylläpidossa.
Signaalinsiirtoreittien avulla plasmakalvon reseptorit saavat aikaan erilaisia vaikutuksia solussa. Solun sisällä ligandit sitoutuvat sisäisiin reseptoreihinsa, jolloin ne voivat vaikuttaa suoraan solun DNA:han ja proteiineja tuottavaan koneistoon. Signaalireittien tulokset ovat hyvin erilaisia ja riippuvat solutyypistä sekä ulkoisista ja sisäisistä olosuhteista. Jäljempänä kuvataan pieni otos vasteista.
9.3.1 Signaalireitin vasteet
Geeniekspressio
Jotkut signaalinvälitysreitit säätelevät RNA:n transkriptiota. Toiset säätelevät proteiinien translaatiota.
Solun aineenvaihdunnan lisääntyminen
Lihassolujen β-adrenergisten reseptorien aktivoituminen lihassoluissa adrenaliinin vaikutuksesta johtaa syklisen AMP:n lisääntymiseen solun sisällä. Adrenaliini on lisämunuaisen tuottama hormoni, joka valmistaa elimistöä lyhytaikaisiin hätätilanteisiin.
Solujen kasvu
Solujen signaalireiteillä on suuri merkitys myös solujen jakautumisessa. Solut eivät normaalisti jakaannu, elleivät muiden solujen antamat signaalit stimuloi niitä. Solujen kasvua edistäviä ligandeja kutsutaan kasvutekijöiksi. Useimmat kasvutekijät sitoutuvat solupinnan reseptoreihin, jotka ovat yhteydessä tyrosiinikinaaseihin.
Solukuolema
Kun solu on vaurioitunut, tarpeeton tai mahdollisesti vaarallinen elimistölle, solu voi käynnistää mekanismin, joka käynnistää ohjelmoidun solukuoleman eli apoptoosin. Apoptoosin avulla solu voi kuolla kontrolloidulla tavalla, joka estää mahdollisesti vahingollisten molekyylien vapautumisen solun sisältä. Joissakin tapauksissa, kuten virusinfektiossa tai syövästä johtuvassa hallitsemattomassa solun jakautumisessa, solun normaalit kontrollit ja tasapainot eivät kuitenkaan toimi. Myös ulkoinen signalointi voi käynnistää apoptoosin. Esimerkiksi useimmilla normaaleilla eläinsoluilla on reseptoreita, jotka ovat vuorovaikutuksessa solunulkoisen matriisin kanssa, joka on glykoproteiinien muodostama verkosto, joka tarjoaa eläinsoluille rakenteellista tukea. Solureseptorien sitoutuminen solunulkoiseen matriisiin käynnistää solun sisällä signaalikaskadin. Jos solu kuitenkin siirtyy pois solunulkoisesta matriisista, signalointi lakkaa ja solu käy läpi apoptoosin. Tämä järjestelmä auttaa estämään solujen kulkeutumisen elimistössä ja lisääntymisen hallitsemattomasti, kuten tapahtuu etäpesäkkeitä muodostavien kasvainsolujen kohdalla.
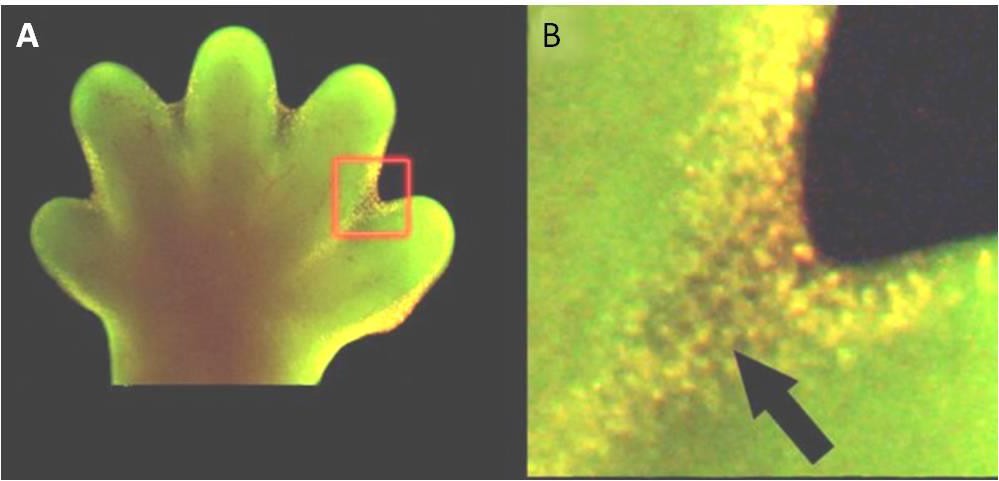
Apoptoosi on olennainen myös normaalin alkionkehityksen kannalta. Selkärankaisilla esimerkiksi kehityksen varhaisiin vaiheisiin kuuluu verkkomaisen kudoksen muodostuminen yksittäisten sormien ja varpaiden välille (kuva 9.15). Normaalin kehityksen aikana nämä tarpeettomat solut on eliminoitava, jotta täysin erilliset sormet ja varpaat voivat muodostua. Solun signalointimekanismi käynnistää apoptoosin, joka tuhoaa kehittyvien sormenpäiden välissä olevat solut.
9.3.2 Signaalireittien lopettaminen
Kasvainsoluissa usein havaittu poikkeava signalointi on osoitus siitä, että signaalin lopettaminen sopivaan aikaan voi olla yhtä tärkeää kuin signaalin aloittaminen. Yksi tapa pysäyttää tietty signaali on hajottaa ligandi tai poistaa se niin, että se ei enää pääse reseptoriinsa. Yksi syy siihen, että hydrofobiset hormonit, kuten estrogeeni ja testosteroni, saavat aikaan pitkäkestoisia tapahtumia, on se, että ne sitoutuvat kantajaproteiineihin. Nämä proteiinit mahdollistavat liukenemattomien molekyylien liukenemisen vereen, mutta ne myös suojaavat hormoneja kiertävien entsyymien aiheuttamalta hajoamiselta.
Solun sisällä monet erilaiset entsyymit peruuttavat merkkikaskadien tuloksena syntyviä solumuutoksia. Esimerkiksi fosfataasit ovat entsyymejä, jotka poistavat kinaasien proteiineihin kiinnittämän fosfaattiryhmän prosessissa, jota kutsutaan defosforylaatioksi. cAMP hajotetaan AMP:ksi fosfodiesteraasin avulla, jolloin sen signaali päättyy. Vastaavasti kalsiumvarastojen vapautumisen kumoavat solukalvoissa sijaitsevat Ca2+-pumput.