Oppimistavoitteet
- Määritellä ja antaa esimerkkejä radioaktiivisuuden päätyypeistä.
Atomit koostuvat subatomisista hiukkasista – protoneista, neutroneista ja elektroneista. Protonit ja neutronit sijaitsevat ytimessä ja muodostavat suurimman osan atomin massasta, kun taas elektronit kiertävät ydintä kuorissa ja alikuorissa ja vastaavat atomin koosta. Muista merkintätapa, jolla tietyn atomin isotooppi voidaan esittää lyhyesti:
\
Tässä esimerkissä alkuaine, jota esitetään symbolilla C, on hiili. Sen järjestysluku, 6, on symbolin vasen alempi alaindeksi, ja se on atomin sisältämien protonien lukumäärä. Massaluku, symbolin vasemmassa yläkulmassa oleva yläindeksi, on kyseisen isotoopin ytimessä olevien protonien ja neutronien lukumäärän summa. Tässä tapauksessa massaluku on 12, mikä tarkoittaa, että neutronien määrä atomissa on 12 – 6 = 6 (eli atomin massaluku miinus protonien määrä ytimessä on yhtä suuri kuin neutronien määrä). Toisinaan atomiluku jätetään tässä merkintätavassa pois, koska alkuaineen symboli itsessään ilmaisee sille ominaisen atomiluvun. Vedyn kahdelle isotoopille, 2H ja 3H, on annettu omat nimensä: deuterium (D) ja tritium (T). Toinen tapa ilmaista tietty isotooppi on luetella massanumero alkuaineen nimen perässä, kuten hiili-12 tai vety-3.
Atomiteoriassa 1800-luvulla oletettiin, että ytimillä oli kiinteä koostumus. Mutta vuonna 1896 ranskalainen tiedemies Henri Becquerel havaitsi, että valokuvauslevyn lähelle sijoitettu uraaniyhdiste aiheutti kuvan levylle, vaikka yhdiste oli kääritty mustaan kankaaseen. Hän päätteli, että uraaniyhdisteestä lähti jonkinlaista säteilyä, joka läpäisi kankaan ja valaisi valokuvauslevyn. Lisätutkimukset osoittivat, että säteily oli hiukkasten ja sähkömagneettisten säteiden yhdistelmä, jonka perimmäinen lähde oli atomiydin. Näitä emansioita kutsuttiin lopulta kollektiivisesti radioaktiivisuudeksi.
Radioaktiivisia emissioita on kolme pääasiallista muotoa. Ensimmäistä kutsutaan alfahiukkaseksi,jota symbolisoidaan kreikkalaisella kirjaimella α. Alfahiukkanen koostuu kahdesta protonista ja kahdesta neutronista, joten se on sama kuin heliumin ydin. (Käytämme usein sanaa \(\ce{^{4}_{2}He}\) kuvaamaan alfahiukkasta). Sen varaus on 2+. Kun radioaktiivinen atomi lähettää alfahiukkasen, alkuperäisen atomin järjestysluku pienenee kahdella (koska se menettää kaksi protonia) ja massaluku pienenee neljällä (koska se menettää neljä ydinhiukkasta). Voimme esittää alfahiukkasen emissiota kemiallisella yhtälöllä – esimerkiksi uraani-235:n alfahiukkasen emissio on seuraava:
\
Miten tiedämme, että reaktion tuote on \(\ce{^{231}_{90}Th}\)? Käytämme aineen säilymislakia, jonka mukaan ainetta ei voi luoda eikä tuhota. Tämä tarkoittaa, että meillä on oltava sama määrä protoneja ja neutroneita kemiallisen yhtälön molemmilla puolilla. Jos uraaniydin menettää 2 protonia, jäljelle jää 90 protonia, jolloin alkuaine on torium. Lisäksi jos menetämme 4 ydinhiukkasta alkuperäisestä 235:stä, jäljelle jää 231 hiukkasta. Näin ollen käytämme vähennyslaskentaa tunnistaaksemme toriumatomin isotoopin – tässä tapauksessa \(\ce{^{231}_{90}Th}\).
Kemistit käyttävät usein nimityksiä kantaisotooppi ja tytärisotooppi kuvaamaan alkuperäistä atomia ja muuta tuotetta kuin alfahiukkasta. Edellisessä esimerkissä \(\ce{^{235}_{92}U}\) on kantaisotooppi ja \(\ce{^{231}_{90}Th}\) on tytärisotooppi. Kun yksi alkuaine muuttuu tällä tavoin toiseksi, se käy läpi radioaktiivisen hajoamisen.
Esimerkki \(\PageIndex{1}\):
Kirjoita ydinyhtälö, joka kuvaa radon-222:n radioaktiivista hajoamista alfahiukkassäteilyn avulla, ja tunnista tytärisotooppi.
Ratkaisu
Radonin järjestysluku on 86, joten kantaisotooppi esitetään muodossa \(\ce{^{222}_{86}Rn}\). Esitämme alfahiukkasen muodossa \(\ce{^{4}_{2}He}\) ja käytämme vähennyslaskentaa (222 – 4 = 218 ja 86 – 2 = 84) tunnistaaksemme tytärisotoopin poloniumin isotoopiksi, \(\mathrm{^{218}_{84}Po}\):
\(\ce{_{86}^{222}Rn\rightarrow \, _2^4He + \, _{84}^{218}Po}\)
Harjoitus \(\PageIndex{1}\): Polonium-209
Kirjoita ydinvoimayhtälö, joka kuvaa polonium-209:n radioaktiivista hajoamista alfahiukkaspäästön avulla, ja tunnista tytärisotooppi.
Vastaus
\(\ce{_{84}^{209}Po\rightarrow \, _2^4He + \, _{82}^{205}Pb}\)
Toisen tärkeimmän radioaktiivisen emissiotyypin nimi on beetahiukkanen, jota symbolisoidaan kreikkalaisella kirjaimella β. Beetahiukkanen on ytimestä (ei ydintä ympäröivistä elektronikuorista) sinkoutunut elektroni, jolla on 1- varaus. Beetahiukkanen voidaan esittää myös muodossa \(\ce{^0_{-1}e}\) tai β-. Ytimeen kohdistuvan beetahiukkassäteilyn nettovaikutus on, että neutroni muuttuu protoniksi. Kokonaismassaluku pysyy samana, mutta koska protonien määrä kasvaa yhdellä, atomiluku kasvaa yhdellä. Hiili-14 hajoaa emittoimalla beetahiukkasen:
\
Jälleen kerran atomilukujen summa on sama yhtälön molemmilla puolilla, samoin kuin massalukujen summa. (Huomaa, että elektronille annetaan ”atomiluku” 1-, joka vastaa sen varausta.)
Kolmas merkittävä radioaktiivisen säteilyn tyyppi ei ole hiukkanen vaan pikemminkin hyvin energinen sähkömagneettisen säteilyn muoto, jota kutsutaan gammasäteilyksi ja jota symbolisoidaan kreikkalaisella kirjaimella γ. Gammasäteilyllä itsellään ei ole sähköistä kokonaisvarautumista, mutta se voi lyödä elektroneja irti aineenäytteessä olevista atomeista ja tehdä näytteestä sähköisesti varautunutta (minkä vuoksi gammasäteilyä kutsutaan ionisoivaksi säteilyksi). Esimerkiksi radon-222:n radioaktiivisessa hajoamisessa syntyy sekä alfa- että gammasäteilyä, joista jälkimmäisen energia on 8,2 × 10-14 J jokaista hajoavaa ydintä kohti:
\
Tämä ei ehkä vaikuta suurelta energialähteeltä, mutta jos 1 mooli radonatomia hajoaisi, gammasäteilyn energia olisi 49 miljoonaa kJ!
Esimerkki \\(\Sivunindeksi{2}\): Kirjoita ydinyhtälö, joka kuvaa boorin-12 radioaktiivista hajoamista beetahiukkassäteilyn avulla, ja tunnista tytärisotooppi. Samanaikaisesti beetahiukkasen kanssa emittoituu gammasäteilyä.
Ratkaisu
Eläisisotooppi on \(\ce{^{12}_{5}B}\), kun taas yksi tuotteista on elektroni, \(\ce{^{0}_{-1}e}\\). Jotta massa- ja järjestysluvut olisivat samat molemmilla puolilla, tytärisotoopin massaluvun on oltava 12 ja sen järjestysluvun 6. Alkuaine, jonka järjestysluku on 6, on hiili. Täydellinen ydinyhtälö on siis seuraava:
\
Tytärisotooppi on \(\ce{^{12}_6 C}\).
Harjoitus \(\PageIndex{2}\): Jodi-131
Kirjoita ydinyhtälö, joka kuvaa jodi-131:n radioaktiivista hajoamista beetahiukkassäteilyn avulla, ja tunnista tytärisotooppi. Samanaikaisesti beetahiukkasen kanssa emittoituu gammasäteilyä.
Vastaus
\
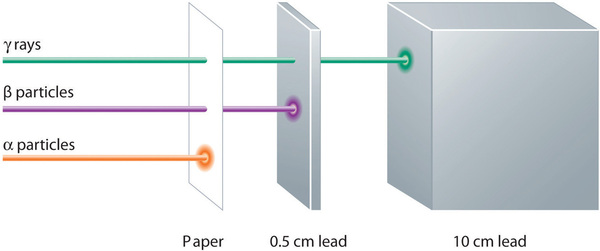
Alfa-, beeta- ja gammasäteilyllä on erilainen kyky läpäistä ainetta. Suhteellisen suuri alfahiukkanen pysähtyy helposti aineeseen (vaikka se saattaa välittää huomattavan määrän energiaa aineeseen, johon se koskettaa). Beetahiukkaset tunkeutuvat hieman aineeseen, ehkä korkeintaan muutaman senttimetrin päähän. Gammasäteet voivat tunkeutua syvälle aineeseen ja välittää suuren määrän energiaa ympäröivään aineeseen. Taulukossa \(\PageIndex{1}\) on yhteenveto kolmen tärkeimmän radioaktiivisen päästötyypin ominaisuuksista.
| Tunnus | Alfahiukkaset | Betahiukkaset | Gammasäteet |
|---|---|---|---|
| symbolit | α, \(\mathrm{_{2}^{4}He}\) | β, \(\ce{^{0}_{-1} e}\\) | γ |
| identiteetti | heliumydin | elektroni | elektromagneettinen säteily |
| varaus | 2+ | 1- | ei |
| massaluku | 4 | 0 | 0 |
| läpäisykyky | minimaalinen (ei läpäise ihoa) | lyhyt (läpäisee ihon ja joitakin kudoksia hieman) | syvä (läpäisee kudoksia syvälle) |
Satunnaisesti, atomiydin hajoaa pienempiin osiin radioaktiivisessa prosessissa, jota kutsutaan spontaaniksi fissioksi (tai halkeamiseksi). Tyypillisesti fissiossa syntyvät tytärisotoopit ovat pikemminkin vaihteleva sekoitus tuotteita kuin tietty isotooppi, kuten alfa- ja beetahiukkaspäästössä. Usein fissiossa syntyy ylimääräisiä neutroneita, jotka joskus vangitaan muihin ytimiin, mikä voi aiheuttaa uusia radioaktiivisia tapahtumia. Uraani-235 fissioituu spontaanisti vähäisessä määrin. Yksi tyypillinen reaktio on
\
jossa \(\ce{_0^1n}\) on neutroni. Kuten kaikissa ydinprosesseissa, atomilukujen ja massalukujen summien on oltava samat yhtälön molemmilla puolilla. Spontaania fissiota esiintyy vain suurissa ytimissä. Pienin ydin, jossa esiintyy spontaania fissiota, on lyijy-208.
Fissio on radioaktiivinen prosessi, jota käytetään ydinvoimaloissa ja yhdessä ydinpommityypissä.
Key Takeaway
Radioaktiivisuuden päätyyppejä ovat alfahiukkaset, beetahiukkaset ja gammasäteet.
Konseptin kertausharjoitus
-
Mitä ovat radioaktiivisuuden päätyypit? Kirjoita kutakin tyyppiä havainnollistavat kemialliset yhtälöt.
Vastaus
-
Radioaktiivisuuden päätyypit ovat alfahajoaminen, beetahajoaminen ja gammasäteilyn emittoituminen; alfahajoaminen, jossa on gammasäteilyä: \(\mathrm{_{86}^{222}Rn \rightarrow \, _{84}^{218}Po + \, ^4_2He + \gamma}\); beetahajoaminen: \(\ce{_6^{14}C \rightarrow _7^{14}N + ^0_{-1}e}\) (vastaukset vaihtelevat)