- trans-Cinnamaldehyd Kemiske egenskaber, anvendelse, produktion
- Overblik
- Farmakokinetik
- Anvendelser
- Toksicitet
- Kemiske egenskaber
- Kemiske egenskaber
- Kemiske egenskaber
- Definition
- Syntese Reference(r)
- Generel beskrivelse
- Luft &Vand Reaktioner
- Reaktivitetsprofil
- Brandfare
- Potentiel eksponering
- Sendelse
- Inkompatibiliteter
- Affaldsbortskaffelse
trans-Cinnamaldehyd Kemiske egenskaber, anvendelse, produktion
Overblik
Cinnamaldehyd, et gammelt smagsstof, der stammer fra kaneltræer og andre arter af Cinnamomum-slægten, har nu tiltrukket sig stigende interesse for sin evne til at forebygge udviklingen af diabetes og dens komplikationer. Cinnamaldehyd er en gul og tyktflydende væske, der udgør 98 % af den æteriske olie fra kanelbark, og som først blev isoleret af Dumas og Péligot og derefter syntetiseret i laboratoriet af den italienske kemiker Luigi Chiozza (1828-1889) i 1854. I 2007 rapporterede Subash et al. for første gang om en hypoglykæmisk og hypolipidæmisk virkning af cinnamaldehyd på streptozotocin (STZ)-inducerede diabetiske Wistar-rotter af hankøn. Cinnamaldehyd er siden blevet undersøgt indgående i dyremodeller af diabetes og fedme.
Cassia eller kinesisk kanel er et meget anvendt krydderi, der udvindes af den indre bark af kaneltræet. Cassia er blevet brugt i tusindvis af år til medicinske formål og anses for at være en af de 50 grundlæggende urter i traditionel kinesisk medicin. Flere dele af Cassia-planten anvendes til medicinske formål, herunder roden, barken, bladene og blomsterne. Kanelekstrakter er blevet rapporteret at have forskellige gavnlige virkninger, herunder antiallergiske, antimikrobielle, antivirale, antioxidative, gastrobeskyttende, antiangiogene og anti-Alzheimer-effekter samt insulinlignende biologiske aktiviteter . Kanelekstrakter indeholder flere aktive forbindelser, herunder æteriske olier (cinnamaldehyd og cinnamylaldehyd), tanniner, slim og kulhydrater. Interessant nok viser cinnamaldehyd, også kendt som cinnamylaldehyd, anti-fedmeeffekter ved at reducere lipidakkumulering og nedregulere peroxisome proliferator-aktiveret receptor-γ, CCAAT/enhancer-bindende protein α og sterolregulerende elementbindende protein 1. Desuden hæmmer cinnamaldehyd lipopolysaccharidinduceret mikroglial aktivering ved at målrette low-density lipoproteinreceptor-relateret protein-1. Det blev også rapporteret, at cinnamaldehyd har antimutagene virkninger i kræftceller.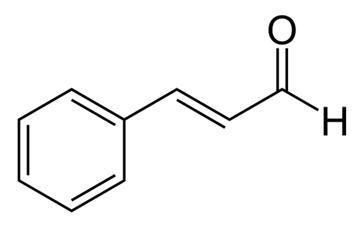
Figur 1 den kemiske struktur af cinnamaldehyd;
Farmakokinetik
Cinnamaldehyd findes naturligt i trans-cinnamaldehyd-form. I et forsøg udført af Zhao et al. vurderes farmakokinetikken af cinnamaldehyd hos rotter ved hjælp af en relativt følsom metode med gaskromatografi-massespektrometri (GC-MS) via oral (500 mg/kg) og intravenøs injektion (i.v., 20 mg/kg) administration. Resultaterne viser, at AUC0-t for cinnamaldehyd ved oral indgift og ved i.v.-indgift er henholdsvis 1984 ± 531 og 355 ± 53 ng h/ml. T1/2 og Tmax for cinnamaldehyd er længere ved oral indgift (6,7 ± 1,5 t og 1,6 ± 0,5 t) end ved i.v.-indgift (1,7 ± 0,3 t og 0,033 t). Cmax er henholdsvis 249 ± 36 ng/ml ved oral indgift og 547 ± 142 ng/ml ved i.v. indgift. Resultaterne tyder på, at biotilgængeligheden af cinnamaldehyd forbedres bedre ved i.v. administration end ved oral administration.
Forfatterne påviser endvidere, at Cmax og AUC0-t er proportionale med dosis (fra 125 til 500 mg), mens Tmax og den gennemsnitlige opholdstid ikke ændres som reaktion på dosiseskalering. I betragtning af at cinnamaldehyd og cinnamylalkohol kan omdannes til hinanden hos rotter, analyserer forfatterne også den farmakokinetiske egenskab af cinnamylalkohol i rotternes plasma. De farmakokinetiske data for cinnamylalkohol er 1105±337 ng-h/ml for AUC0-t, 6,7±2,8 timer for T1/2, 1,5±0,7 timer for Tmax og 221±66 ng/ml for Cmax ved en oral dosis på 500 mg/kg. Interessant nok er methylcinnamat også blevet opdaget i metabolitterne. For farmakokinetiske egenskaber ved methylcinnamat opfordres interesserede læsere til at konsultere Zhao et al.s artikel. Kort sagt er cinnamaldehyd godt fordelt i hele kroppen efter absorption. Cinnamaldehyd har mulighed for at omdanne sig til cinnamylalkohol og kan også oxideres til cinnaminsyre efter at være kommet ind i kroppen. For fuldt ud at forstå de farmakokinetiske egenskaber ved cinnamaldehyd bør methylcinnamat og cinnamylalkohol også bestemmes i plasmaet. Cinnamaldehyds ustabilitet sætter imidlertid spørgsmålstegn ved, at cinnamaldehyds bioaktivitet sandsynligvis skyldes summen af dets metabolitter. Det forventes derfor, at der vil blive gjort yderligere forsøg på at løse disse potentielle problemer. Desuden skal den nyudviklede SMV-cinnamaldehyd med forbedret biotilgængelighed også undersøges nærmere med hensyn til den antidiabetiske virkning.
Anvendelser
Kanelekstrakter har forskellige gavnlige virkninger, herunder antiallergiske, antimikrobielle, antivirale, antioxidative, gastrobeskyttende, antiangiogene og anti-Alzheimer-virkninger samt insulinlignende biologiske aktiviteter. Cinnamaldehyd viser anti-fedmevirkninger ved at reducere lipidakkumulering og nedregulere peroxisome proliferator-aktiveret receptor-γ, CCAAT/enhancer-bindende protein α og sterolregulerende elementbindende protein 1. Desuden hæmmer cinnamaldehyd lipopolysaccharidinduceret mikroglialaktivering ved at målrette low-density lipoproteinreceptor-relateret protein-1. Det blev også rapporteret, at cinnamaldehyd har antimutagene virkninger i kræftceller. Effekten af cinnamaldehyd ved behandling af kræft og diabetes er fremhævet nedenfor:
Kræft
Kwon et al. rapporterede for første gang, at kanelekstrakter inducerer in vitro og in vivo melanomcelledød gennem hæmning af NF-κB og AP-1. En efterfølgende undersøgelse viste, at HCA er den vigtigste antitumorigene forbindelse, der findes i kanelekstrakter, og at den udøver sine væksthæmmende virkninger i 29 typer humane kræftceller in vitro og i SW620 humane tumor xenografts in vivo.
Andre forskergrupper har også rapporteret om antitumorigene virkninger af kanelekstrakter. De hæmmer melanomkræftceller ved at inducere ekspressionen af pro-angiogene faktorer; de forbedrede også de antitumorigene aktiviteter af CD8 T-celler ved at øge deres cytolytiske aktivitet. Kanelekstrakter hæmmer også vaskulær endothelial vækstfaktor, hvilket blev opdaget ved at screene forbindelser for deres hæmmende aktivitet mod VEGFR2. De fleste af de antitumorigene virkninger af kanelekstrakter kan tilskrives cinnamaldehyderne, hovedkomponenten i den æteriske olie, der er ansvarlig for smagen og aromaen af hele kanel. Det blev rapporteret, at kanelamaldehyder hæmmer kræftcellers proliferation ved at hæmme cyclin D1 i flere typer tumorer. Kanelaldehyder fremkalder også apoptose ved at generere reaktive oxygenarter i HL-60 leukæmiceller og gennem aktivering af proapoptotiske Bcl-2-familieproteiner og MAPK-signalvejen i humane hepatomceller. Desuden viste dimeriske cinnamaldehyder afledt af HCA større antitumorigene virkninger end monomeriske cinnamaldehyder ved at inducere apoptose og cellecyklusstop. Desuden har en række undersøgelser vist, at de antitumorigene virkninger af HCA og dets derivater formidles gennem flere molekylære mekanismer. En nylig undersøgelse viste, at polyfenoler med et cinnamaldehyd-stillads udløste cellecyklusstop i G2/M-fasen og apoptotisk celledød i cisplatinresistente humane ovariecancerceller, hvilket tyder på, at cinnamaldehydforbindelser kunne være effektive i kombinationskemoterapier til kræftpatienter. Samlet set er de molekylære mekanismer, der ligger til grund for de kræftbekæmpende og antimetastatiske virkninger af cinnamaldehyder, forskellige, hvilket tyder på, at cinnamaldehyd er en multitargeting-forbindelse. Forskellige kræfters differentierede reaktionsevne på forskellige cinnamaldehydderivater skal evalueres for at muliggøre udvælgelse af den mest effektive forbindelse for hver enkelt kræfttype.
Anti-diabetes
Der er i løbet af de seneste årtier blevet udført nye undersøgelser for at evaluere dens gavnlige rolle i forvaltningen af diabetes og dens komplikationer. Det er påvist, at oral indgivelse af cinnamaldehyd fra 20 mg/kg-kropsvægt til 40 mg/kg-BW pr. dag i en periode på mellem 21 og 60 dage resulterede i en betydelig forbedring af blodglukose- og glykosyleret hæmoglobinniveauer samt insulinfølsomhed hos STZ-inducerede diabetiske rotter. Og 20 mg/kg-BW antages at være den effektive dosis til at forebygge udviklingen af diabetes hos dyr. Endvidere øger cinnamaldehydbehandling i 4 uger plasmainsulinniveauerne og leverglykogenindholdet samt nedsætter triglycerid- og low-density lipoprotein-cholesterolniveauerne hos STZ- og/eller HFD-insulterede Wistar-hanrotter. Camacho et al. fandt endvidere, at administration med cinnamaldehyd i 5 uger til HFD-fodrede C57BL/6J-mus signifikant førte til en reduktion af tilvæksten i kropsfedtmasse. De hævdede dog, at behandling med cinnamaldehyd ikke ændrede plasma fastende insulinniveauer og foderforbrug. Årsagen til denne uoverensstemmelse med hensyn til insulinregulering kan tilskrives, at den genetiske baggrund for C57BL/6J-mus er ændret i nogle produktionsanlæg. De forskellige understammer af mus kan udvise betydelige forskelle i fænotyperne. Desuden kan cinnamaldehyd muligvis udvise glukosesænkende virkning ved at forbedre insulinfølsomheden i periferien i Camachos undersøgelse.
Cinnamaldehyd har evnen til at forbedre diabetisk fedtvæv ved at reducere visceral fedtaflejring og fremme lipolyse og fedtsyreoxidation og termogenese, hvilket er forbundet med en opregulering af energiforbrugsgener, en hæmning af PPARγ/CEBP-α og SREBP1, en opregulering af HSL og PNPLA2 og MGL, en induktion af AMPK-fosforylering og en stigning i Cpt1a i WAT og Acsl4 i BAT, samt en stimulering af det sympatiske nervesystem. Desuden forhindrer cinnamaldehyd ekspression af inflammatoriske gener og forbedrer GLUT-ekspressionen hos diabetiske dyr. Cinnamaldehyd kan beskytte mod diabetes ved at forbedre insulinfølsomheden og glukoseoptagelsen gennem regulering af PI3K/IRS-1 og RBP4-GLUT4-vejen i skeletmuskelvæv samt regulering af mitokondriernes metabolisme gennem PGC-1α/MEF2/GLUT4-vejen i C2C12-celler. Cinnamaldehyd har også positive virkninger på diabetisk lever ved at forbedre glykogensyntesen ved at regulere aktiviteterne af PK og PEPCK og sænke RBP4-niveauet samt normalisere de afvigende leverenzymer, hvilket tyder på en gavnlig rolle af denne forbindelse i glukosemetabolismen og insulinfølsomheden i diabetisk lever.
Antimikrobielle virkninger
Undersøgelser har bekræftet den antimikrobielle aktivitet af cinnamaldehyd, nelliker, timian og rosmarin over for E. coli O157:H7 og Salmonella. Wendakoon og Sakaguchi rapporterede, at cinnamaldehyds carbonylgruppe binder sig til proteinerne og forhindrer aminosyre-decarboxylaseaktivitet i Enterobacter aerogenes. Smid et al. observerede, at Saccharomyces cerevisiae’s cytoplasmiske membran blev beskadiget ved behandling med cinnamaldehyd, hvilket førte til overdreven udsivning af metabolitter og enzymer fra cellen og til sidst til tab af levedygtighed. De fleste undersøgelser har antydet, at de æteriske oliers virkemåde afhænger af typen af mikroorganismer, hovedsagelig af deres cellevægstruktur og deres ydre membranarrangement. De observerede skader på grund af de betydelige forskelle i de ydre membraner hos gram-negative og gram-positive bakterier.
Toksicitet
Selv i dag antages cinnamaldehyd stadig at være et sikkert naturligt ingrediensstof, der tolereres godt af mennesker og dyr. Begrebet er også godt accepteret af FDA og Europarådet med forslag om et acceptabelt dagligt indtag på 1,25 mg/kg.
Akut toksicitet
Cinnamaldehyd rapporteres at have den høje sikkerhedsmargin, og administreret 20 gange den effektive dosis(20 mg/kg) af denne forbindelse forårsagede ikke unormale adfærdsmæssige tegn og forstyrrede serumkemiske værdier i hele undersøgelsen. Den akutte toksicitet af cinnamaldehyd er lav, med orale værdier for median letal dosis(LD50), der varierer fra en lav værdi på 0,6 g/kg BW til en høj værdi på 3,4 g/kg BW hos forskellige arter.
Langtidstoksicitet
Resultaterne af en tre måneders undersøgelse viser, at kropsvægten er reduceret hos hunrotter, der udsættes for 16.500 eller 33.000 ppm, og hos hunmus, der udsættes for 8200 ppm eller mere. Desuden er foderforbruget reduceret i alle udsatte grupper af rotter og i den højeste dosisgruppe af mus. Endvidere øger eksponering for cinnamaldehyd forekomsten af pladeepithelial hyperplasi i forstuvet mave. Desuden udviser mus, der udsættes for cinnamaldehyd, også en øget forekomst af olfaktorisk epitheldegeneration i næsehulen. Alle rotter overlevede i hele undersøgelsen på tre måneder.
Andre
Cinnamaldehyd kan også vise cytotoksiske virkninger i F344 rottehepatocytter, hvilket fremgår af udtømning af glutathionniveauet, og i HepG2-celler, hvilket fremgår af et stigende antal mikronukleus. Behar et al. undersøgte den potentielle toksicitet af dette produkt i humane embryonale celler og lungeceller. Resultaterne viser, at behandling med cinnamaldehyd depolymeriserer mikrotubuli i humane lungefibroblaster. Cinnamaldehyd nedsætter også celleproliferation og -differentiering ved at hæmme cellevækst og -differentiering og ved at ændre cellens morfologi og motilitet samt øge DNA-strengsbrud og celledød. En undersøgelse udført af Olsen et al. viser, at cinnamaldehyd virker hudirriterende ved at øge den kolde smertetærskel og sænke den mekaniske smertetærskel samt ved at øge hudens temperatur og perfusion hos mennesker.
- Zhou M, Chen Z, Shen S. Recent advanceson cinnamaldehyde. Journal of Economic Animal 2015;19:1-5.
- Khare P, Jagtap S, Jain Y, Baboota RK, Mangal P, Boparai RK, Bhutani KK, Sharma SS, Premkumar LS, Kondepudi KK, Chopra K, Bishnoi M. Cinnamaldehydtilskud forhindrer fastende induceret hyperfagi, lipidakkumulering og inflammation hos mus fodret med fedtholdig diæt. BioFactors 2016;42:201-211.
- Ma R, Zhu R, Wang L, Guo Y, Liu C, Liu H, Liu F, Li H, Li Y, Fu M, Zhang D. Diabetisk osteoporose: En gennemgang af brugen af traditionel kinesisk medicin samt klinisk og præklinisk forskning. Evidence-based complementary and alternative medicine : eCAM 2016;2016;2016:3218313.
- Dumas JP, E. Organic chemistry research – on cinnamon oil, the hippuric acid and sebacic acid. Annales de chimie et de physique 1834;57:305-334.
- Chiozza L. Sur la production artificielle de l´essence de cannelle”. Comptes rendus 1856;42:222-227.
- Subash Babu P, Prabuseenivasan S, Ignacimuthu S. Cinnamaldehyde–et potentielt antidiabetisk middel. Phytomedicine : international journal of phytotherapy and phytopharmacology 2007;14:15-22.
- Hagenlocher Y, Bergheim I, Zacheja S, Schaffer M, Bischoff SC, Lorentz A. 2013. Kanelekstrakt hæmmer degranulering og de novo-syntese af inflammatoriske mediatorer i mastceller. Allergy 68: 490-497.
- Matan N, Rimkeeree H, Mawson AJ, Chompreeda P, Haruthaithanasan V, Parker M. 2006. Antimikrobiel aktivitet af kanel- og nellikeolier under modificerede atmosfæreforhold. Int J Food Microbiol 107: 180-185.
- Fink RC, Roschek B Jr, Alberte RS. 2009. HIV type-1 indgangshæmmere med en ny virkemåde. Antivir Chem Chem Chemother 19: 243-255.
- Yang CH, Li RX, Chuang LY. 2012. Antioxidant aktivitet af forskellige dele af Cinnamomum cassia ekstraheret med forskellige ekstraktionsmetoder. Molecules 17: 7294-7304.
- Peterson DW et al. 2009. Kanelekstrakt hæmmer tau-aggregation forbundet med Alzheimers sygdom in vitro. J Alzheimers Dis 17: 585-597.
- Cheng DM, Kuhn P, Poulev A, Rojo LE, Lila MA, Raskin I. 2012. In vivo og in vitro antidiabetiske virkninger af vandigt kanelekstrakt og kanelpolyphenolforstærket fødevarematrix. Food Chem 135: 2994-3002.
- Kim JE et al. 2015a. Et nyt kanelrelateret naturprodukt med Pim-1-hæmmende aktivitet hæmmer leukæmi og hudkræft. Cancer Res 75: 2716-2728.
- Hwang H et al. 2011. 2′-Hydroxycinnamaldehyd er målrettet low-density lipoproteinreceptorrelateret protein-1 for at hæmme lipopolysaccharid-induceret mikroglial aktivering. J Neuroimmunol2011 230: 52-56.
- Shaughnessy DT, Setzer RW, DeMarini DM. 2001. Den antimutagene virkning af vanillin og cinnamaldehyd på spontan mutation i Salmonella TA104 skyldes en reduktion i mutationer på GC-, men ikke AT-steder. Mutat Res 480: 55-69.
- Zhang LQ, Zhang ZG, Fu Y, Xu Y. Forskningsfremskridt inden for trans-cinnamaldehyds farmakologiske virkninger. Zhongguo Zhong yao za zhi = Zhongguo zhongyao zazhi = China journal of Chinese materia medica 2015;40:4568-4572.
- Kwon BM et al. 1998. Syntese og in vitro cytotoksicitet af cinnamaldehyder over for humane solide tumorceller. Arch Pharm Res 21: 147-152.
- Lee CW et al. 1999. Hæmning af menneskelig tumorvækst af 2′-hydroxyog 2′-benzoyloxycinnamaldehyder. Planta Med 65: 263-266
- Kwon HK et al. 2009. Kanelekstrakt undertrykker tumorprogression ved at modulere angiogenese og effektorfunktionen af CD8+ T-celler. Cancer Lett 278: 174-182.
- Lu J, Zhang K, Nam S, Anderson RA, Jove R,WenW. 2010. Ny angiogenesehæmmende aktivitet i kanelekstrakt blokerer VEGFR2-kinase og downstream-signalering. Carcinogenesis 31: 481-488.
- Jeong HW et al. 2000. Kanelamaldehyder hæmmer cyclinafhængig kinase 4/cyclin D1. Bioorg Med Chem Lett 10: 1819-1822.
- Ka H et al. 2003. Cinnamaldehyd inducerer apoptose ved ROS-medieret mitokondriel permeabilitetsovergang i humane promyelocytiske leukæmiceller HL-60-celler. Cancer Lett 196: 143-152.
- Wu SJ, Ng LT, Lin CC. 2005. Cinnamaldehyd-induceret apoptose i humane PLC/PRF/5-celler gennem aktivering af de proapoptotiske Bcl-2-familieproteiner og MAPK-vejen. Life Sci 77: 938-951.
- Shin DS et al. 2006. Syntese og biologisk evaluering af dimeriske cinnamaldehyder som potente antitumormidler. Bioorg Med Chem 14: 2498-2506.
- Shin SY et al. 2014. Polyphenoler, der bærer cinnamaldehyd-saffold, viser cellevæksthæmmende virkninger på cisplatinresistente A2780/Cis ovariecancerceller. Bioorg Med Chem 22: 1809-1820.
- Lee SC, Xu WX, Lin LY, Yang JJ, Liu CT. Kemisk sammensætning og hypoglykæmisk og bugspytkirtelbeskyttende virkning af æterisk olie fra blade af indfødt kanel. Journal of agricultural and food chemistry 2013;61:4905-4913.
- El-Bassossy HM, Fahmy A, Badawy D. Cinnamaldehyde beskytter mod forhøjet blodtryk i forbindelse med diabetes. Food and chemical toxicology : an international journal published for the British Industrial Biological Research Association 2011;49:3007-3012.
- Li M, Xu Y, Zhang W. Effekter af cinnamaldehyd på ekspressionsniveauet af irs-1 og p85 alpha i gastrocnemius hos type 2 diabetiske rotter. Medical Journal of Wuhan University 2009;30:723-726=731.
- Kumar S, Vasudeva N, Sharma S. Gc-ms-analyse og screening af antidiabetisk, antioxidant- og hypolipidæmisk potentiale af cinnamomum tamala-olie i streptozotocininduceret diabetes mellitus hos rotter. Cardiovascular diabetology 2012;11;11:95.
- Camacho S, Michlig S, de Senarclens-Bezencon C, Meylan J, Meystre J, Pezzoli M, Markram H, le Coutre J. Anti-fedme og anti-hyperglykæmiske virkninger af cinnamaldehyd via ændret ghrelin-sekretion og funktionel indvirkning på fødeindtagelse og gastrisk tømning. Scientific reports 2015;5;5:7919.
- Navarro SJ, Trinh T, Lucas CA, Ross AJ, Waymire KG, Macgregor GR. Den c57bl/6j-musestammebaggrund modificerer effekten af en mutation i bcl2l2. G3 2012;2:99-102.
- Mekada K, Abe K, Murakami A, Nakamura S, Nakata H, Moriwaki K, Obata Y, Yoshiki A. Genetiske forskelle mellem c57bl/6-understammer. Experimental animals 2009;58:141-149.
- Kiselycznyk C, Holmes A. All mice are not created equal. Frontiers in neuroscience 2011;5:10.
- Attane C, Peyot ML, Lussier R, Zhang D, Joly E, Madiraju SR, Prentki M. Differential insulin sekretion of high-fat diet-fed c57bl/6nn and c57bl/6nj mice: Implikationer af blandet genetisk baggrund i metaboliske undersøgelser. PloS one 2016;11:e0159165.
- Nicholas P G, Schnuckc. JK, Mermierd. CM, Conne. CA, Vaughanc. RA. Trans-cinnamaldehyd stimulerer mitokondriel biogenese gennem pgc-1α og pparβ/δ, der fører til øget glut4-ekspression. Biochimie 2015;119;119:45-51.
- Zhang W, Xu YC, Guo FJ, Meng Y, Li ML. Anti-diabetiske virkninger af cinnamaldehyd og berberin og deres indvirkning på retinolbindende protein 4-ekspression i rotter med type 2-diabetes mellitus. Chin Med J 2008;121:2124-2128.
- Bandyopadhyay GK, Yu JG, Ofrecio J, Olefsky JM. Øget p85/55/50-ekspression og nedsat phosphotidylinositol 3-kinase-aktivitet i insulinresistent menneskelig skeletmuskel. Diabetes 2005;54;54:2351-2359.
- Saraswathi V, Ramnanan CJ, Wilks AW, Desouza CV, Eller AA, Murali G, Ramalingam R, Milne GL, Coate KC, Edgerton DS. Virkning af hæmatopoietisk cyclooxygenase-1-mangel på fedme-relateret fedtvævsbetændelse og metaboliske forstyrrelser hos mus. Metabolism: clinical and experimental 2013;62;62:1673-1685.
- Ohaeri OC. Effekt af hvidløgsolie på niveauerne af forskellige enzymer i serum og væv hos streptozotocin diabetiske rotter. Bioscience reports 2001;21;21:19-24.
- Mahfouz MH, Assiri AM, Mukhtar MH. Vurdering af neutrofilt gelatinase-associeret lipocalin (ngal] og retinolbindende protein 4 hos type 2-diabetiske patienter med nefropati. Biomarker insights 2016;11;11:31-40.
- SHAN, B., CAY, Y.-Z., BROOKS, J.D. og CORKE, H. 2007. Antibakterielle egenskaber og de vigtigste bioaktive komponenter i kanelstang: Aktivitet mod fødevarebårne patogene bakterier. J. Agric. Food Chem. 55, 5484-5490
- RHAYOUR, K., BOUCHIKHI, T., TANTAOUI-ELARAKI, A., SENDIDE, K. og REMMAL, A. 2003. Mekanismen for bakteriedræbende virkning af æteriske olier af oregano og nellike og deres phenoliske hovedbestanddele på Escherichia coli og Bacillus subtilis. J. Essent. Oil Res. 15, 356-362.
- KIM, H.-O., PARK, S.-W. og PARK, H.-D. 2004. Inaktivering af Escherichia coli O157:H7 med cinnamisk aldehyd oprenset fra Cinnamomum cassia-skud. Food Microbiol. 21, 105-110
- WENDAKOON, C. og SAKAGUCHI, M. 1995. Hæmning af aminosyre-decarboxylaseaktivitet hos Enterobacter aerogenes af aktive komponenter i krydderier. J. Food Prot. 58, 280-283.
- SMID, E.J., KOEKEN, J.P.G. og GORRIS, L.G.M. 1996. Fungicidal og fungistatisk virkning af de sekundære plantemetabolitter cinnamaldehyd og carvone. I Modern Fungicides and Antimicrobial Compounds pp. 173-180, Intercept, Andover, U.K.
- Dugoua JJ, Seely D, Perri D, Cooley K, Forelli T, Mills E, Koren G. From type 2 diabetes to antioxidant activity: En systematisk gennemgang af sikkerheden og virkningen af almindelig kanelbark og cassia kanelbark. Canadian journal of physiology and pharmacology 2007;85:837-847.
- Anand P, Murali KY, Tandon V, Murthy PS, Chandra R. Insulinotropisk virkning af cinnamaldehyd på transkriptionel regulering af pyruvatkinase, phosphoenolpyruvatcarboxykinase og glut4-translokation i eksperimentelle diabetiske rotter. Chemico-biologiske interaktioner 2010;186;186:72-81.
- Gowder SJT. Sikkerhedsvurdering af fødevarearoma -cinnamaldehyd. Biosafety 2014;3
- Hooth MJ, Sills RC, Burka LT, Haseman JK, Witt KL, Orzech DP, Fuciarelli AF, Graves SW, Johnson JD, Bucher JR. Toksikologiske og kræftfremkaldende undersøgelser af mikroindkapslet trans-cinnamaldehyd hos rotter og mus. Food and chemical toxicology : an international journal published for the British Industrial Biological Research Association 2004;42:1757-1768.
- Swales NJ, Caldwell J. Studies on trans-cinnamaldehyde ii: Mechanisms of cytotoxicity in rat isolated hepatocytes. Toxicology in vitro : an international journal published in association with BIBRA 1996;10:37-42.
- Sanyal R, Darroudi F, Parzefall W, Nagao M, Knasmuller S. Inhibition of the genotoxic effects of heterocyclic amines in human derived hepatoma cells by dietary bioantimutagens. Mutagenesis 1997;12:297-303.
- Behar RZ, Luo W, Lin SC, Wang Y, Valle J, Pankow JF, Talbot P. Distribution, kvantificering og toksicitet af cinnamaldehyd i væsker og aerosoler til genopfyldning af elektroniske cigaretter. Tobacco control 2016
- Olsen RV, Andersen HH, Møller HG, Eskelund PW, Arendt-Nielsen L. Somatosensoriske og vasomotoriske manifestationer af individuel og kombineret stimulering af trpm8 og trpa1 ved hjælp af topisk l-menthol og trans-cinnamaldehyd hos raske frivillige. European journal of pain 2014;18:1333-1342.
Zhao H, Xie Y, Yang Q, Cao Y, Tu H, Cao W, Wang S. Farmakokinetisk undersøgelse af cinnamaldehyd hos rotter ved gc-ms efter oral og intravenøs administration. Journal of pharmaceutical and biomedical analysis 2014;89;89:150-157.
Kemiske egenskaber
trans-Cinnamaldehyd er hovedbestanddel af cassiaolie (ca. 90 %) og kanelbarkolie fra Sri Lanka (ca. 75 %). Mindre mængder findes i mange andre æteriske olier. I naturen er den trans-isomer fremherskende.
trans-Cinnamaldehyd er en gullig væske med en karakteristisk krydret lugt, der minder stærkt om kanel. Da det er en ???,??-umættet aldehyd, gennemgår det mange reaktioner, hvoraf hydrogenering til cinnamisk alkohol, dihydrocinnamaldehyd og dihydrocinnamisk alkohol er vigtig. Cinnaminsyre dannes ved autoxidation.
I industriel målestok fremstilles cinnamaldehyd næsten udelukkende ved alkaliske kondensation af benzaldehyd og acetaldehyd. Selvkondensering af acetaldehyd kan undgås ved at anvende et overskud af benzaldehyd og ved langsomt at tilsætte acetaldehyd.
Cinnamaldehyd anvendes i mange sammensætninger til at skabe krydrede og orientalske noter (f.eks. sæbeparfumer). Det er den vigtigste bestanddel af kunstig kanelolie. Desuden er det et vigtigt mellemprodukt i syntesen af kanelalkohol og dihydrocinnamisk alkohol.
Kemiske egenskaber
KLAR GULLIG VÆSKE
Kemiske egenskaber
Brændbar, gullig, olieagtig væske (tykner ved udsættelse for luft). Stærk skarp, krydret, kanelagtig lugt.
Definition
ChEBI: E-stereoisomeren (trans) af cinnamaldehyd, som er moderen i klassen af cinnamaldehyder.
Syntese Reference(r)
Chemistry Letters, 12, s. 1207, 1983
Journal of the American Chemical Society, 93, s. 2080, 1971 DOI: 10.1021/ja00737a057
Tetrahedron Letters, 18, s. 1215, 1977
Generel beskrivelse
Klar gul væske med en lugt af kanel og en sødlig smag.
Luft &Vand Reaktioner
Kan være følsom over for længere tids udsættelse for luft og lys. Uopløseligt i vand.
Reaktivitetsprofil
trans-Cinnamaldehyd er uforeneligt med stærke oxideringsmidler og stærke baser. trans-Cinnamaldehyd kan også reagere med natriumhydroxid.
Brandfare
trans-Cinnamaldehyd er brandfarligt.
Potentiel eksponering
Botanisk fungicid og insekticid. Anvendes som svampedræbende middel, tiltrækningsmiddel for majsrodorm og hunde- og katteafvisende middel. Kan anvendes på jorddække til svampe, rækkeafgrøder, græsplæne og alle fødevarer. Ikke opført til brug i EU-lande.
Sendelse
UN1989 Aldehyder, n.o.s., Fareklasse: 3; Etiketter: 3-Brændbar væske
Inkompatibiliteter
Aldehyder er ofte involveret i selvkondensations- eller polymerisationsreaktioner. Disse reaktioner er eksoterme; de er ofte katalyseret af syre. Aldehyder oxideres let til carboxylsyrer. Brandfarlige og/eller giftige gasser dannes ved kombination af aldehyder med azo- og diazoforbindelser, dithiocarbamater, nitrider og stærke reduktionsmidler. Aldehyder kan reagere med luft og først give peroxosyrer og til sidst carboxylsyrer. Disse autoxidationsreaktioner aktiveres af lys, katalyseres af salte af overgangsmetaller og er autokatalytiske (katalyseres af reaktionens produkter). Tilsætning af stabilisatorer (antioxidanter) til forsendelser af aldehyder forsinker autoxidationen. Ukompatibel med oxidationsmidler (chlorater, nitrater, peroxider, permanganater, perchlorater, klor, brom, fluor osv.); kontakt kan forårsage brand eller eksplosioner. Holdes væk fra alkaliske materialer, stærke baser, stærke syrer, oxosyrer, epoxider, ketoner, azofarvestoffer, kaustika, boraner, hydraziner
Affaldsbortskaffelse
Forbrænding. I overensstemmelse med 40CFR165 skal anbefalingerne for bortskaffelse af pesticider og pesticidbeholdere følges.