
Oprindelsen af J-kobling kan visualiseres ved hjælp af en vektormodel for et simpelt molekyle som hydrogenfluorid (HF). I HF har de to kerner spin 1/2. Fire tilstande er mulige, afhængigt af den relative tilpasning af H- og F-kerne-spinene til det ydre magnetfelt. NMR-spektroskopiens udvælgelsesregler foreskriver, at ΔI = 1, hvilket betyder, at en given foton (i radiofrekvensområdet) kun kan påvirke (“vende”) et af de to kernespind.J-kobling giver tre parametre: multipliciteten (“antallet af linjer”), koblingens størrelse (stærk, middel, svag) og koblingens fortegn.
MultiplicitetRediger
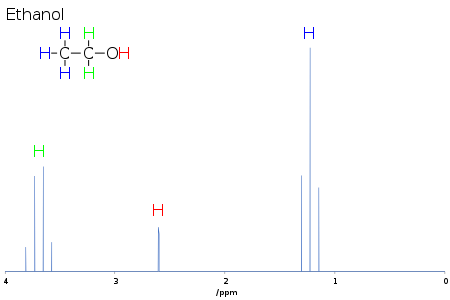
Multiplicippet giver oplysninger om antallet af centre, der er koblet til det pågældende signal, og deres kernespin. For simple systemer, som ved 1H-1H-kobling i NMR-spektroskopi, er multipliciteten én mere end antallet af tilstødende protoner, som er magnetisk ikke-ækvivalente med de pågældende protoner. For ethanol er hver methylproton koblet til de to methylenprotoner, så methylsignalet er en triplet. Og hver methylenproton er koblet til de tre methylprotoner, så methylensignalet er en kvartet.
Nuclei med spins større end 1/2, som kaldes quadrupolære, kan give anledning til større splitting, selv om kobling til quadrupolære kerner i mange tilfælde ikke observeres. Mange grundstoffer består af kerner med kernespin og uden kernespin. I disse tilfælde er det observerede spektrum summen af spektrer for hver isotopomer. En af de store fordele ved NMR-spektroskopi for organiske molekyler er, at flere vigtige kerner med lettere spin 1/2 enten er monoisotopiske, f.eks. 31P og 19F, eller har meget stor naturlig hyppighed, f.eks. 1H. En yderligere fordel er, at 12C og 16O ikke har noget kernespin, så disse kerner, som er almindelige i organiske molekyler, forårsager ikke splittingmønstre i NMR.
Størrelsen af J-koblingRediger
For 1H-1H-kobling giver størrelsen af J oplysninger om koblingspartnernes nærhed. Generelt set er tobindingskobling (dvs. 1H-C-1H) stærkere end trebindingskobling (1H-C-C-C-1H). Størrelsen af koblingen giver også oplysninger om de dihedralvinkler, der forbinder koblingspartnerne, som beskrevet af Karplus-ligningen for trebindingskoblingskonstanter.
For heteronuklear kobling er størrelsen af J relateret til koblingspartnernes kernemagnetiske momenter. 19F, med et højt kernemagnetisk moment, giver anledning til stor kobling til protoner. 103Rh, med et meget lille kernemagnetisk moment, giver kun små koblinger til 1H. For at korrigere for virkningen af det kernemagnetiske moment (eller tilsvarende det gyromagnetiske forhold γ) diskuteres ofte den “reducerede koblingskonstant” K, hvor
K = 4π2J/hγxγy.
For kobling af en 13C-kerne og en direkte bundet proton er det dominerende udtryk i koblingskonstanten JC-H Fermi-kontaktvekselvirkningen, som er et mål for s-karakteren af bindingen ved de to kerner.
Hvor det ydre magnetfelt er meget lavt, f.eks. som f.eks. ved NMR i jordfeltet, dominerer J-koblingssignaler i størrelsesordenen hertz normalt de kemiske forskydninger, som er i størrelsesordenen millihertz og normalt ikke kan opløses.
Tegn på J-koblingRediger
Værdien af hver koblingskonstant har også et fortegn, og koblingskonstanter af sammenlignelig størrelse har ofte modsat fortegn. Hvis koblingskonstanten mellem to givne spins er negativ, er energien lavere, når disse to spins er parallelle, og omvendt, hvis deres koblingskonstant er positiv. For et molekyle med en enkelt J-koblingskonstant er NMR-spektret uændret, hvis koblingskonstantens fortegn er omvendt, selv om spektrallinjer på bestemte positioner kan repræsentere forskellige overgange. Det simple NMR-spektrum angiver derfor ikke koblingskonstantens fortegn, som der ikke er nogen enkel måde at forudsige.
For nogle molekyler med to forskellige J-koblingskonstanter kan de to konstanters relative fortegn imidlertid eksperimentelt bestemmes ved et dobbeltresonansforsøg. For eksempel i diethylthallium-ionen (C2H5)2Tl+ viste denne metode, at methyl-thallium (CH3-Tl) og methylen-thallium (CH2-Tl) koblingskonstanterne har modsat fortegn.
Den første eksperimentelle metode til bestemmelse af det absolutte fortegn for en J-koblingskonstant blev foreslået i 1962 af Buckingham og Lovering, som foreslog anvendelse af et stærkt elektrisk felt til at tilpasse molekylerne i en polær væske. Feltet frembringer en direkte dipolær kobling af de to spins, som føjer sig til den observerede J-kobling, hvis deres fortegn er parallelle, og trækker sig fra den observerede J-kobling, hvis deres fortegn er modsatrettede. Denne metode blev først anvendt på 4-nitrotoluen, for hvilket J-koblingskonstanten mellem to tilstødende (eller ortho) ringprotoner blev vist at være positiv, fordi opdelingen af de to to toppe for hver proton falder med det anvendte elektriske felt.
En anden måde at tilpasse molekyler til NMR-spektroskopi er at opløse dem i et opløsningsmiddel i en nematisk flydende krystal. Denne metode er også blevet anvendt til at bestemme det absolutte fortegn for J-koblingskonstanter.