
Typ dine eksempler her.
- 9.1 Signalmolekyler og cellulære receptorer
- 9.2 Udbredelse af signalet
- 9.3 Reaktion på signalet
Forestil dig, hvordan livet ville være, hvis du og de mennesker omkring dig ikke kunne kommunikere. Du ville ikke kunne udtrykke dine ønsker over for andre, og du ville heller ikke kunne stille spørgsmål for at finde ud af mere om dine omgivelser. Den sociale organisation er afhængig af kommunikation mellem de individer, der udgør dette samfund.
Som med mennesker er det afgørende for de enkelte celler at kunne interagere med deres omgivelser og med hinanden. Dette gælder, uanset om en celle vokser alene i en dam eller om den er en af mange celler, der udgør en større organisme. For at kunne reagere korrekt på eksterne stimuli har cellerne udviklet komplekse kommunikationsmekanismer, så de kan modtage en besked, overføre informationen over plasmamembranen og derefter producere ændringer i cellen som reaktion på beskeden.
I flercellede organismer sender og modtager cellerne konstant kemiske beskeder for at koordinere andre organers, vævers og cellers handlinger. Evnen til at sende meddelelser hurtigt og effektivt gør det muligt for cellerne at koordinere og finjustere deres funktioner. Selv om nødvendigheden af cellulær kommunikation i større organismer synes indlysende, kommunikerer selv encellede organismer med hinanden. Gærceller sender signaler til hinanden for at hjælpe hinanden med at parre sig. Nogle former for bakterier koordinerer deres handlinger for at danne store komplekser kaldet biofilm eller for at organisere produktionen af toksiner for at fjerne konkurrerende organismer. Cellernes evne til at kommunikere gennem kemiske signaler opstod i enkeltceller og var afgørende for udviklingen af flercellede organismer. Effektiv, fejlfri kommunikation er afgørende for alt liv.
- 9.1 | Signalmolekyler og cellulære receptorer
- 9.1.1.1 Signalformer
- Paracrine signalering
- Autokrin signalering
- Endokrin signalering
- Direkte signalering
- 9.1.2 Typer af receptorer
- Interne receptorer
- Cell-surface-receptorer
- 9.1.3 Signalmolekyler
- Små hydrofobiske ligander
- Vandopløselige ligander
- 9.2 | Signalets udbredelse
- 9.2.2.1 Signalveje og signalforstærkning
- 9.2.2 Metoder til intracellulær signalering
- Fosforylering
- Sekundbudbringere
- 9.3 | Svar på signalet
- 9.3.3.1 Reaktioner på signalvejen
- Genekspression
- Stigning i cellulær metabolisme
- Cellevækst
- Celledød
- 9.3.2 Afslutning af signalveje
9.1 | Signalmolekyler og cellulære receptorer
Ved afslutningen af dette afsnit vil du kunne:
- Beskriv fire typer af signalering, der findes i flercellede organismer.
- Sammenligne interne receptorer med receptorer på celleoverfladen.
- Kend forholdet mellem en ligands kemi og dens virkningsmekanisme.
Der findes to former for kommunikation i den levende celleverden. Kommunikation mellem celler kaldes intercellulær signalering, og kommunikation inden for en celle kaldes intracellulær signalering. En nem måde at huske forskellen på er ved at forstå, at præfikset inter- betyder “mellem” (en interstate highway krydser mellem stater) og intra- betyder “inde” (et IV betyder intravenøst eller “inde i venen”).
Kemiske signaler frigives af en signalcelle og modtages af en målcelle. Målceller har proteiner kaldet receptorer, som binder sig til signalmolekyler og forårsager et respons. Signalmolekyler, der binder sig til receptorer, kaldes ligander. Ligander og receptorer er specifikke for hinanden; en receptor vil typisk kun binde sig til sin specifikke ligand. Der findes dog forskellige typer af signalering.
9.1.1.1 Signalformer
Der findes fire kategorier af kemisk signalering i flercellede organismer: autokrin signalering, parakrin signalering, endokrin signalering og direkte signalering over gap junctions (figur 9.2). Den væsentligste forskel mellem de forskellige kategorier af signalering er den afstand, som signalet tilbagelægger for at nå målcellen.
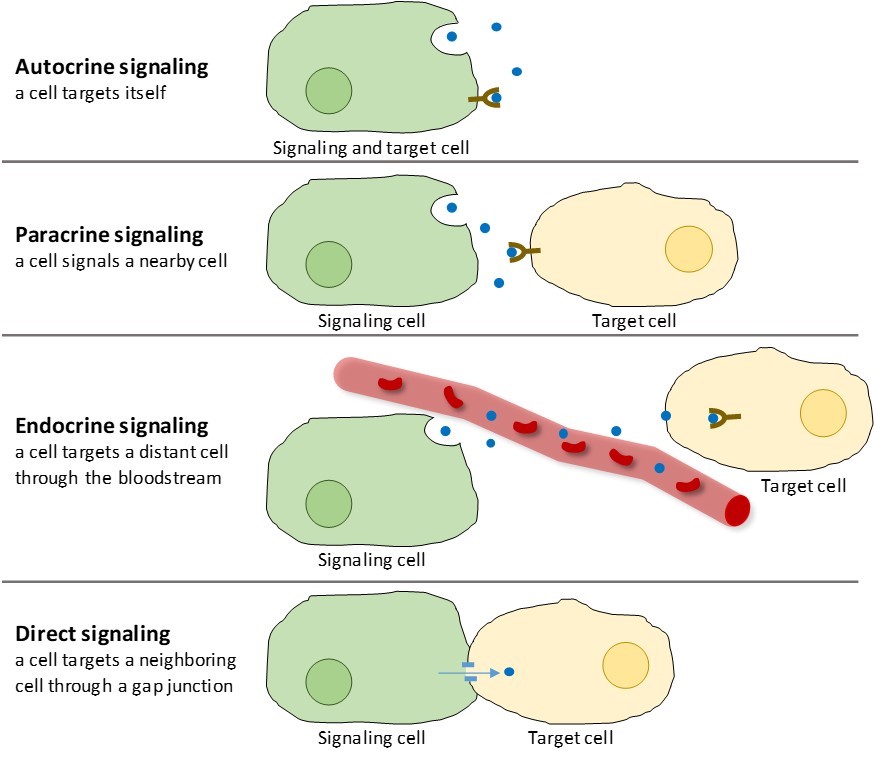
Paracrine signalering
Signaler, der virker lokalt mellem celler, der er tæt på hinanden, kaldes parakrine signaler. Paracrine signaler bevæger sig ved diffusion gennem den ekstracellulære matrix (figur 9.2). Disse typer signaler fremkalder normalt hurtige reaktioner, der kun varer kort tid. For at holde responsen lokaliseret, bliver parakrine ligander normalt hurtigt nedbrudt af enzymer eller fjernet af nabocellerne. Fjernelse af signalerne genetablerer koncentrationsgradienten for signalmolekylet, hvilket gør det muligt for dem at diffundere hurtigt gennem det intracellulære rum, hvis de frigives igen.
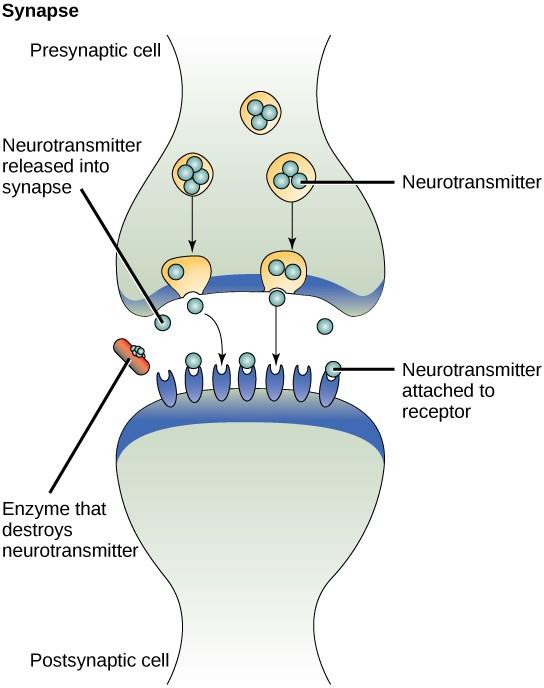
Et eksempel på parakrin signalering er overførsel af signaler mellem nerveceller. Det lille rum mellem nervecellerne, hvor signaloverførslen finder sted, kaldes en synapse. Signalerne spredes langs nervecellerne ved hjælp af hurtige elektriske impulser. Når disse impulser når frem til enden af en nervecelle, frigøres kemiske ligandstoffer, kaldet neurotransmittere, i synapsen af den præsynaptiske celle (den celle, der afgiver signalet). Neurotransmitterne spredes på tværs af synapsen (figur 9.3). Den lille afstand mellem nervecellerne gør det muligt for signalet at rejse hurtigt, hvilket muliggør en øjeblikkelig reaktion, f.eks. “tag din hånd væk fra komfuret!” Når neurotransmitteren binder receptoren på overfladen af den postsynaptiske celle, udløses den næste elektriske impuls. Neurotransmitterne nedbrydes hurtigt eller reabsorberes af den præsynaptiske celle, så den modtagende nervecelle hurtigt kan komme sig og være forberedt på at reagere hurtigt på det næste synaptiske signal.
Autokrin signalering
Når en celle reagerer på sit eget signalmolekyle, kaldes det autokrin signalering (auto = “selv”). Autokrin signalering forekommer ofte sammen med andre typer signalering. Når der f.eks. frigives et parakrint signal, kan den signalgivende celle reagere på signalet sammen med sine naboer (figur 9.2).
Autokrin signalering forekommer ofte under den tidlige udvikling af en organisme for at sikre, at cellerne udvikler sig til de korrekte væv. Autokrin signalering regulerer også smertefornemmelse og inflammatoriske reaktioner. Endvidere kan en celle, hvis den er inficeret med en virus, signalere til sig selv, at den skal gennemgå programmeret celledød, hvorved virussen dræbes i processen.
Endokrin signalering
Signaler fra fjerntliggende celler kaldes endokrine signaler, og de stammer fra endokrine celler. (I kroppen er mange endokrine celler placeret i endokrine kirtler, f.eks. i skjoldbruskkirtlen, hypothalamus og hypofysen). Disse typer signaler giver normalt en langsommere reaktion, men har en længerevarende virkning. De ligander, der frigives ved endokrin signalering, kaldes hormoner, signalmolekyler, der produceres i en del af kroppen, men som påvirker andre kropsregioner et stykke væk (figur 9.2).
Hormoner tilbagelægger de store afstande mellem endokrine celler og deres målceller via blodbanen, som er en relativt langsom måde at bevæge sig i hele kroppen på. På grund af deres transportform bliver hormoner fortyndet og er til stede i lave koncentrationer, når de virker på deres målceller. Dette adskiller sig fra parakrin signalering, hvor de lokale koncentrationer af signalmolekyler kan være meget høje.
Direkte signalering
Gap junctions hos dyr og plasmodesmata hos planter er forbindelser mellem plasmamembranerne i naboceller. Disse vandfyldte kanaler gør det muligt for små signalmolekyler at diffundere mellem de to celler. Små molekyler, som f.eks. calciumioner (Ca2+), kan bevæge sig mellem cellerne, men store molekyler som proteiner og DNA kan ikke passere gennem kanalerne. Kanalernes specificitet sikrer, at cellerne forbliver uafhængige, men at de hurtigt og nemt kan overføre signaler. Direkte signalering gør det muligt for en gruppe af celler at koordinere deres reaktion på et signal, som kun én af dem kan have modtaget. I planter er plasmodesmata allestedsnærværende, hvilket gør hele planten til et gigantisk kommunikationsnetværk.
9.1.2 Typer af receptorer
Receptorer er proteinmolekyler i målcellen eller på dens overflade, der binder sig til ligander. Der findes to typer receptorer, interne receptorer og receptorer på celleoverfladen.
Interne receptorer
Interne receptorer, også kendt som intracellulære eller cytoplasmatiske receptorer, findes i målcellens cytoplasma og reagerer på hydrofobiske ligandmolekyler, der er i stand til at bevæge sig gennem plasmamembranen. Når de er inde i cellen, binder mange af disse molekyler sig til proteiner, der fungerer som regulatorer af mRNA-syntesen (transkription) for at formidle genekspression.
Genekspression er den cellulære proces, hvor informationen i en celles DNA omdannes til en sekvens af aminosyrer, der i sidste ende danner et protein. Når liganden binder til den interne receptor, udløses en konformationsændring, der blotlægger et DNA-bindingssted på receptorproteinet. Ligand-receptorkomplekset bevæger sig ind i kernen og binder sig derefter til specifikke regulerende regioner af kromosom-DNA’et og fremmer initieringen af transkription (figur 9.4). Transkription er den proces, hvor informationen i en celles DNA kopieres til en særlig form for RNA kaldet messenger RNA (mRNA); cellen bruger informationen i mRNA’et til at sammenkæde specifikke aminosyrer i den korrekte rækkefølge og producerer et protein. Når en ligand binder sig til en intern receptor, kan den således direkte påvirke genekspressionen i målcellen.
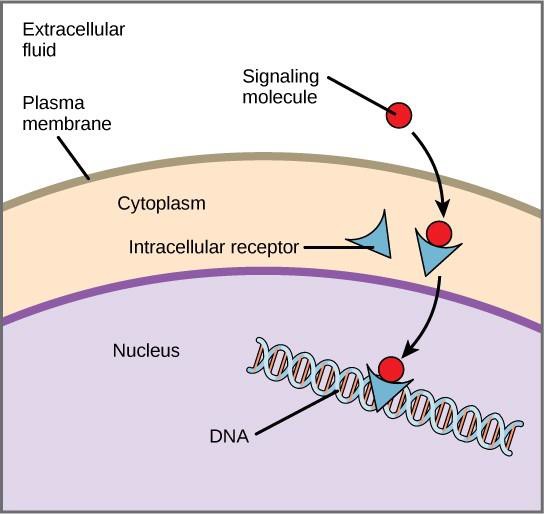
Cell-surface-receptorer
Cell-surface-receptorer, også kendt som transmembranreceptorer, er integrale proteiner, der binder til eksterne signalmolekyler. Disse receptorer spænder over plasmamembranen og udfører signaltransduktion, hvor et ekstracellulært signal omdannes til et intercellulært signal. (Figur 9.5). Da receptorproteiner på celleoverfladen er grundlæggende for cellens normale funktion, bør det ikke komme som nogen overraskelse, at en fejlfunktion i et af disse proteiner kan have alvorlige konsekvenser. Fejl i proteinstrukturerne for visse receptormolekyler har vist sig at spille en rolle i hypertension (højt blodtryk), astma, hjertesygdomme og kræft.
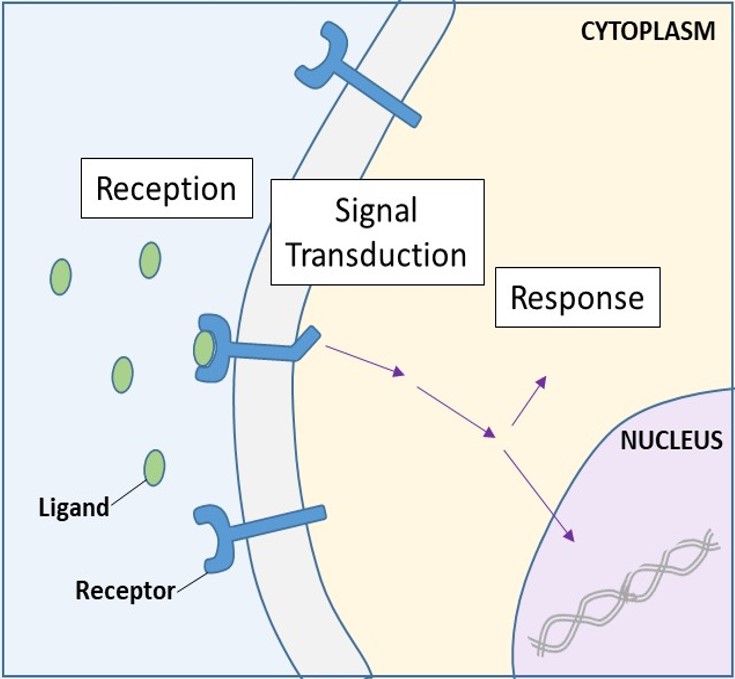
Hver receptor på celleoverfladen har tre hovedkomponenter: et eksternt ligandbindingsdomæne eller ekstracellulært domæne; et hydrofobt membranoverskridende område; og et intracellulært domæne. Celleoverfladereceptorer er involveret i det meste af signaleringen i flercellede organismer. Der findes tre generelle kategorier af receptorer på celleoverfladen: enzymbundne receptorer, ionkanalbundne receptorer og G-proteinbundne receptorer.
Enzymbundne receptorer er receptorer på celleoverfladen med intracellulære domæner, som er associeret med et enzym. I nogle tilfælde er selve det intracellulære domæne af receptoren et enzym. Andre enzymrelaterede receptorer har et lille intracellulært domæne, der interagerer direkte med et enzym. Enzymbundne receptorer har normalt store ekstracellulære og intracellulære domæner, men det membranoverskridende område består af en enkelt alfa-helix i peptidstrengen.
Når en ligand binder til det ekstracellulære domæne af en enzymbunden receptor, overføres et signal gennem membranen, hvorved enzymet aktiveres. Aktivering af enzymet sætter en kæde af begivenheder i gang i cellen, som i sidste ende fører til et respons.
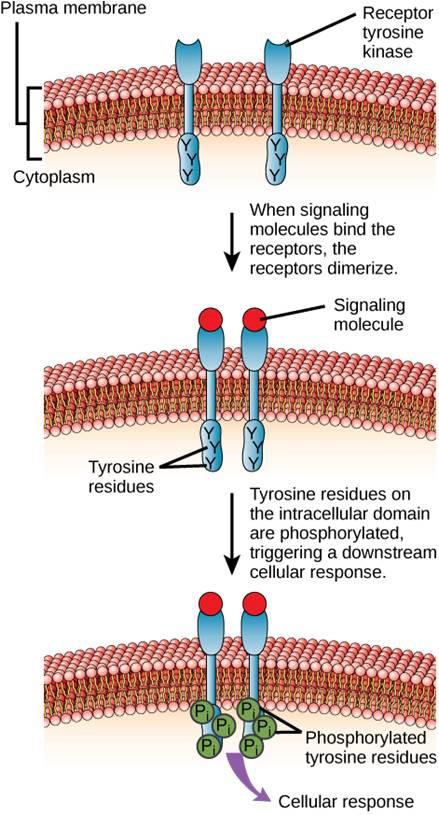
Et eksempel på en enzymbunden receptor er tyrosinkinase-receptoren (figur 9.6). En kinase er et enzym, der overfører fosfatgrupper fra ATP til et andet protein. Tyrosinkinase-receptoren overfører fosfatgrupper til tyrosinmolekyler. Først binder signalmolekyler sig til det ekstracellulære domæne af to nærliggende tyrosinkinase-receptorer. De to nærliggende receptorer bindes derefter sammen eller dimeriseres. Derefter tilføjes fosfater til tyrosinrester på receptorernes intracellulære domæne (fosforylering). De fosforylerede rester kan derefter overføre signalet til den næste budbringer i cytoplasmaet.
Epidermale vækstfaktorreceptorer er et eksempel på receptortyrosinkinaser, der følger denne måde at signalere på. Defekter i ErbB-signalering i denne familie kan føre til neuromuskulære sygdomme som f.eks. multipel sklerose og Alzheimers sygdom.
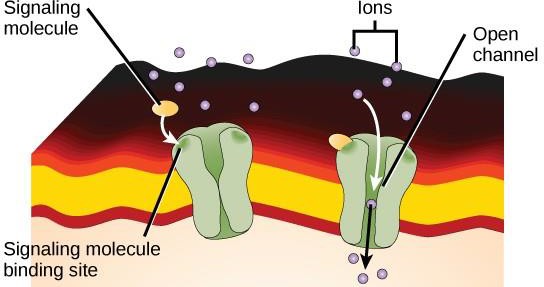
Ion-kanal-relaterede receptorer binder sig til en ligand og åbner en kanal gennem membranen, som tillader specifikke ioner at passere. Denne type receptor på celleoverfladen har en omfattende membranoverskridende region med hydrofobiske aminosyrer. Omvendt er de aminosyrer, der beklæder kanalens inderside, hydrofile for at muliggøre passage af ioner. Når en ligand binder sig til kanalens ekstracellulære område, sker der en konformationsændring i proteinets struktur, som tillader ioner som natrium, calcium, magnesium eller hydrogen at passere (figur 9.7).
G-protein-knyttede receptorer binder til en ligand og aktiverer et tilknyttet G-protein. Det aktiverede G-protein interagerer derefter med et nærliggende membranprotein, som kan være en ionkanal eller et enzym (figur 9.8). Alle G-proteinbundne receptorer har syv transmembrandomæner, men hver receptor har et specifikt ekstracellulært domæne og et G-proteinbindingssted.
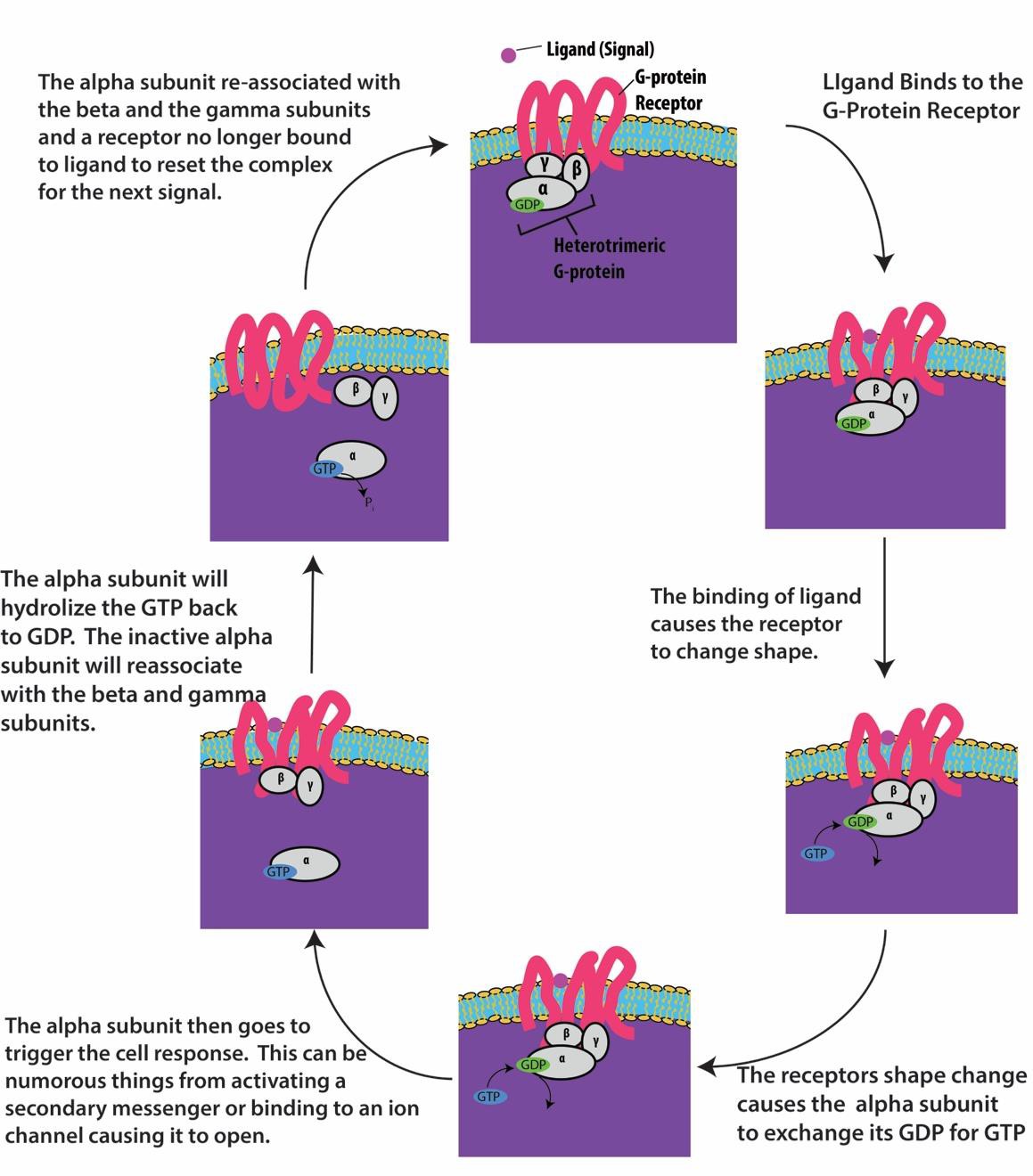
Cellens signalering ved hjælp af G-proteinkoblede receptorer foregår som en cyklus. Når liganden binder til receptoren, aktiverer den deraf følgende formændring G-proteinet, som frigiver GDP og optager GTP. G-proteinets underenheder deler sig derefter i α- og βγ-underenheder. En eller begge af disse G-proteinfragmenter kan være i stand til at aktivere andre proteiner i cellen. Efter et stykke tid hydrolyseres GTP’en på den aktive α-underenhed af G-proteinet til GDP, og βγ-underenheden deaktiveres. Underenhederne associeres igen for at danne det inaktive G-protein, og cyklussen begynder igen (figur 9.8).
G-proteintilknyttede receptorer anvendes i mange fysiologiske processer, herunder dem til synstransduktion, smag og regulering af immunsystemet og inflammation.

HER2 er en receptortyrosinkinase. I 30 procent af de menneskelige brystkræftformer er HER2 permanent aktiveret, hvilket resulterer i ureguleret celledeling. Lapatinib, et lægemiddel, der anvendes til behandling af brystkræft, hæmmer den proces, hvorved receptoren fosforylerer sig selv, og reducerer dermed tumorvæksten med 50 procent. Hvilke af følgende trin ville blive hæmmet af Lapatinib?
- Signalmolekylebinding, dimerisering og det nedstrøms cellulære respons
- Dimerisering og det nedstrøms cellulære respons
- Det nedstrøms cellulære respons
- Phosphataseaktivitet, dimerisering og det nedstrøms cellulære respons
9.1.3 Signalmolekyler
Ligander, der produceres af signalceller, er kemiske signaler, der bevæger sig til målceller og forårsager et respons. De typer af molekyler, der tjener som ligander, er utroligt varierede og spænder fra små proteiner til små ioner. Ligander kategoriseres som enten små hydrofobiske ligander, som kan krydse plasmamembraner, eller vandopløselige ligander, som ikke kan det.
Små hydrofobiske ligander
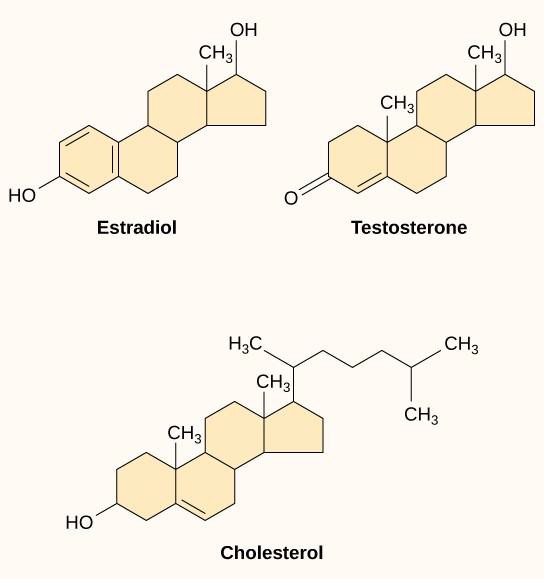
Små hydrofobiske ligander, også kaldet lipidopløselige ligander, kan diffundere direkte gennem plasmamembranen og interagere med interne receptorer. Vigtige medlemmer af denne klasse af ligander er steroidhormonerne. Steroider er lipider, der har et kulstofskelet med fire sammensmeltede ringe; forskellige steroider har forskellige funktionelle grupper knyttet til kulstofskelettet. Steroidhormoner omfatter det kvindelige kønshormon østradiol, som er en type østrogen; det mandlige kønshormon testosteron; og kolesterol, som er en vigtig strukturel komponent i biologiske membraner og en forløber for steroidhormoner (figur 9.10). Andre hydrofobiske hormoner omfatter skjoldbruskkirtelhormoner og D-vitamin. For at være opløselige i blodet skal hydrofobiske ligander binde sig til bæreproteiner, mens de transporteres gennem blodbanen.
Vandopløselige ligander
Da vandopløselige ligander er polære, kan de ikke passere gennem plasmamembranen uden hjælp. Nogle gange er de for store til at kunne passere gennem membranen overhovedet. I stedet binder de fleste vandopløselige ligander sig til det ekstracellulære domæne af receptorer på celleoverfladen (se figur 9.5). Denne gruppe af ligander er ret forskelligartet og omfatter små molekyler, peptider og proteiner.
9.2 | Signalets udbredelse
I slutningen af dette afsnit vil du kunne:
- Forklare, hvordan bindingen af en ligand igangsætter signaltransduktion i hele cellen.
- Erkende, at intracellulære signaler overføres ved hjælp af fosforylering eller sekundære budbringere.
Når et vandopløseligt ligand binder til sin receptor, overføres signalet gennem membranen og ind i cytoplasmaet. Fortsættelse af et signal på denne måde kaldes signaltransduktion (figur 9.5). Signaltransduktion sker kun med receptorer på celleoverfladen, da interne receptorer er i stand til at komme ind i cellen.
Når en ligand binder til sin receptor, sker der konformationsændringer, der påvirker receptorens intracellulære domæne. Disse konformationelle ændringer fører til aktivering af det intracellulære domæne eller dets tilknyttede proteiner. I nogle tilfælde medfører binding af liganden dimerisering af receptoren, hvilket betyder, at to receptorer binder sig til hinanden for at danne et stabilt kompleks kaldet en dimer. En dimer er en kemisk forbindelse, der dannes, når to molekyler (ofte identiske) forbindes med hinanden. Bindingen af receptorerne på denne måde gør det muligt for deres intracellulære domæner at komme i tæt kontakt og aktivere hinanden.
9.2.2.1 Signalveje og signalforstærkning
Selv om signalmolekyler ofte findes i meget lave koncentrationer, kan de have dybtgående virkninger. Efter at liganden binder til receptoren på celleoverfladen, sætter aktiveringen af receptorens intracellulære komponenter en kæde af begivenheder i gang, som kaldes en signalvej eller en signalkaskade. I en signalvej aktiverer sekundære budbringere, enzymer og/eller aktiverede proteiner andre proteiner eller budbringere (figur 9.11). Hvert medlem af signalvejen kan aktivere tusindvis af det næste medlem af signalvejen i en proces, der kaldes signalforstærkning. Da signalet forstærkes ved hvert trin, kan der genereres et meget stort respons fra en enkelt receptor, der binder en ligand.
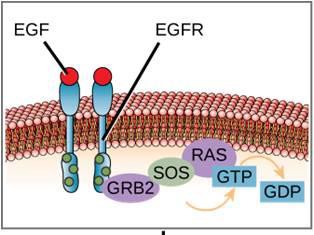
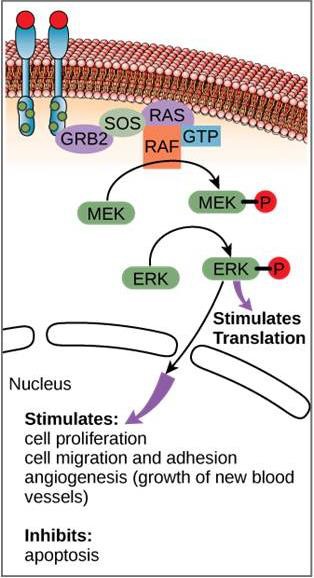
Et eksempel på en signalvej er vist i figur 9.11. Epidermal vækstfaktor (EGF) er et signalmolekyle, der er involveret i reguleringen af cellevækst, sårheling og vævsreparation. Receptoren for EGF (EGFR) er en tyrosinkinase. En aktiveret kinase fosforylerer og aktiverer mange nedstrømsmolekyler. Når EGF binder til EGFR, signalerer en kaskade af nedstrømsfosforyleringsbegivenheder, at cellen skal vokse og dele sig. Hvis EGFR aktiveres på uhensigtsmæssige tidspunkter, kan der opstå ukontrolleret cellevækst (kræft).
I visse kræftformer er GTPaseaktiviteten af RAS G-proteinet G-proteinet hæmmet. Det betyder, at RAS-proteinet ikke længere kan hydrolyserer GTP til GDP. Hvilken virkning vil dette have på nedstrøms cellulære hændelser?
9.2.2 Metoder til intracellulær signalering
Induktionen af en signalvej afhænger af et enzyms modifikation af en cellulær komponent. Der er mange enzymatiske modifikationer, der kan forekomme for at aktivere den næste komponent i signalvejen. Følgende er nogle af de mere almindelige hændelser i intracellulær signalering.
Fosforylering
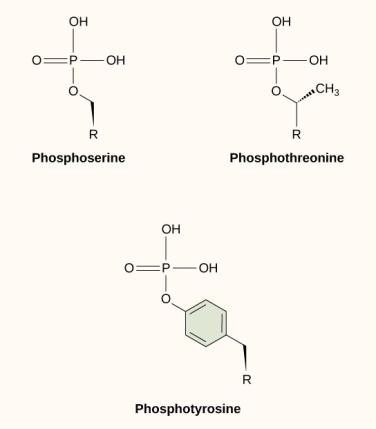
En af de mest almindelige kemiske modifikationer, der forekommer i signalveje, er tilføjelsen af en fosfatgruppe til et molekyle i en proces kaldet fosforylering. Fosfatet kan tilføjes til et nukleotid som f.eks. GMP for at danne GDP eller GTP. Fosfater tilføjes også ofte til serin-, threonin- og tyrosinrester i proteiner, hvor de erstatter hydroxylgruppen i aminosyren (figur 9.12). Overførslen af fosfatet katalyseres af et enzym, der kaldes en kinase. Fosforylering kan aktivere eller inaktivere enzymer, og omvendelse af fosforylering, affosforylering, vil vende effekten.
Sekundbudbringere
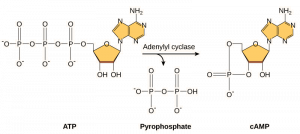
Sekundbudbringere er små molekyler, der viderefører et signal, efter at det er blevet igangsat ved at signalmolekylet er blevet bundet til receptoren. Disse molekyler hjælper med at sprede et signal gennem cytoplasmaet ved at ændre visse cellulære proteiners adfærd. En anden budbringer, der anvendes af mange forskellige celletyper, er cyklisk AMP (cAMP). Cyklisk AMP syntetiseres af enzymet adenylylcyklase ud fra ATP (figur 9.13). Den vigtigste rolle for cAMP i cellerne er at binde sig til og aktivere et enzym kaldet cAMP-afhængig kinase (A-kinase). A-kinase regulerer mange vitale metaboliske veje: Det fosforylerer serin- og threoninrester af sine målproteiner og aktiverer dem i processen. A-kinase findes i mange forskellige celletyper, og målproteinerne i de enkelte celletyper er forskellige. En anden sekundær budbringer er Ca2+som kan frigives for at oversvømme cellen.
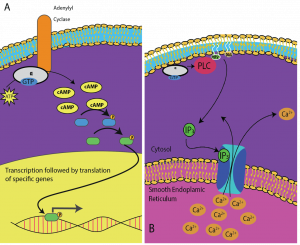
Differente celler reagerer forskelligt på cAMP. I figur 9.14 er alfa-underenheden fra en G-proteinreceptor vist, som aktiverer to forskellige typer signalering. I det første billede produceres cAMP af enzymet adenylatcyklase, når det aktiveres af alfa-underenheden. cAMP aktiverer derefter andre proteiner, der påvirker gentranskriptionen. På det andet billede udløser alfa-underenheden fra G-proteinet en kaskade, der frigør Ca2+ fra det glatte endoplasmatiske reticulum. I dette tilfælde er Ca2+ den sekundære budbringer, der forårsager det cellulære respons.
9.3 | Svar på signalet
Ved afslutningen af dette afsnit vil du kunne:
- Erkende, at signalveje styrer proteinekspression, cellulær metabolisme og cellevækst.
- Erkende apoptosens rolle i udviklingen og vedligeholdelsen af en sund organisme.
Med hjælp af signaltransduktionsveje frembringer receptorer i plasmamembranen en række forskellige virkninger på cellen. Inde i cellen binder ligandene sig til deres interne receptorer, hvilket giver dem mulighed for at påvirke cellens DNA og proteinproducerende maskineri direkte. Resultaterne af signalvejene er yderst varierede og afhænger af den pågældende celletype samt af de ydre og indre forhold. Et lille udsnit af reaktioner er beskrevet nedenfor.
9.3.3.1 Reaktioner på signalvejen
Genekspression
Nogle signaltransduktionsveje regulerer transkriptionen af RNA. Andre regulerer oversættelsen af proteiner.
Stigning i cellulær metabolisme
Aktiveringen af β-adrenerge receptorer i muskelceller ved hjælp af adrenalin fører til en stigning i cyklisk AMP inde i cellen. Adrenalin er et hormon, der produceres af binyrerne, og som gør kroppen klar til kortvarige nødsituationer.
Cellevækst
Cellens signalveje spiller også en vigtig rolle i celledelingen. Celler deler sig normalt ikke, medmindre de bliver stimuleret af signaler fra andre celler. De ligander, der fremmer cellevækst, kaldes vækstfaktorer. De fleste vækstfaktorer binder sig til receptorer på celleoverfladen, der er knyttet til tyrosinkinaser.
Celledød
Når en celle er beskadiget, overflødig eller potentielt farlig for en organisme, kan en celle iværksætte en mekanisme, der udløser programmeret celledød eller apoptose. Apoptose gør det muligt for en celle at dø på en kontrolleret måde, der forhindrer frigivelse af potentielt skadelige molekyler fra cellens indre. I nogle tilfælde, f.eks. i forbindelse med en virusinfektion eller ukontrolleret celledeling på grund af kræft, svigter cellens normale kontrolmekanismer imidlertid. Ekstern signalering kan også udløse apoptose. F.eks. har de fleste normale dyreceller receptorer, der interagerer med den ekstracellulære matrix, et netværk af glykoproteiner, som giver strukturel støtte til dyreceller. Når cellulære receptorer binder sig til den ekstracellulære matrix, starter en signalkaskade i cellen. Men hvis cellen bevæger sig væk fra den ekstracellulære matrix, ophører signalgivningen, og cellen undergår apoptose. Dette system er med til at forhindre, at celler rejser gennem kroppen og formerer sig ukontrolleret, som det sker med tumorceller, der danner metastaser.
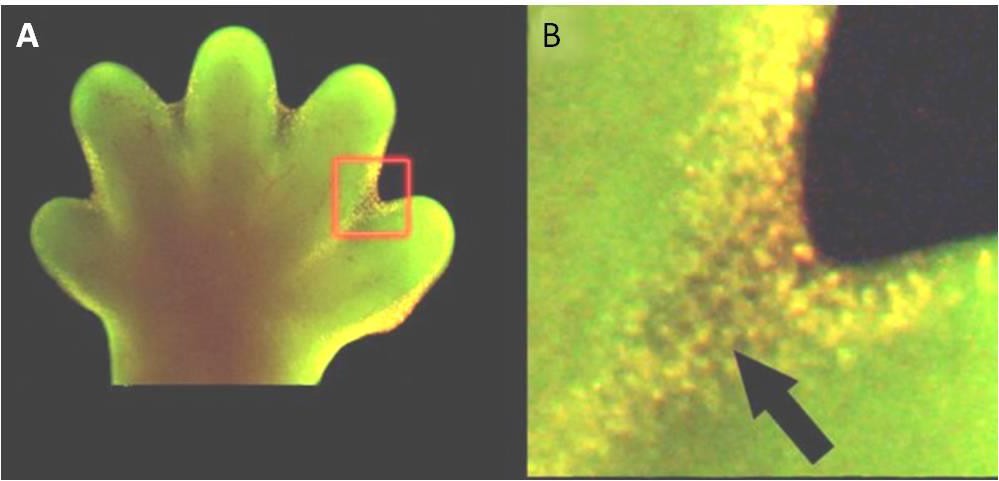
Apoptose er også afgørende for en normal embryologisk udvikling. Hos hvirveldyr omfatter de tidlige udviklingsstadier f.eks. dannelsen af netlignende væv mellem de enkelte fingre og tæer (figur 9.15). I løbet af den normale udvikling skal disse unødvendige celler elimineres, således at der kan dannes fuldt adskilte fingre og tæer. En cellesignalmekanisme udløser apoptose, som ødelægger cellerne mellem de udviklende fingre.
9.3.2 Afslutning af signalveje
Den afvigende signalering, der ofte ses i tumorceller, er et bevis på, at afslutningen af et signal på det rette tidspunkt kan være lige så vigtig som initieringen af et signal. En metode til at standse et specifikt signal er at nedbryde liganden eller fjerne den, så den ikke længere kan få adgang til sin receptor. En af grundene til, at hydrofobiske hormoner som østrogen og testosteron udløser langvarige hændelser, er, at de binder sig til bæreproteiner. Disse proteiner gør det muligt for de uopløselige molekyler at være opløselige i blodet, men de beskytter også hormonerne mod nedbrydning af cirkulerende enzymer.
Inden for cellen vender mange forskellige enzymer de cellulære modifikationer, der er resultatet af signalkaskaderne, tilbage. F.eks. er fosfataser enzymer, der fjerner den fosfatgruppe, der er knyttet til proteiner af kinaser i en proces kaldet defosforylering. cAMP nedbrydes til AMP af fosfodiesterase, hvorved dets signal afsluttes. På samme måde omgøres frigivelsen af calciumlagre af Ca2+-pumper, der er placeret i cellemembranerne.