Se eu lhe perguntar o que lhe vem à cabeça no instante em que ouve a palavra QUÍMICA, tenho quase a certeza que se vai imaginar de pé num laboratório de química e a segurar diferentes instrumentos de laboratório. Não é? Mas se você olhar atentamente para o mundo ao seu redor, infinitas reações químicas estão ocorrendo a qualquer segundo. Assim, pode-se dizer com razão que a química constitui uma grande parte da sua vida diária. A química e as reacções químicas não se limitam apenas aos laboratórios, mas também ao mundo à sua volta. O elemento carbono forma a unidade básica dos compostos orgânicos, inorgânicos e organometálicos. No momento em que você vai dormir até acordar, processos químicos infinitos estão ocorrendo em cada célula do seu corpo. Mesmo os processos ocorrem quando você acorda, todas as suas atividades diárias como beber água, tomar um banho, cozinhar sua comida, limpar seu carro, rir ou chorar são guiados por diferentes processos químicos. Vamos discutir alguns exemplos de química que ocorrem ao nosso redor:
1. Composição corporal
Seu corpo é um lugar fascinante. O carbono e o oxigénio são os dois elementos mais essenciais do corpo. Os outros elementos que estão presentes no seu corpo são azoto, fósforo, hidrogénio, oxigénio, cálcio, potássio, enxofre, magnésio, etc.
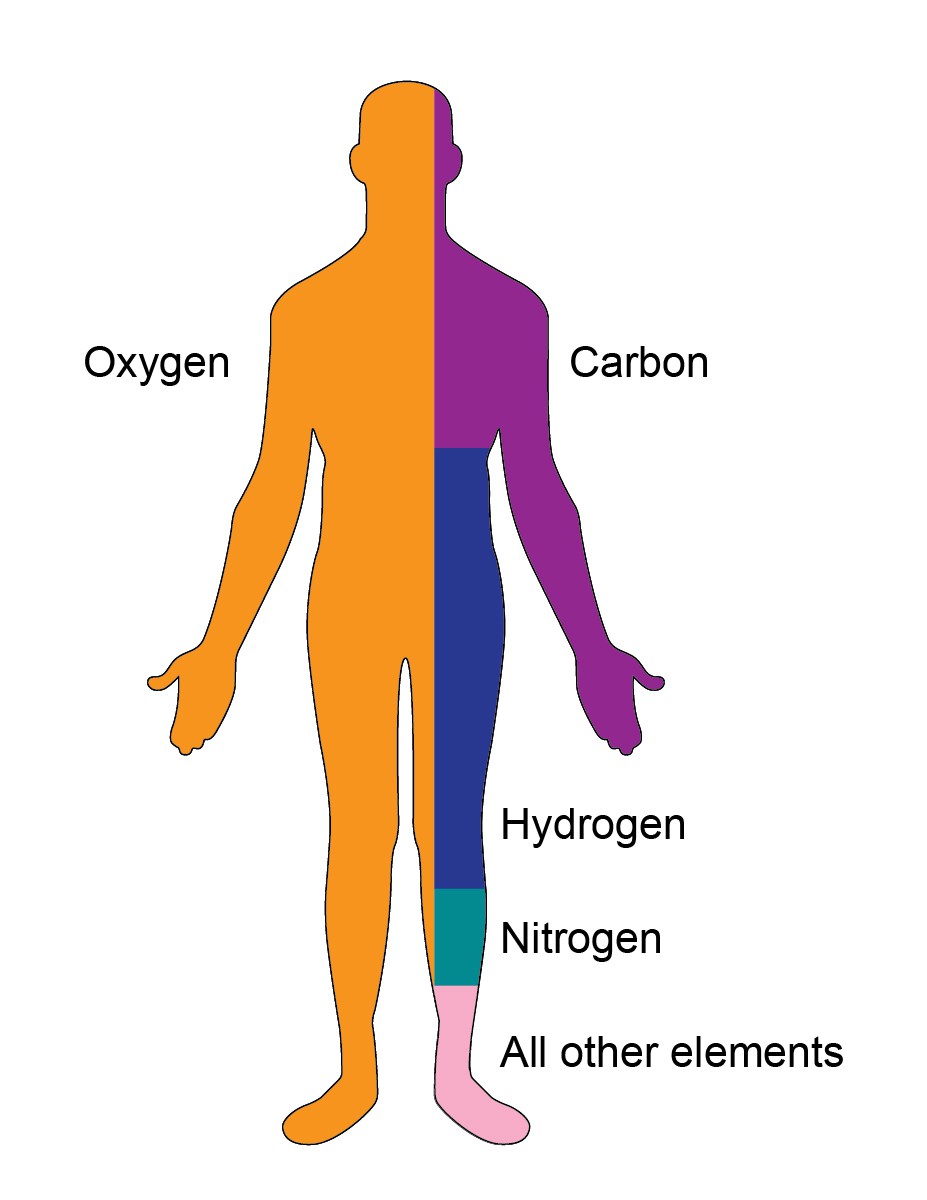
| ELEMENTO | PERCENTAGEM NO CORPO | FUNÇÃO |
|---|---|---|
| Oxygen (O) | 65 | -Solvente primário -Temperatura de regulação &Pressão osmótica |
| Carbono (C) | 18 | -Fonte de energia -Blocos de construção do corpo |
| Hidrogénio (H) | 10 | -Presente na água e todo orgânico moléculas |
| Nitrogénio (N) | 3 | -fundidos em proteínas e ácidos nucleicos |
| Cálcio (Ca) | 1.5 | -Critical for muscle contraction |
| Fósforo (P) | 1.0 | -Atos como amortecedor Provê força e estrutura aos ossos e dentes |
| Potássio (K) | 0.35 | Electrólito de cristais -Ajuda na transmissão do impulso nervoso -Regula o batimento cardíaco |
| Sulfur (S) | 0.25 | -Renviar forma às proteínas que ajudam no bom funcionamento das proteínas |
| Sódio (Na) | 0.15 | -Importante eletrólito para regular a quantidade de água -Ajuda na sinalização nervosa |
| Magnésio (Mg) | 0.05 | Requerido em mais de 300 reações bioquímicas -Builds muscle and bones -Cofeitor em muitas reações enzimáticas |
| Iron (Fe) | 0.006 | Ajuda na produção de sangue |
| Cobre (Cu), Zinco (Zn), Selenium (Se), Molibdénio (Mb), Fluorina (F), Iodo (I), Manganês (Mn), Cobalto (Co) |
Total é inferior a 0.70 | Cobre é um micronutriente para o crescimento e desenvolvimento, e também essencial para várias funções metabólicas -Zinco desempenha um papel importante no crescimento celular, divisão celular, cicatrização de feridas, e a decomposição dos carboidratos -Selenium protege o organismo dos danos oxidativos -Molibdénio remove toxinas do metabolismo do enxofre contendo aminoácidos -Fluorina é responsável pela mineralização e formação do esmalte dentário -Iodo é essencial para a formação de hormonas da tiróide -Manganês ajuda na formação dos tecidos conjuntivos, ossos, fatores de coagulação do sangue, hormônios sexuais além de serem críticos no metabolismo de gorduras e carboidratos, absorção de cálcio e regulação do açúcar no sangue |
| Lithium (Li), Strontium (Sr), Alumínio (Al), Silício (Si), Lead (Pb), Arsênio (As), Vanádio (V), Bromo (Br) |
Presente em quantidades vestigiais | -Lítio é essencial para a manutenção da saúde neurológica -Strontório auxilia na formação óssea e previne a perda óssea; a forma radioativa do estrôncio também pode matar algumas células cancerígenas -Alumina é responsável pela compactação da cromatina -Silício ajuda a promover firmeza e força nas artérias, tecidos conjuntivos, tendões, pele e olhos -Vanádio desempenha um papel nas enzimas metabolizadoras |
2. Química das Emoções

Quando você está se sentindo feliz, triste, extasiado, relaxado ou estressado, há muitas reações químicas ocorrendo em seu corpo. É por causa dos mensageiros químicos chamados neurotransmissores liberados no cérebro que você pode se apaixonar e chorar rios por causa do desgosto do coração. 
3. Química na Produção de Alimentos
As plantas produzem alimentos para si mesmas através da fotossíntese; que é uma reação química complexa em si mesma. A reação química que ocorre na fotossíntese é a reação química mais comum e vital. Os animais também libertam energia para realizar actividades diárias através de reacções químicas respiratórias semelhantes.
6 CO2 + 6 H2O + luz → C 6H12O6 + 6 O2

4. Química em Higiene
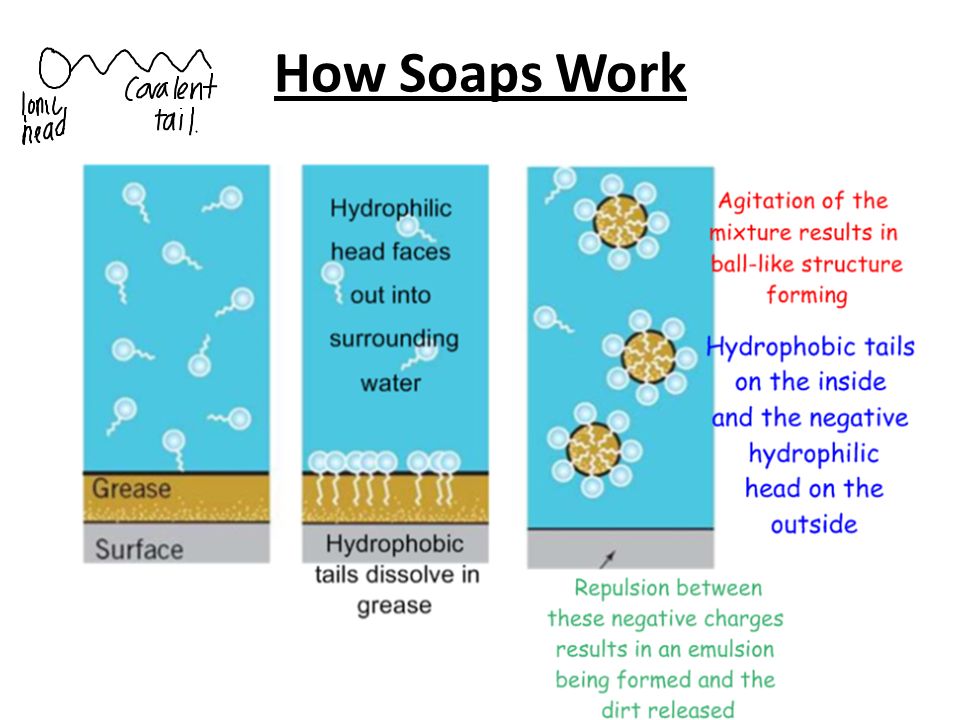
5. A Química da Cebola


6. Química na Panificação


7. Química em conservantes alimentares


8. Química na Digestão

9. O funcionamento de um protector solar


10. Química na Formação da Ferrugem
Fe + O2 + H2O → Fe2O3. XH2O