Historia clínica
Dos pacientes con deficiencia de ornitina transcarbamilasa, un trastorno del ciclo de la urea, fueron trasladados a nuestra unidad de cuidados intensivos en 12 meses. Ambos eran hombres previamente sanos que inicialmente se presentaron con síntomas neurológicos anodinos pero progresivos después de procedimientos menores (resúmenes de casos en el Recuadro 1).
Cada paciente desarrolló sus síntomas neurológicos iniciales (cefalea, lentitud mental, incoordinación) unas 24-48 horas después del probable precipitante, que en cada caso fue una dosis única de un corticosteroide. En el paciente 1, la somnolencia a las 48 horas evolucionó hacia la incoherencia, la visión borrosa y la agitación grave que requirió la intubación 2 días después. En el Paciente 2, la cefalea, las náuseas, la visión borrosa y el dolor epigástrico a las 48 horas progresaron durante los 2 días siguientes a confusión y lentitud en el habla; al día siguiente, se produjo un coma que requirió intubación.
En su presentación en un hospital periférico, se había llevado a cabo un amplio panel de investigaciones patológicas para cada paciente, incluyendo análisis de sangre (recuento sanguíneo completo, pruebas de función renal, niveles de enzimas hepáticas, perfil de coagulación y marcadores inflamatorios), punción lumbar e imágenes cerebrales (tomografía computarizada y resonancia magnética). Los resultados de estas investigaciones fueron todos irrelevantes.
La identificación de la hiperamonemia significativa se retrasó hasta unas 36-48 horas después de la presentación en el hospital. Los pacientes estaban en coma cuando fueron trasladados a nuestro hospital. El paciente 1 tuvo una estancia prolongada en nuestra unidad de cuidados intensivos, con un estado de consciencia mínima persistente; el paciente 2 procedió a la muerte cerebral y a la donación de órganos.
Los médicos estarán familiarizados con las causas más comunes de hiperamoniemia, incluyendo un aumento de la carga proteica asociada a la enfermedad hepática, y la disfunción de las enzimas del ciclo de la urea causada por medicamentos como el valproato sódico. Las causas menos comunes pero importantes de niveles elevados de amoníaco en sangre son los trastornos hereditarios del ciclo de la urea (TCE). Las formas más graves se presentan en los primeros años de vida, pero las formas más leves de estos trastornos pueden hacerse evidentes durante la edad adulta.
Los TCU son un grupo de errores innatos del metabolismo, con una incidencia total estimada de entre 1:80001 y 1:30 0002 nacimientos. Están causados por la disfunción de cualquiera de las seis enzimas o dos proteínas transportadoras que intervienen en la biosíntesis de la urea, un proceso que ocurre predominantemente en el hígado. El ciclo de la urea es la vía terminal para la eliminación del amoníaco formado durante el catabolismo de los aminoácidos. El amoníaco es neurotóxico, y cualquier aumento agudo de los niveles en sangre por encima de 50 μmol/L puede provocar síntomas neurológicos. Mientras que los niveles de amoníaco por encima de 100 μmol/L pueden causar obtusión, las elevaciones más leves deben interpretarse dentro del contexto clínico de su aparición.
La ECU que afectaba a nuestros dos pacientes era la deficiencia de ornitina transcarbamilasa (OTC), el más común de los trastornos del ciclo de la urea. La deficiencia de OTC es un rasgo ligado al cromosoma X y, por lo tanto, se expresa más comúnmente en los varones, aunque las mujeres portadoras pueden descompensarse después de un estrés importante, como el parto.3 Las otras UCD son rasgos autosómicos recesivos.4
La primera presentación en la edad adulta puede atribuirse al grado más leve de la deficiencia y, con frecuencia, también a la autolimitación de la ingesta de proteínas como comportamiento aprendido, lo que permite la estabilidad hasta que sobreviene un factor de estrés ambiental. Las condiciones que provocan un aumento de las demandas del ciclo de la urea, como la carga de proteínas, la infección, los corticosteroides sistémicos, la pérdida rápida de peso, la cirugía, los traumatismos y la quimioterapia5 , pueden precipitar la descompensación en individuos con una UCD. El caso de un hombre de 44 años que murió de una deficiencia de OTC no diagnosticada previamente después de una cirugía de bypass de la arteria coronaria se informó en esta revista en 2007.6
En los dos pacientes descritos en nuestro artículo, una única pero significativa dosis incidental de corticosteroides fue el evento precipitante inicial, con un ayuno prolongado que perpetuó un ciclo metabólico vicioso que culminó en una hiperamonemia grave.
La hiperamonemia en adultos puede presentarse con síntomas psiquiátricos o neurológicos, incluyendo cefalea, confusión, agitación con comportamiento combativo, disartria, ataxia, alucinaciones y deterioro visual,3 síntomas que reflejan una encefalopatía metabólica tóxica. Los síntomas abdominales (náuseas, vómitos) pueden acompañar a los fenómenos del sistema nervioso.
Nuestros dos casos ilustran el curso de la hiperamoniemia progresiva si no se inicia el tratamiento de forma precoz: empeoramiento del deterioro cognitivo y del edema cerebral, con desarrollo de coma, convulsiones y muerte por hipertensión intracraneal.
Cuando no hay una explicación alternativa para la naturaleza desproporcionada y progresiva de la alteración cognitiva de un paciente, esto debe tomarse como una pista importante para explorar la posibilidad de una etiología metabólica. Dado que el deterioro se produce a lo largo de varios días, existe la posibilidad de intervenir para salvar la vida del paciente si se detecta la enfermedad a tiempo.
En estos casos, la medición del nivel de amoníaco en sangre como parte de un análisis metabólico debe realizarse lo antes posible. Si el nivel de amoníaco es elevado, debe consultarse a un especialista en metabolismo, preparar un perfil de aminoácidos en plasma, medir los ácidos orgánicos y el ácido orótico en orina e iniciar un tratamiento de emergencia para la hiperamonemia.
Los tres elementos del tratamiento de un coma hiperamonémico ligado al ciclo de la urea incluyen:
-
eliminación física del amoníaco mediante hemodiálisis o hemodiafiltración;
-
reversión del estado catabólico mediante infusión de insulina/dextrosa e intralípidos; y
-
retención temporal de proteínas e inicio de eliminadores de nitrógeno, una vez disponibles.
Estas medidas deben iniciarse bajo la dirección de un médico especialista en metabolismo, y en una unidad de cuidados intensivos en la que pueda controlarse la agitación o el coma. Los niveles de amoníaco pueden reducirse rápidamente mediante diálisis; su eliminación depende de las tasas de flujo, lo que hace que la hemodiálisis intermitente sea el método más eficaz de eliminación, como se muestra en el cuadro 2. Por esta razón, abogamos por la diálisis intermitente en lugar de la hemodiafiltración venovenosa continua para el control temprano del amoníaco en el contexto de la emergencia.
Aunque el deterioro neurológico grave al inicio del tratamiento es muy preocupante, esto no debería ser en sí mismo una razón para suspender el tratamiento, ya que es posible una buena recuperación neurológica. Esto queda ilustrado por el informe de un caso de un paciente de mediana edad que se recuperó, a pesar de la postura decorticada cuando se inició la terapia.5
Abogamos por la evaluación temprana de los niveles de amoníaco en pacientes con un estado de conciencia alterado inexplicable, o cuando su alteración cognitiva parece desproporcionada a cualquier enfermedad sistémica concurrente. Muchos de los elementos necesarios de la atención pueden iniciarse en unidades de cuidados intensivos no terciarias. El inicio del tratamiento en el hospital de presentación es esencial, ya que se trata de una emergencia médica; el resultado neurológico y la supervivencia dependen críticamente del momento de la intervención. Si se reconocen a tiempo y se tratan adecuadamente, el pronóstico de recuperación neurológica es bueno.
Lecciones para la práctica
-
Los trastornos del ciclo de la urea pueden presentarse por primera vez en la edad adulta, desenmascarados por factores desencadenantes como una enfermedad sistémica, un aumento de la carga proteica, una intervención quirúrgica o los corticosteroides.
-
La evaluación de los niveles de amoníaco es una prueba sencilla pero fundamental en los pacientes con una alteración inexplicable de la conciencia.
-
Una sesión de hemodiálisis intermitente es muy eficaz para el control rápido del amoníaco, y superior a la hemodiafiltración continua para una corrección rápida.
-
El tratamiento de emergencia de la hiperamoniemia debe llevarse a cabo de forma precoz para evitar lesiones neurológicas devastadoras.
Caja 1 – Historias clínicas de los dos pacientes
Paciente 1: 24 años, varón
Antecedentes médicos
- Apnea obstructiva del sueño; sin antecedentes familiares destacables; individuo de alto funcionamiento
- Probable precipitante: dexametasona intraoperatoria (8 mg) durante la septoplastia nasal
Evolución
- Vagosidad y letargia 48 h después de la operación, progresando en 24 h a incoherencia
- Intubado 12 h después por agitación severa
- GCS disminuyó a 5-6 en las siguientes 48 h; nivel de amoníaco, 334 μmol/L (RR, < 50 μmol/L); se inició tratamiento específico de la enfermedad
- Se elevaron las presiones intracraneales 6 h después (pupilas dilatadas con edema cerebral en TAC cerebral), lo que llevó a una craniectomía descompresiva complicada por un hematoma frontal, requiriendo evacuación
- Prolongada estancia en la unidad de cuidados intensivos y en el hospital
Resultado
- Estado de mínima conciencia persistente (a los 22 meses)
- Dado de alta a centro de enfermería
- Análisis bioquímicos de plasma y orina consistentes con deficiencia de OTC (ácido orótico elevado; nivel de glutamina en plasma elevado; niveles de ornitina, citrulina y arginina bajos)
- Las pruebas genéticas confirmaron la mutación del gen OTC asociada a la deficiencia de OTC
Paciente 2: 39 años, varón
Antecedentes médicos
- Dolor crónico de rodilla; sin antecedentes familiares destacables; individuo de alto funcionamiento
- Probable precipitante: inyección de cortisona en la rodilla por dolor de rodilla
Progreso
- Dolor de cabeza, náuseas, dolor epigástrico, visión borrosa e incoordinación 48 h después de la inyección
- Progresó durante las siguientes 48 h a confusión, Discurso lento
- Disminución progresiva del GCS, requiriendo intubación
- Actividad convulsiva
- La repetición del TAC cerebral mostró edema cerebral
- Nivel de amoníaco: 652 μmol/L (RR, < 50 μmol/L); tratamiento específico de la enfermedad iniciado; monitor de presión intracraneal insertado; falta de control de la hipertensión intracraneal; decisión de paliar
Resultado
- Se procedió a la muerte cerebral y a la donación de órganos (excepto donación de hígado: contraindicada)
- Hallazgos bioquímicos consistentes con deficiencia de OTC (elevación profunda del ácido orótico en orina, nivel de glutamina en plasma alto, nivel de arginina bajo)
- Las pruebas genéticas confirmaron la mutación del gen OTC asociada a la deficiencia de OTC
GCS = puntuación de coma de Glasgow; RR = rango de referencia; TC = tomografía computarizada; OTC = ornitina transcarbamilasa.
Cuadro 2 – Niveles de amoníaco en nuestros dos pacientes, y su respuesta al tratamiento*
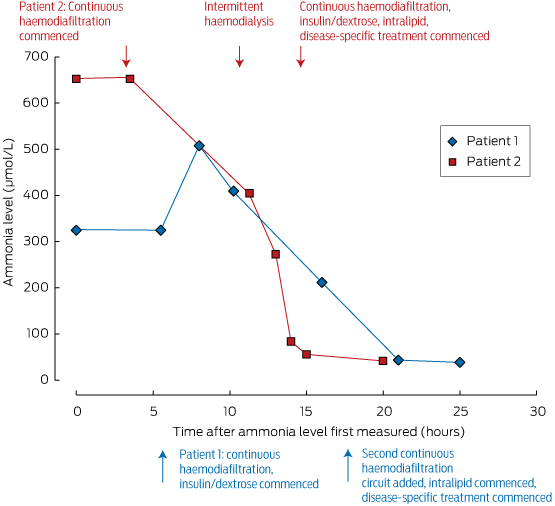
* Obsérvese el rápido ritmo de descenso de los niveles de amoníaco sérico en el paciente 2 conseguido tras iniciar la hemodiálisis intermitente (unas 10 horas después de la primera medición).